2021年6月18日、去る2月15日に承認された新規ジェネリック医薬品を中心とした様々な医薬品が薬価収載されました。
今回、新たに承認された後発医薬品はデュロキセチン(サインバルタ)、ジルムロ(ザクラス)、エスゾピクロン(ルネスタ)、ソリフェナシン(ベシケア)、タダラフィルAD(アドシルカ)、エピナスチン点眼(アレジオン点眼)、ブリモニジン点眼(アイファガン点眼)、パロノセトロン(アロキシ)、ペメトレキセド(アリムタ)の9種類です。
- 1 新登場のジェネリック医薬品
- 1.1 後発医薬品に関連する加算の対象となる範囲と時期
- 1.2 エスゾピクロン錠(ルネスタのジェネリック)
- 1.3 ジルムロ配合錠/OD錠(ザクラスのジェネリック)
- 1.4 ソリフェナシンコハク酸塩錠/OD錠(ベシケアのジェネリック)
- 1.5 タダラフィル錠AD(アドシルカのジェネリック)
- 1.6 デュロキセチンカプセル/錠/OD錠(サインバルタのジェネリック)
- 1.7 エピナスチン塩酸塩点眼液0.05%(アレジオン点眼液のジェネリック)
- 1.8 ブリモニジン酒石酸塩点眼液0.1%(アイファガン点眼液のジェネリック)
- 1.9 パロノセトロン静注/点滴静注(アロキシ静注/点滴静注のジェネリック)
- 1.10 ペメトレキセド点滴静注(アリムタのジェネリック)
- 2 新規格が登場した後発医薬品
- 3 薬価収載が見送られた後発医薬品
- 4 そのほか気になる薬価収載
- 5 所感
- 6 参考
新登場のジェネリック医薬品
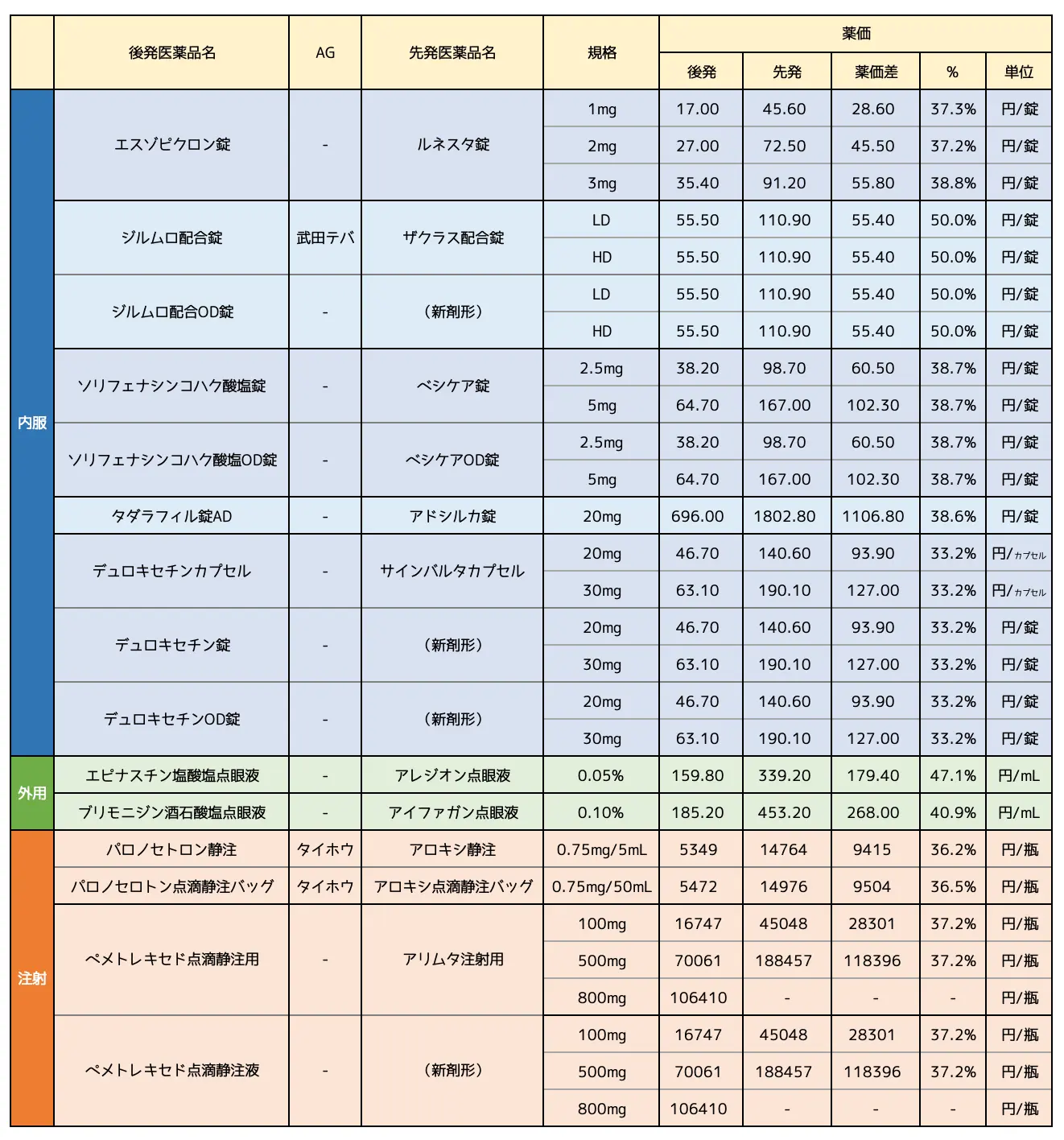
まずは今回の薬価収載の目玉。
ジェネリックが初めて登場するものについてまとめます。
承認時に投稿した過去記事もありますので興味があればどうぞ。
https://yakuzaishi.love/entry/generic-drugs-approval-20210215
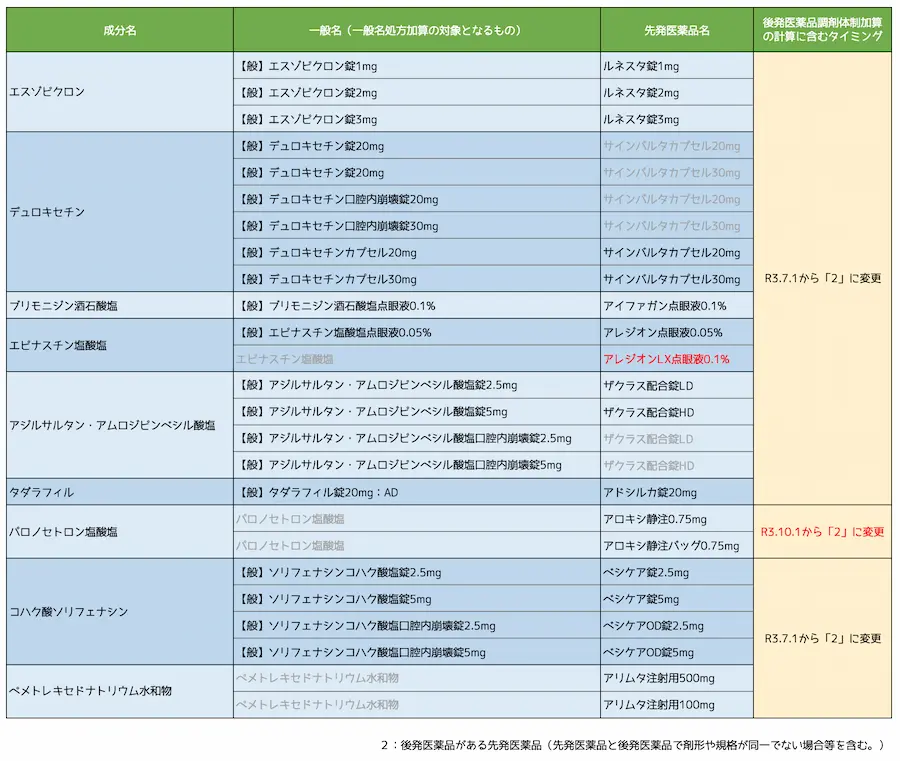
後発医薬品に関連する加算の対象となる範囲と時期
今回、薬価収載された後発医薬品に関連して、
- 一般名処方加算の対象となる一般名
- 後発医薬品調剤体制加算の計算(分母)に含まれる先発医薬品
をまとめました。
一般名処方加算の対象となる一般名については特に問題ないと思うのですが、みなさんが一番気になるのはアレジオンLX点眼液0.1%も令和3年7月1日から「後発医薬品がある先発医薬品」とみなされる点です。
パロノセトロン塩酸塩は薬価収載同時発売のものがないので3ヶ月遅れで計算に含まれるようになります。
エスゾピクロン錠(ルネスタのジェネリック)
まずはエスゾピクロン錠。ルネスタのジェネリックです。
エスゾピクロン錠は13社の製品が薬価収載されています。
以上、全13社
※「日医工」(日医工)は承認されていたが薬価収載されず
| 規格 | 後発:エスゾピクロン錠 収載時薬価(円/錠) | 先発:ルネスタ錠 R3年度薬価(円/錠) |
|---|---|---|
| 1mg | 17.00 | 45.60 |
| 2mg | 27.00 | 72.50 |
| 3mg | 35.40 | 91.20 |
薬価収載された製品数が10を超すため薬価は先発品の0.4掛け(40%)で計算されます。
ですが、エスゾピクロンの薬価を先発品のルネスタの薬価と比較してみると、1mgは37.3%、2mgは37.2%、3mgは38.8%となっています。
これはルネスタが新薬創出等加算(新薬創出・適応外薬解消等促進加算)の対象であるためです。
先発品であるルネスタの薬価から新薬創出等加算の累積加算分を引いてから0.4掛けされたため、後発医薬品の薬価はさらに安くなっています。
気になる共同販売は?
昨今の後発医薬品の供給問題で話題になった共同販売。
別の会社の製品だと思っていたのに、実際は共同販売が行われており、同じ製造元でしたってケースは今回も多そうです。
生物学的同等性試験のデータを比較してグループ分けしてみると・・・。
- グループ1:アメル、NPI、ケミファ
- グループ2:DSEP、トーワ、日新、明治、YD
- グループ3:サワイ、KMP
- グループ4:TCK、ニプロ、明治
といった具合になります。
ジルムロ配合錠/OD錠(ザクラスのジェネリック)
ジルムロ配合錠/OD錠。ザクラスのジェネリックです。
ジルムロ配合錠は8社、ジルムロ配合OD錠は2社の製品が薬価収載されています。
以上、全8社
※武田テバはAG(オーソライズドジェネリック)
以上、全2社
| 規格 | 後発:ジルムロ配合錠/配合OD錠 収載時薬価(円/錠) | 先発:ザクラス配合錠 R3年度薬価(円/錠) |
|---|---|---|
| LD | 55.50 | 110.90 |
| HD | 55.50 | 110.90 |
LD:アジルサルタン20mg/アムロジピン2.5mg、HD:アジルサルタン20mg/アムロジピン5mg
薬価収載された製品数が10を超さなかったため、ジルムロの薬価は先発品であるザクラスの0.5掛け(50%)で計算されています。
気になる共同販売は?
ジルムロについても共同販売がないか推察してみました。
生物学的同等性試験のデータを比較してグループ分けしてみると・・・。
共同販売と推察されるのは「YD」、「TCK」の2社のみでした。
他は全て単独っぽいです。
OD錠の大きさは?
先発品であるザクラス配合錠(普通錠)とジルムロ配合OD錠「トーワ」と「サワイ」を比較してみます。
| 医薬品名 | ザクラス配合錠LD ザクラス配合錠HD | ジルムロ配合OD錠LD「トーワ」 ジルムロ配合OD錠HD「トーワ」 | ジルムロ配合OD錠LD「サワイ」 ジルムロ配合OD錠HD「サワイ」 |
|---|---|---|---|
| 直径(mm) | 8.2 8.2 | 8.5 9.5 | 8.6 8.6 |
| 厚さ(mm) | 約4.7 約4.7 | 3.7 4.0 | 4.7 4.7 |
OD錠になるとどうしても少し大きくなりますが、HDを比較すると沢井製薬が少し有利かな?
アジルバのジェネリックが登場しない理由
ザクラス配合錠よりも先に発売されているアジルサルタン単剤であるアジルバ錠のジェネリックが登場しない理由ですが、小児用量に関する治験を実施するため、再審査期間が延長されているのが理由のようですね。(延長後の再審査期間:令和3年10月17日まで)
https://www.mhlw.go.jp/web/t_doc?dataId=00tc0816&dataType=1&pageNo=1
アジルバのジェネリックは再審査が終了後に登場するはずです。
早ければ年末に薬価収載されるかな?
ソリフェナシンコハク酸塩錠/OD錠(ベシケアのジェネリック)
ソリフェナシンコハク酸塩錠/OD錠。ベシケア錠/OD錠のジェネリックです。
ソリフェナシンコハク酸塩錠は4社、ソリフェナシンコハク酸塩OD錠は4社の製品が薬価収載されています。
日医工がオーソライズドジェネリックの承認を受けていたのですが薬価収載見送りとなっています。
以上、全4社
※日医工がAGの承認を取得していたが薬価収載見送りに
以上、全4社
※日医工がAGの承認を取得していたが薬価収載見送りに
| 規格 | 後発:ソリフェナシンコハク酸塩錠/OD錠 収載時薬価(円/錠) | 先発:ベシケア錠/OD錠 R3年度薬価(円/錠) |
|---|---|---|
| 2.5mg | 38.20 | 98.70 |
| 5mg | 64.70 | 167.00 |
薬価収載された製品数が10を超さなかったため、薬価は先発品の0.5掛け(50%)で計算されます。
ですが、ソリフェナシンの薬価は先発品であるベシケアの38.7%になっています。
これはベシケアが新薬創出等加算(新薬創出・適応外薬解消等促進加算)の対象であるためです。
先発品であるベシケアの薬価から新薬創出等加算の累積加算分を引いてから0.5掛けされたため、後発医薬品の薬価はさらに安くなっています。
OD錠の品質は?
ベシケアOD錠は添付文書に以下の記載があります。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.2 本剤をかみ砕かないで服用するよう患者に指導すること。本剤をかみ砕いた際にマスキング粒が壊れ、有効成分由来の刺激性を感じる可能性がある。引用元:ベシケアOD錠 添付文書
このことから、ベシケアOD錠を作る際には成分由来の苦味が出ないような工夫がされていることがわかります。
ジェネリックでこの問題をクリアできるか気になっていたんですが、各社の添付文書に同等の記載があるため、同じようにマスキング粒を用いて苦味を軽減しているようです。
気になる共同販売は?
ソリフェナシンコハク酸塩錠/OD錠についても共同販売がないか推察してみました。
生物学的同等性試験のデータを比較してグループ分けしてみても共同販売はなさそうな印象です。
タダラフィル錠AD(アドシルカのジェネリック)
タダラフィル錠AD。アドシルカのジェネリックです。
タダラフィルには3種類の先発医薬品が存在しており、末尾に先発医薬品名の頭文字をつけることでどの先発医薬品の後発医薬品に該当するかを区別しています。
- タダラフィル錠CI:シアリス錠(勃起不全(満足な性行為を行うに十分な勃起とその維持が出来ない患者))のジェネリック
- タダラフィル錠ZA:ザルティア錠(前立腺肥大症に伴う排尿障害)のジェネリック
- タダラフィル錠AD:アドシルカ錠(肺動脈性肺高血圧症)のジェネリック
以上、全4社
| 後発:タダラフィル錠AD20mg 収載時薬価(円/錠) | 先発:アドシルカ錠20mg R3年度薬価(円/錠) |
|---|---|
| 696.00 | 1802.80 |
薬価収載された製品数が10を超えないため、薬価は先発品の0.5掛け(50%)で計算されます。
ですが、タダラフィルADの薬価は先発品であるアドシルカの38.6%になっています。
これはアドシルカが新薬創出等加算(新薬創出・適応外薬解消等促進加算)の対象であるためです。
先発品であるアドシルカの薬価から新薬創出等加算の累積加算分を引いてから0.5掛けされたため、後発医薬品の薬価はさらに安くなっています。
デュロキセチンカプセル/錠/OD錠(サインバルタのジェネリック)
デュロキセチンカプセル/錠/OD錠。サインバルタカプセルのジェネリックで、新剤形として普通錠とOD錠も登場します。
デュロキセチンカプセルは14社、デュロキセチン錠は2社、デュロキセチンOD錠は2社の製品が薬価収載されています。
以上、全14社
※日医工G、ケミファ、杏林が薬価収載見送りに
以上、全2社
以上、全2社
| 規格 | 後発:デュロキセチンカプセル/錠/配合OD錠 収載時薬価(円/カプセル・錠) | 先発:サインバルタカプセル R3年度薬価(円/カプセル) |
|---|---|---|
| 20mg | 46.70 | 140.60 |
| 30mg | 63.10 | 190.10 |
薬価収載された製品数が10を超えたため、薬価は先発品の0.4掛け(40%)で計算されます。
ですが、デュロキセチンの薬価は先発であるサインバルタの33.2%になっています。
これはサインバルタが新薬創出等加算(新薬創出・適応外薬解消等促進加算)の対象であるためです。
先発品であるサインバルタの薬価から新薬創出等加算の累積加算分を引いてから0.4掛けされたため、後発医薬品の薬価はさらに安くなっています。
先発医薬品との適応違い
デュロキセチンが承認された2月の時点では、「慢性腰痛症に伴う疼痛」と「変形性関節症に伴う疼痛」は先発のサインバルタのみの適応でした。
ですが、薬価収載が近づくに連れて各社が適応を取得していきました。
| 適応 | サインバルタ(先発) | デュロキセチン(後発) |
|---|---|---|
| うつ病・うつ状態 | ○ | ○ |
| 糖尿病性神経障害に伴う疼痛 | ○ | ○ |
| 線維筋痛症に伴う疼痛 | ○ | ○ |
| 慢性腰痛症に伴う疼痛 | ○ | △ |
| 変形性関節症に伴う疼痛 | ○ | △ |
△:2021年6月30日時点で適応未取得のメーカー:アメル(共和薬品工業)、タカタ(高田製薬)、フェルゼン(ダイト)、トーワ(東和薬品) アメル・タカタ:2021年6月23日に適応追加、トーワ:2021年6月30日に適応追加
承認時点ではジェネリックには「慢性腰痛症」と「変形性関節症」の適応がありませんでしたが、現在、適応追加の承認が進み、一部メーカーを除いて先発品と適応が揃っています。
気になる共同販売は?
まず、カプセルの大きさは全て先発医薬品と同じです。
(20mg:4号、30mg:3号)
次に生物学的同等性試験を比較してみると・・・。
- グループ1:DSEP、オーハラ
- グループ2:JG、三笠
- グループ3:KMP、サワイ
- グループ4:YD、フェルゼン、日新、明治
- グループ5:アメル、高田
と分けられるので、このグループで共同販売してるのではないかと推察できます。(※トーワとニプロは独自)
錠剤とOD錠は大きさも気になるが・・・
錠剤とOD錠は後発医薬品独自の剤形になりますが、大きさが気になるところです。
まずは錠剤。
| 医薬品名 | デュロキセチン錠20mg「ケミファ」 デュロキセチン錠30mg「ケミファ」 | デュロキセチン錠20mg「トーワ」 デュロキセチン錠30mg「トーワ」 |
|---|---|---|
| 直径(mm) | 8.5 10.0 | 8.5 10.0 |
| 厚さ(mm) | 5.4 5.9 | 5.4 5.9 |
全く同じですね・・・。
ひょっとして・・・と生物学的同等性試験をみてみると、やっぱり。
おそらくデュロキセチン錠「ケミファ」と「トーワ」は共同販売と推察されます。
次にOD錠。
| 医薬品名 | デュロキセチンOD錠20mg「ニプロ」 デュロキセチンOD錠30mg「ニプロ」 | デュロキセチンOD錠20mg「明治」 デュロキセチンOD錠30mg「明治」 |
|---|---|---|
| 直径(mm) | 9.7 11.1 | 9.6 11.1 |
| 厚さ(mm) | 5.2 5.8 | 5.2 5.8 |
ほぼ同じ・・・。
生物学的同等性試験を比べてみると、全く同じデータ。
デュロキセチンOD錠「ニプロ」と「明治」は共同販売と推察されます。
錠/OD錠は粉砕可能?
デュロキセチン錠/OD錠は添付文書に以下の記載があります。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.3 腸溶性コーティングを施しているため、錠剤を砕いたり、すりつぶしたりしないで服用するよう指導すること。原薬が酸に不安定であり、胃酸で失活することがある。引用元:デュロキセチンOD錠「ニプロ」 添付文書
ということで錠剤やOD錠を粉砕するのは難しそうですね。
OD錠を軽く潰すのは大丈夫そうかな?
発売状況は?
デュロキセチンに関しては多くのメーカーが8月以降の発売開始と発表しています。
その理由はおそらく安定供給のため。
そんな中、薬価収載同時発売を行う会社が2社。
「アメル」(共和薬品工業)と「YD」(陽進堂)です。
絶対、発注が集中するだろうに・・・。と思っていたら案の定、発売を待たずして出荷調整になったようですね。
エピナスチン塩酸塩点眼液0.05%(アレジオン点眼液のジェネリック)
エピナスチン塩酸塩点眼液0.05%。アレジオン点眼液0.05%のジェネリックです。
今の時点ではアレジオンLX点眼液0.1%のジェネリックはまだ承認されていないので注意です。
エピナスチン塩酸塩点眼液0.05%は12社の製品が薬価収載されています。
以上、全12社
※「SEC」(参天アイケア)はAGとして承認されていたが薬価収載されず
| 後発:エピナスチン塩酸塩点眼液0.05% 収載時薬価(円/mL) | 先発:アレジオン点眼液0.05% R3年度薬価(円/mL) |
|---|---|
| 159.80 | 339.20 |
エピナスチン塩酸塩点眼液0.05%の薬価は先発品であるアレジオン点眼液0.05%の薬価の47.1%になっています。
気になる添加物は?
点眼薬で気になるのは添加物の違いです。
特に先発のアレジオン点眼液0.05%は防腐剤としてのベンザルコニウム塩化物を使用していない(発売当初は使用していたが途中で製剤変更を行なった)ため、コンタクトレンズの使用制限がありません。
後発医薬品も同じようにコンタクトレンズの使用制限がないのかどうか気になるところではありますが、結論から言うと、今回薬価収載されたものは全てコンタクトレンズ着用の制限はありません。
添加物についてもほぼ同じなのですが、一部細かい違いがあります。
アレジオン点眼液0.05%の添加物:リン酸二水素ナトリウム水和物1、リン酸水素ナトリウム水和物、ホウ酸、塩化ナトリウム、エデト酸ナトリウム水和物、pH調節剤
- 全く同じ:SN、杏林、GO、センジュ、TS、トーワ、ニットー、ニプロ、わかもと
- 1がリン酸二水素ナトリウムに変更:サワイ、日新
- 等張化剤が追加:日点
容器の違い
点眼薬は容器の違いも重要になってきます。
単純に考えれば点眼メーカーのものが使いやすいor使い慣れているのでいいんだと思いますが、これについてはサンプル等で比較するしかなさそうですね。
アレジオンLXのジェネリックは薬価収載どころか承認もされていないのに・・・
今回、薬価収載されたのは「エピナスチン塩酸塩点眼液0.05%」でアレジオン点眼液0.05%のジェネリックです。
アレジオンLX0.1%のジェネリック(「エピナスチン塩酸塩点眼液0.1%」)は薬価収載どころか承認されてもいません。
ですが、厚生労働省のホームページを見ると・・・。
アレジオンLX点眼液0.1%:R3.7.1から 「2」に変更
2:後発医薬品がある先発医薬品(先発医薬品と後発医薬品で剤形や規格が同一でない場合等を含む。ただし、全ての後発医薬品が経過措置として使用期限を定められている場合を除きます。後発医薬品と同額又は薬価が低いものについては、「☆」印を付しています。)
引用元:5.その他(各先発医薬品の後発医薬品の有無に関する情報)|薬価基準収載品目リスト及び後発医薬品に関する情報について(令和3年7月1日適用)
と記載されています。
つまり、アレジオンLX点眼液0.1%にはジェネリック医薬品が存在しないのに、後発医薬品調剤体制加算の計算上は後発医薬品の存在する先発医薬品として扱われる(計算の分母に含まれる)ということになります・・・。
ブリモニジン酒石酸塩点眼液0.1%(アイファガン点眼液のジェネリック)
ブリモニジン酒石酸塩点眼液0.1%。アイファガン点眼液0.1%のジェネリックです。
ブリモニジン酒石酸塩点眼液0.1%は5社の製品が薬価収載されています。
以上、全5社
| 後発:ブリモニジン酒石酸塩点眼液0.1% 収載時薬価(円/mL) | 先発:アイファガン点眼液0.1% R3年度薬価(円/mL) |
|---|---|
| 185.20 | 453.20 |
ブリモニジン酒石酸塩点眼液0.1%の薬価は先発品であるアイファガン点眼液0.1%の薬価の40.1%になっています。
気になる添加物は?
点眼薬で気になるのは添加物の違いです。
特に先発のアイファガン点眼液0.1%は防腐剤としてのベンザルコニウム塩化物を使用していないため、コンタクトレンズの使用制限がありません。
アイファガン点眼液0.1%の添加物:塩化カルシウム水和物、塩化マグネシウム、ホウ酸、ホウ砂、カルメロースナトリウム、亜塩素酸ナトリウム、等張化剤、pH調節剤
後発医薬品も同じようにコンタクトレンズの使用制限がないのかどうか気になるところではありますが、結論から言うと、今回薬価収載されたものは全てコンタクトレンズ着用の制限はありません。
添加物については先発であるアイファガン点眼液0.1%と比較して以下の違いがあります。
- ヒプロメロース、20%塩酸ポリヘキサニド液、塩化ナトリウム、塩化カリウム(カルメロースナトリウム、亜塩素酸ナトリウム、等張化剤ー):NIT
- 塩化ナトリウム、塩化カリウム(等張化剤ー):SEC、わかもと、日点
- 塩化ナトリウム、塩化カリウム、塩酸、水酸化ナトリウム(等張化剤、pH調節剤ー):サワイ、日新
容器の違い
点眼薬は容器の違いも重要になってきます。
単純に考えれば点眼メーカーのものが使いやすいor使い慣れているのでいいんだと思いますが、これについてはサンプル等で比較するしかなさそうですね。
パロノセトロン静注/点滴静注(アロキシ静注/点滴静注のジェネリック)
パロノセトロン静注/点滴静注。アロキシ静注/点滴静注のジェネリックです。
パロノセトロン静注/点滴静注は1社 AGのみ薬価収載されています。
- パロノセトロン静注0.75mg/5mL「タイホウ」(岡山大鵬薬品)
- パロノセトロン点滴静注バッグ0.75mg/50mL「タイホウ」(岡山大鵬薬品)
| 剤形 | 後発:パロノセトロン「タイホウ」 収載時薬価(円/瓶) | 先発:アロキシ R3年度薬価(円/瓶) |
|---|---|---|
| 静注0.75mg/5mL | 5,349 | 14,764 |
| 点滴静注バッグ0.75mg/50mL | 5,472 | 14,976 |
本来、パロノセトロンの薬価は先発医薬品の0.5掛け(50%)で計算されます。
ですが、パロノセトロン点滴静注0.75mg/5mL「タイホウ」の薬価は先発品であるアロキシ静注0.75mg 5mLの薬価の36.2%、パロノセトロン点滴静注バッグ0.75mg/50mL「タイホウ」の薬価は先発品であるアロキシ点滴静注バッグ0.75mg 50mLの36.5%になっています。
これはアロキシが新薬創出等加算(新薬創出・適応外薬解消等促進加算)の対象であるためです。
先発品であるアロキシの薬価から新薬創出等加算の累積加算分を引いてから0.5掛けされたため、後発医薬品の薬価はさらに安くなっています。
ペメトレキセド点滴静注(アリムタのジェネリック)
ペメトレキセド点滴静注。アリムタ注射用のジェネリックです。
ペメトレキセド点滴静注液は3社、ペメトレキセド点滴静注用は5社の製品が薬価収載されています。
先発のアリムタは「注射用」(凍結乾燥製剤)のみでしたが、後発のペメトレキセドは凍結乾燥製剤の「点滴静注用」に加えて新剤形の「点滴静注液」(液剤)が追加されています。また、アリムタは100mgと500mgの2規格でしたが、ペメトレキセドには800mgの新規格が追加されています。
以上、全3社
※800mgの収載なし
以上、全5社
※800mgの収載なし
| 医薬品名 | 後発医薬品:ペメトレキセド点滴静注液/静注用 収載時薬価(円/瓶) | 先発医薬品:アリムタ注射用 R3年度薬価(円/瓶) |
|---|---|---|
| 100mg | 16,747 | 45,048 |
| 500mg | 70,061 | 188,457 |
| 800mg | 106,410 | – |
本来、ペメトレキセド点滴静注の薬価は先発医薬品の0.5掛け(50%)で計算されます。
ですが、ペメトレキセド点滴静注/静注用の薬価は先発品であるアリムタ注射用の薬価の37.2%になっています。
これはアリムタが新薬創出等加算(新薬創出・適応外薬解消等促進加算)の対象であるためです。
先発品であるアリムタの薬価から新薬創出等加算の累積加算分を引いてから0.5掛けされたため、後発医薬品の薬価はさらに安くなっています。
新規格が登場した後発医薬品
フェンタニルクエン酸塩1日用テープ0.5mg(フェントステープ0.5mgのジェネリック)
フェンタニルクエン酸塩1日用テープ。フェントステープのジェネリックです。
1mg/2mg/4mg/6mg/8mgはすでに後発医薬品が販売されていますが、0.5mgの後発医薬品は存在していませんでした。
今回1社のみ薬価収載されています。
- フェンタニルクエン酸塩1日用テープ0.5mg「テイコク」
| 後発:フェンタニルクエン酸塩1日用テープ0.5mg「テイコク」 収載時薬価(円/枚) | 先発:フェントステープ0.5mg R3年度薬価(円/枚) |
|---|---|
| 133.10 | 278.80 |
薬価収載が見送られた後発医薬品
今回残念ながら薬価収載が見送られたものについてまとめておきます。
新登場のはずが薬価収載が見送られたもの
薬価収載となっていれば初のジェネリック登場だったはずのものです。
- シルデナフィル錠20mgRE「JG」(日本ジェネリック):レバチオ錠 初のジェネリックの予定でした
- ブンチモ配合懸濁性点眼液「サンド」:アゾルガ配合懸濁性点眼液 初のジェネリック(AG)の予定でした
- リドプロクリーム「サトウ」:エクラクリーム 初のジェネリック(AG)の予定でした
- エリブリンメシル酸塩静注液1mg「日医工」:ハラヴェン静注 初のジェネリック(AG)の予定でした
そのほか薬価収載が見送られたもの
薬価収載が見送られたもののうち、特に気になったものです。
- アマルエット配合錠のAG:「ファイザー」
- エスゾピクロン錠:「日医工」
- エピナスチン塩酸塩点眼液0.05%のAG:「SEC」(参天アイケア)
- ソリフェナシンコハク酸塩錠/OD錠のAG:「日医工」
- デュロキセチンカプセル:「日医工G」(日医工岐阜工場)、「ケミファ」(富士化学工業)、「杏林」(キョーリンリメディオ、販売元:杏林製薬)
- パロノセトロン静注0.75mg/2mL「日医工」
- パロノセトロン点滴静注バッグ0.75mg/100mL「サワイ」
色んな戦略があるんでしょうが、薬価収載しないのならなんで承認取得したんでしょう?
日医工については仕方がないですけどね。
2021年2月製造販売承認取得品目の薬価基準収載見送りのお知らせ
そのほか気になる薬価収載
後発医薬品以外で気になった薬価収載品をまとめておきます。
テネリアOD錠20mg/40mg
テネリアのOD錠が薬価収載されています。
ゆず風味と聞いた気がしますが、OD錠を追加するなら普通錠をなくして欲しいなあ。
ドボベットフォーム
ドボベットにフォームが追加になっています。
いわゆる泡状スプレーですね。
所感
今回の薬価収載、日医工と小林化工の製品が一つもありません。
小林化工については2月の製造承認の時点でいろんな問題が表に出ており、承認自体を見送っていました。
日医工はその後、流通・承認に関わる様々な問題がおき、その問題は現在も継続しています。
2021年2月製造販売承認取得品目の薬価基準収載見送りのお知らせ
昨年から続く、後発医薬品の供給問題。
後発医薬品の新規採用に対する考え方にも大きな影響を与えたのではないでしょうか?
これまで値引き率で採用メーカーを決めていた薬局もAGや大手後発メーカーである沢井製薬や東和薬品の製品を優先して採用するようになったという話も耳にしました。
また、後発医薬品調剤体制加算のことは気になるけど、新発売してすぐに切り替えるのではなく、しばらく様子をみたいという薬局の話も聞こえてきます。
これまで製造委託や共同販売、原薬の情報を後悔していないメーカーがほとんどですが、今回の問題をきっかけに積極的に公開するメーカーも増えています。
ジェネリック医薬品の選択については、これまではユースフルジェネリックのような服薬上の利便性を追求した製品、先発医薬品と完全に同等と言われるAG1、先発医薬品メーカーが販売している製品などが採用を決める上での判断材料でしたが、今回の問題により、「安定供給」という大きな判断材料が加わったのではないかと思います。
当たり前のように見えて実際には困難な「安定供給」
ジェネリック医薬品の薬価問題、参入メーカーの多さなど、問題は山積みですが、これからは品質はもちろん、安定供給が期待できるメーカーを採用していこうと考える薬局が増えていくと思います。
それをどうやって見極めていくのか?
単純に生産力のある規模の大きな会社を選べばいいのか?
薬局にも薬剤師にもそういった視点が求められていく時代になるのではないかと考えます。
ちなみに、うちの薬局はしばらくは採用見送りです。
もう少し様子を見てから採用を決めたいと思います。
参考
官報 令和3年6月17日号(号外第137号)薬価基準収載品目リスト及び後発医薬品に関する情報について
(令和3年6月18日適用)
5.その他(各先発医薬品の後発医薬品の有無に関する情報) PDF
処方箋に記載する一般名処方の標準的な記載(一般名処方マスタ)について(令和3年6月18日適用)
一般名処方マスタ PDF