2021年9月21日、厚生労働省は「後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて」を公開しました。
今回の対応は、診療報酬上の特例に当たります。
後発医薬品の出荷停止や出荷調整が相次いでいることを踏まえ、後発医薬品調剤体制加算等で用いる後発医薬品の使用割合の計算から出荷停止品目を除外することを認めるというものです。
2020年度診療報酬改定での後発医薬品調剤体制加算と調剤基本料の注7(後発医薬品に係る減算)についてまとめた記事は↓です。
小林化工や日医工の行政処分(業務停止)をきっかけに、日本全体で後発医薬品の入荷が難しくなっています。
後発医薬品を入手できないことを原因に、後発医薬品の使用率が減り、後発医薬品調剤体制加算が算定できなくなってしまうことで経営的に圧迫されていまうことに配慮した対応となります。
後発医薬品調剤体制加算の変更について
まずは今回の特例で後発医薬品調剤体制加算がどのように変化するのか簡単にまとめます。
今回の特例は「厚生労働省が供給停止品目として認めている医薬品については、後発医薬品調剤体制加算と調剤基本料の注7(後発医薬品に係る減算)の計算式から除外して考えることができる」というものです。
出荷調整等でやむを得ず後発医薬品から先発医薬品に戻すケースが多くなると、後発医薬品調剤体制加算を算定するための後発医薬品の数量シェアが維持できず算定できなくなってしまう可能性がありますが、今回の特例を利用することでそれを回避できるというわけです。
後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて
新指標の割合(後発医薬品の数量シェア)を算出する際に供給停止品目を除外することが可能
- 対象:後発医薬品調剤体制加算、調剤基本料の注7(後発医薬品に係る減算)、後発医薬品使用体制加算、外来後発医薬品使用体制加算
- 対象期間:令和3年6月〜令和4年3月 診療分
- 適用方法:
特例を適用するかどうかは月毎に判断可能(3ヶ月の集計で適用、非適用が混在してもよい)
特例を適用する月は供給停止品目を全て除外する(供給停止品目のうち一部だけを除外することはできない)
後発医薬品の供給状況が知りたい場合はDSJP(drugshortage.jp)をご利用ください。

DSJPはボランティアで運営する医療用医薬品の供給状況データベースです。
ぺんぎん薬剤師も運営として参加させてもらっています。
復習:後発医薬品調剤体制加算(R2年度改定)
後発医薬品調剤体制加算(2020年度改定)は調剤基本料の加算です。
以下の通り3段階の点数が設定されています。
第1節 調剤技術料
区分00 調剤基本料(処方箋の受付1回につき)
- 注6 保険薬局及び保険薬剤師療養担当規則(昭和32年厚生省令第16号)第7条の2に規定する後発医薬品(以下「後発医薬品」という。)の調剤に関して別に厚生労働大臣が定める施設基準に適合しているものとして地方厚生局長等に届け出た保険薬局において調剤した場合には、当該基準に係る区分に従い、次に掲げる点数を所定点数に加算する。
- イ 後発医薬品調剤体制加算1 15点
- ロ 後発医薬品調剤体制加算2 22点
- ハ 後発医薬品調剤体制加算3 28点
【省令、告示】 (2) 1 診療報酬の算定方法の一部を改正する件(告示)(令和2年 厚生労働省告示第57号)別表第3(調剤点数表)P1〜2
第十五 調剤
五 後発医薬品調剤体制加算の施設基準
- (1)通則
当該保険薬局において調剤した薬剤の規格単位数量に占める後発医薬品のある先発医薬品及び後発医薬品を合算した規格単位数量の割合が五割以上であること。- (2)後発医薬品調剤体制加算1の施設基準
当該保険薬局において調剤した後発医薬品のある先発医薬品及び後発医薬品を合算した規格単位数量に占める後発医薬品の規格単位数量の割合が七割五分以上であること。- (3)後発医薬品調剤体制加算2の施設基準
当該保険薬局において調剤した後発医薬品のある先発医薬品及び後発医薬品を合算した規格単位数量に占める後発医薬品の規格単位数量の割合が八割以上であること。- (4)後発医薬品調剤体制加算3の施設基準
当該保険薬局において調剤した後発医薬品のある先発医薬品及び後発医薬品を合算した規格単位数量に占める後発医薬品の規格単位数量の割合が八割五分以上であること。【省令、告示】 (4) 1 特掲診療料の施設基準等の一部を改正する件(告示)(令和2年厚生労働省告示第59号)P131〜132
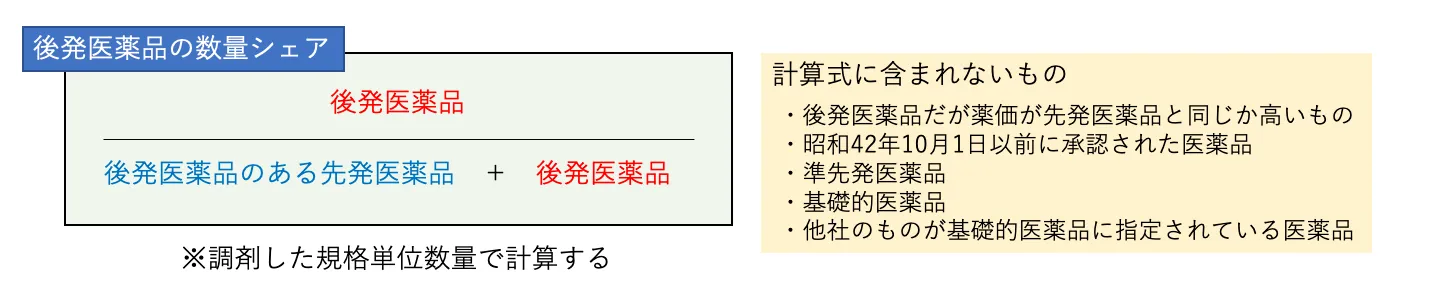
後発医薬品調剤体制加算の施設基準のうち、最も重要となるのが「調剤した後発医薬品のある先発医薬品及び後発医薬品について、当該薬剤を合算した規格単位数量に占める後発医薬品の規格単位数量の割合」、いわゆる、後発医薬品の数量シェア(後発品置換え率)です。
計算式にすると以下のようになります。
後発医薬品の数量シェア(置換え率)=〔後発医薬品の数量〕/(〔後発医薬品のある先発医薬品の数量〕+〔後発医薬品の数量〕)
復習:調剤基本料の注7(後発医薬品に係る減算)(R2年度改定)
逆に、後発医薬品の数量シェアが4割以下の場合は調剤基本料が2点減算されてしまいます。
第94 調剤基本料の注7に規定する厚生労働大臣が定める保険薬局
- 以下のいずれかに該当する保険薬局は調剤基本料を2点減算する。
ただし、処方箋受付回数が1月に600回以下の保険薬局は除くものとする。
- (1) 当該保険薬局において調剤した後発医薬品のある先発医薬品及び後発医薬品について、当該薬剤を合算した規格単位数量に占める後発医薬品の規格単位数量の割合が40%以下であること。ただし、当該保険薬局における処方箋受付状況を踏まえ、やむを得ないものは除く。
- (2) 当該保険薬局において調剤した後発医薬品のある先発医薬品及び後発医薬品について、当該薬剤を合算した規格単位数量に占める後発医薬品の規格単位数量の割合について、毎年7月1日現在で届出書の記載事項について行う報告等を通じ、直近1年間に地方厚生(支)局長への報告していないこと。
- 「当該保険薬局における処方箋受付状況を踏まえ、やむを得ないもの」とは、直近1月間の当該保険薬局における処方箋受付回数のうち、先発医薬品の変更不可の記載がある処方箋の受付回数が50%以上の場合のことをいう。この場合の処方箋受付回数は、調剤基本料の施設基準に定める処方箋受付回数に準じて取り扱う。
- 1の(1)の後発医薬品の後発医薬品の調剤数量割合に基づく当該減算への該当性については、直近3月間の当該保険薬局において調剤した後発医薬品のある先発医薬品及び後発医薬品について、当該薬剤を合算した規格単位数量に占める後発医薬品の規格単位数量の割合をもって翌月に判断し、該当する場合は、翌々月から調剤基本料を減算する。
- 1の(2)の直近1年間に地方厚生(支)局長に報告を行っていない保険薬局に該当した場合は、当該報告を行った場合には、報告を行った月の翌月より、当該保険薬局に該当しないものとして取り扱う。
- 調剤基本料の注7に係る規定は、令和2年9月30日までの間に限り、なお従前の例による。
【省令、告示】 (4) 2 特掲診療料の施設基準等及びその届出に関する手続きの取扱いについて(通知)(令和2年3月5日保医発0305第3号)P260
特例の効果:後発医薬品が入手できない場合も加算を維持(減算を回避)できる
今回の特例では、一覧(別添2)に示された供給停止品目と同一成分・同一投与形態の医薬品について計算式から除外することが可能となります。
同一成分・同一投与形態の医薬品ということなので、剤形違いを含む先発医薬品・後発医薬品全てが計算式から除外されます。
つまり、一覧に示された供給停止品目は後発医薬品のない先発医薬品の扱いになるため、数量シェアの計算に影響を与えない(与えにく)ということになります。
また、この特例を使用する場合は、医薬品ごとではなく、一覧に記載されているすべての品目を対象にしなければなりません。
ですが、特例を使用するかどうかは1ヶ月ごとに変更できるので、算定に有利な場合のみ使用することが可能です。
「後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて」の通知を読み解く
ここからは今回の通知について詳しく読み解いていきたいと思います。
今回の通知と添付書類へのリンクを掲載しておきます。
- 令和3年9月21日 後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて:https://www.mhlw.go.jp/content/12404000/000834839.pdf
- 別添2:https://www.mhlw.go.jp/content/12404000/000834840.xlsx
- 様式1-1:https://www.mhlw.go.jp/content/12404000/000835291.xlsx
- 様式1-2:https://www.mhlw.go.jp/content/12404000/000835292.xlsx
- 様式1-3:https://www.mhlw.go.jp/content/12404000/000835293.xlsx
1-(1)後発医薬品使用体制加算等における後発医薬品の使用割合等に係る要件の取扱いについて
1.供給停止となっている後発医薬品等の診療報酬上の臨時的な取扱いについて
(1)後発医薬品使用体制加算等における後発医薬品の使用割合等に係る要件の取扱いについて① 小林化工株式会社及び日医工株式会社に対する医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和35年法律第145号)による行政処分等を契機として令和3年7月1日時点で供給が停止されていると医政局経済課に報告があった医薬品(以下「供給停止品目」という。)のうち、別添2に示す供給停止品目と同一成分・同一投与形態の医薬品については、「後発医薬品使用体制加算」、「外来後発医薬品使用体制加算」、「後発医薬品調剤体制加算」及び「調剤基本料」注7に規定する減算(後発医薬品減算)(以下「加算等」という。)における実績要件である後発医薬品の使用(調剤)割合(以下「新指標の割合」という。)を算出する際に、算出対象から除外しても差し支えないものとする。
当該取扱いについては、令和4年3月31日を終期とする。
② ①の取扱いを行う場合においては、別添2に示す全ての品目について、新指標の割合の算出対象から除外することとし、一部の成分の品目のみ算出対象から除外することは認められない。
また、①の取扱いについては、1月ごとに適用できることとし、加算等の施設基準について、直近3月の新指標の割合の平均を用いる場合においては、当該3月に①の取扱いを行う月と行わない月が混在しても差し支えないこととする。
なお、カットオフ値の算出については、今回の臨時的な取扱いの対象とはしないこととし、新指標の割合について①の取扱いを行った場合においても、カットオフ値については従前通り算出し、加算等の施設基準の実績要件を満たすかどうか確認すること。
③ 新指標の割合を算出する際に、①の取扱いを行い、加算等の実績要件を満たすこととする場合(後発医薬品減算については減算に該当しないこととなった場合)においては、保険医療機関等は、各月の新指標の割合等を記録するとともに、別紙様式(後発医薬品使用体制加算は様式1-1、外来後発医薬品使用体制加算は様式1-2、後発医薬品調剤体制加算等は様式1-3)を用いて各地方厚生(支)局に報告を行うこと。
なお、前月と加算等の区分が変わらない場合においても、新指標の割合の算出に①の取扱いを行い、実績を満たすこととする場合は、報告の対象となる。
また、加算等の区分に変更が生じる場合又は基準を満たさなくなる場合には、従前通り変更等の届出を行う必要がある。その際、後発医薬品の使用割合等については、①の取扱いを行って算出した割合を記載しても差し支えないこととする。引用元:令和3年9月21日 後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて
赤線部分
には今回の特例の対象となる診療報酬が挙げられています。
- 後発医薬品使用体制加算(入院)
- 外来後発医薬品使用体制加算(院内処方)
- 後発医薬品調剤体制加算
- 調剤基本料 注7に規定する減算
後発医薬品の使用割合が関連するすべての項目が対象で、薬局に関連するのは「後発医薬品調剤体制加算」と「調剤基本料 注7」です。
緑線部分が特例が適応となる期間で(令和3年6月1日〜)令和4年3月31日までの数量シェアの算出に適用可能となっています。
そもそも現在の診療報酬(令和2年度診療報酬改定)の期間が令和4年3月31日までなんですから当然ですね。
次の改定では後発医薬品調剤体制加算もどうなるかわかりませんしね・・・。
ちなみに、特例は令和3年6月1日〜から適用可能ですが、それについては後で紹介します。
供給停止品目(黄色線部分)
黄色線部分
には今回の特例の対象となる供給停止品目についての説明が記載されています。
- 小林化工や日医工への薬機法による行政処分を契機として供給停止している医薬品
- 令和3年7月1日時点で供給が停止されていると医政局経済課に報告があった医薬品
と書かれていますが、要は、「別添2に示す供給停止品目と同一成分・同一投与形態の医薬品」が今回の特例の対象となる供給停止品目(全て内服薬)です。
このリストに掲載されているすべての内服薬は特例により計算式から除外することが可能になります。
ということで、別添2に示されている「供給停止品目:成分名(代表的な製品名)」を五十音順でまとめます。
ちなみに、全て内服薬になっています。
アトルバスタチンカルシウム水和物(リピトール)
アムロジピンベシル酸塩・アトルバスタチンカルシウム水和物(カデュエット、アマルエット)
イルベサルタン(アバプロ、イルベタン)
エパルレスタット(キネダック)
エピナスチン塩酸塩(アレジオン)
エンタカポン(コムタン)
エンテカビル水和物(バラクルード)
オロパタジン塩酸塩(アレロック)
カンデサルタンシレキセチル・アムロジピンベシル酸塩(ユニシア、カムシア)
クラリスロマイシン(クラリス、クラリシッド)
グリメピリド(アマリール)
クロピドグレル硫酸塩(プラビックス)
ゾルピデム酒石酸塩(マイスリー)
トラニラスト(リザベン)
トリアゾラム(ハルシオン)
ナテグリニド(スターシス、ファスティック)
ニカルジピン(ペルジピン)
バルサルタン・アムロジピンべシル酸塩(エックスフォージ、アムバロ)
ピルシカイニド塩酸塩(サンリズム)
フェキソフェナジン塩酸塩(アレグラ)
プランルカスト水和物(オノン)
メサラジン(ペンタサ、アサコール)
ラロキシフェン塩酸塩(エビスタ)
リシノプリル(ゼストリル、ロンゲス)
リスペリドン塩酸塩(リスパダール)
リルマザホン塩酸塩(リスミー)
ロサルタンカリウム・ヒドロクロロチアジド(プレミネント、ロサルヒド)
https://pharmacist.m3.com/column/penguin_news/2685
閲覧には無料登録が必要なのでこの機会に是非!↓のバナーから登録できます。
特例を用いた新指標の割合の算出方法(青線部分)
青線部分
には今回の特例を用いて新指標の割合(数量シェア)を算出する場合の注意点がまとめてあります。
- 特例を用いる場合はすべての供給停止品目を計算から除外する(一部のみ除外することはできない)
- 特例は1ヶ月ごとに適用するかどうかを選択可能(特例を適用する月と適用しない月が混在してもOK)
- カットオフ値に特例は適用しない
復習:カットオフ値
カットオフ値とは「調剤した薬剤の規格単位数量に占める後発医薬品のある先発医薬品及び後発医薬品を合算した規格単位数量の割合」です。
計算式にすると以下のようになります。
後発医薬品のカットオフ値=(〔後発医薬品のある先発医薬品の数量〕+〔後発医薬品の数量〕)/〔全医薬品の数量〕
この値が50%以上であることが後発医薬品調剤体制加算の施設基準になっています。
第93 後発医薬品調剤体制加算
1 後発医薬品調剤体制加算1に関する施設基準
- (2) 当該保険薬局において調剤した薬剤(4に掲げる医薬品を除く。)の規格単位数量に占める後発医薬品のある先発医薬品及び後発医薬品を合算した規格単位数量の割合が50%以上であること。
【省令、告示】 (4) 2 特掲診療料の施設基準等及びその届出に関する手続きの取扱いについて(通知)(令和2年3月5日保医発0305第3号)P259
特例を用いた場合の報告について(ピンク部分)
ピンク部分
には特例を利用した場合の報告についての規定が記載されています。
特例を用いることで、
- 後発医薬品調剤体制加算の算定要件を満たす
- 調剤基本料の注7(後発医薬品に係る減算)から除外される
場合は様式1-3に記載した上で報告を行う必要があります。
特例を用いた場合は、それに加えて、様式1-3も提出します。
1-(2) 特例を用いた場合の報告時期について
(2) (1)③の報告時期について
(1) ①の取扱いによって実績を満たすこととなる保険医療機関等に係る同③の報告を行う時期は次のとおりとする。なお、各期限までに報告が間に合わない場合には、事前に各地方厚生(支)局に相談すること。
① 令和3年9月〜10月の実績について、(1)①の取扱いを実施した保険医療機関等:令和3年11月30日(火)までに、令和3年9月〜10月分の実績等について報告
② 令和3年11月〜令和4年1月の実績について、(1)①の取扱いを実施した保険医療機関等:令和4年2月28 日(月)までに、令和3年9月〜令和4年1月分の実績等について報告((2)①の報告を実施した場合も報告すること)引用元:令和3年9月21日 後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて
(1)とか①で表現されているのでわかりにくい文章ですね。
これは特例を用いた場合(新指標(後発医薬品の数量シェア)の割合を算出した結果、後発医薬品調剤体制加算の施設基準を満たす、調剤基本料の注7から除外される)の報告書の提出期限を示している文章です。
- ① 令和3年9〜10月の数量シェアの算出に特例を適用した場合:令和3年11月30日までに令和3年9〜10月の実績を報告
- ② 令和3年11月〜令和4年1月の数量シェアの算出に特例を適用した場合:令和4年2月28日までに令和3年9月〜令和4年1月分の実績を報告
(①で令和3年9〜10月の実績の報告を行った場合でも再度報告)
となっています。
①の報告をした場合でも②の報告に該当すれば、令和3年9〜10月分についても再度報告する形になります。
報告には様式1-3を用いますが、記入欄は数量シェアの算出に特例利用可能な令和3年6月分から設けられています。
別添1 Q&A 特例はいつから適用可能となるか?
【調剤】
問3 後発医薬品調剤体制加算等について、1(1)①の取扱いにより令和3年6月から8 月の診療分の新指標の割合について、令和3年10月1日までに必要な届出を実施した場合、令和3年10月診療分から算定可能となるか。
(答)そのとおり。ただし、1(1)①の取扱いにより算出した新指標の割合を用いた場合に当該加算等の区分が変更とならない場合は、変更等の届出は不要である。
なお、令和3年6月診療分以降の新指標の割合について、1(1)①の取扱いを行い、算出した割合を使用することができる。引用元:令和3年9月21日 後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて 別添1
令和3年6月診療分以降の新指標の割合(数量シェア)について特例が適用可能です。
よって、令和3年6〜8月の数量シェアによって施設基準が判断される令和3年10月1日から、特例を用いての算定が可能ということになります。
おまけ:医科についてのQ&A
【医科】
問1 1(1)①の取扱いの対象となる医薬品について、一般名処方を行った場合、一般名処方加算1及び2は算定できるか。
(答)算定可。なお、今回の臨時的な取扱いについては、加算等の施設基準における新指標の割合の算出等に係るものであり、一般名処方加算における後発医薬品のある医薬品の取扱いを変更するものではない。問2 後発医薬品使用体制加算について、1(1)①の取扱いにより令和3年8月診療分の新指標の割合を算出し、当該加算の区分を判定し、令和3年10月1日までに必要な届出を実施した場合、令和3年10月診療分から算定可能となるか。
(答)そのとおり。ただし、1(1)①の取扱いにより算出した新指標の割合を用いた場合に当該加算の区分が変更とならない場合は、変更等の届出は不要である。
なお、外来後発医薬品使用体制加算についても同様であるが、直近3月分の新指標の割合の平均により区分を判断することとなるため、令和3年6月診療分以降の新指標の割合について、1(1)①の取扱いを行い、算出した割合を使用することができる。引用元:令和3年9月21日 後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて 別添1
問1 今回の供給停止品目は一般名処方加算の対象に関与するものではありません。
問2 後発医薬品使用体制加算(入院)でも考え方は同じです。
補足:後発医薬品の安定供給に関する報告とは?
1.供給停止となっている後発医薬品等の診療報酬上の臨時的な取扱いについて
(1)後発医薬品使用体制加算等における後発医薬品の使用割合等に係る要件の取扱いについて
①小林化工株式会社及び日医工株式会社に対する医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和35年法律第145号)による行政処分等を契機として令和3年7月1日時点で供給が停止されていると医政局経済課に報告があった医薬品(以下「供給停止品目」という。)のうち、別添2に示す供給停止品目と同一成分・同一投与形態の医薬品については、「後発医薬品使用体制加算」、「外来後発医薬品使用体制加算」、「後発医薬品調剤体制加算」及び「調剤基本料」注7に規定する減算(後発医薬品減算)(以下「加算等」という。)における実績要件である後発医薬品の使用(調剤)割合(以下「新指標の割合」という。)を算出する際に、算出対象から除外しても差し支えないものとする。引用元:令和3年9月21日 後発医薬品の出荷停止等を踏まえた診療報酬上の臨時的な取扱いについて
「供給が停止されていると医政局経済課に報告があった医薬品」という部分が気になっていたんですが、↓のような情報をいただきました。
自分はこの様式で報告したことあります。https://t.co/tVe90SYWSE
— 出荷調整で暴れる寸前君 (@LorinserCLS) September 22, 2021
ということで調べてみると、「後発医薬品の安定供給について」(平成18年3月10日医政局長通知)が出てきました。
後発医薬品の安定供給について
後発医薬品の安定供給については、平成18年度薬価制度改革の骨子(平成17年12月16日中央社会保険医療協議会了解)を踏まえ、今後以下のとおりとしますので、周知方よろしくお願いします。
また、後発医薬品の安定供給に当たって、医薬品製造販売業者として必要な情報の収集及び提供について遺漏なく対応するようお願いします。引用元:「後発医薬品の安定供給について」(平成18年3月10日医政局長通知)
安定供給の要件
1.安定供給の要件
後発医薬品の使用促進を図るためには、その安定供給に関し、保険医療機関、保険薬局及び患者の信頼を確保・向上させていくことが肝要である。
薬価基準収載医薬品は、全国レベルで保険医療機関又は保険薬局の注文に応じて継続的に供給することが必要であることから、後発医薬品(薬価基準収載後、3ヶ月を経過していないもの、及び「医療用医薬品の供給停止について」(平成10年10月7日経第56号厚生省健康政策局経済課長通知)に規定する手続きを経て「薬価基準削除願」が提出されたものを除く。以下同じ。)についてその安定供給の要件を以下のとおり規定するので、後発医薬品の製造販売業者は、その遵守に努めること。
1 正当な理由がある場合を除き、少なくとも5年間は継続して製造販売し、保険医療機関及び保険薬局からの注文に迅速に対応できるよう、常に必要な在庫を確保すること。また、医薬品原料の安定的かつ継続的な確保に留意すること。
2 注文を受け付けてから、適切な時間内で保険医療機関及び保険薬局に届けられるよう全都道府県における販売体制を整備すること。また、容易に注文受付先がわかるよう保険医療機関及び保険薬局に必要な情報を提供すること。
3 保険医療機関及び保険薬局からの安定供給に関する苦情を迅速かつ適切に処理しその改善を行う体制を整備し、その実施に努めること。引用元:「後発医薬品の安定供給について」(平成18年3月10日医政局長通知)
ピンクマーカー
をつけた通り、後発医薬品の安定供給について定義されています。
安定供給に関する苦情
2.保険医療機関及び保険薬局からの苦情への対応
今般、(社)日本医師会、(社)日本歯科医師会、(社)日本薬剤師会から後発医薬品の安定供給に関する苦情を当局経済課が受け付け、当該製造販売業者に対し必要な調査及び改善指導を行う仕組みを設けたこと。また、その旨関係団体の長宛に通知したこと。引用元:「後発医薬品の安定供給について」(平成18年3月10日医政局長通知)
後発医薬品の安定供給についての苦情は、医師会、歯科医師会、薬剤師会を通じて医政局経済課が受け付けると明記されています。
3.安定供給に支障を生じた事業者への対応
上記2.において、文書により改善指導を行った場合は、改善指導を行った事業者名及び改善指導の内容等について公表すること。
また、改善指導を行った次年度以降、当該事業者から薬価収載希望を受け付ける場合には、安定供給改善報告書を提出させることとし、その改善が図られない場合は、薬価収載希望書を受け付けないことがあること。引用元:「後発医薬品の安定供給について」(平成18年3月10日医政局長通知)
改善指導の内容についても記載されています。
改善指導の内容ってどこに公表されているんだろ?
後発医薬品の安定供給についての苦情の提出方法が変更(令和3年6月25日)
岡山県の医薬安全課のホームページに「後発医薬品の安定供給について」の一部改正について(令和3年6月25日医政発0625第4号)が掲載されれいます。
「後発医薬品の安定供給について」の一部改正について
今般、「後発医薬品の安定供給について」(平成18年3月10日医政発第0310004号)を一部改正し、FAXで受け付けていた苦情をメールにて受け付けることとしました。
ついては、別添のとおり、(公社)日本医師会、(公社)日本歯科医師会、(公 社)日本薬剤師会に通知しましたので、御了知のうえ、貴管下関係者に対する周知方よろしくお願いいたします。引用元:「後発医薬品の安定供給について」の一部改正について(令和3年6月25日医政発0625第4号)
下記の画像に示している様式を用いて、FAXやメールで苦情を送ることが可能になったようです。
時期的に現在起こっている医薬品の供給問題を受けての改正と思われます。