2023年11月8日、全国的にインフルエンザが流行する中、タミフルドライシロップが限定出荷になってしまいました。
中外製薬株式会社 限定出荷に関するご案内 抗インフルエンザウイルス剤 「タミフルⓇドライシロップ3%」(2023年11月)
↑の案内に記載されているように、唯一の後発品であるオセルタミビルDS「サワイ」はひと足先に、10月から出荷調整されています。
案内文に書かれているように、想定より早い時期にインフルエンザが流行し、需要が高まったことが供給不安の原因ではあると思いますが、
- 2019年以来の流行ということで準備が不十分
- COVID-19の同時感染を考慮した結果、内服薬であるオセルタミビルの処方が増加
のも供給不安を起こした原因なのではないかと思います。
さて、タミフルドライシロップの限定出荷が発表されると同時に、厚生労働省は各都道府県 衛生主管部(局)に「オセルタミビルリン酸塩ドライシロップの在庫逼迫に伴う協力依頼」という事務連絡を送付しています。
今回の記事では、本通知で依頼されている内容について、少し掘り下げてみたいと思います。
やむを得ずオセルタミビル(タミフル)カプセルを脱カプセルした際の自家製剤加算の考え方、脱カプの調製・計算方法については「薬剤師の覚え書」の方でもまとめていますので、答えだけ知りたいときは以下も参考にしてください。
Q:タミフルDSが手に入らずカプセルを脱カプセルした場合は加算を算定できますか? | 薬剤師の覚え書 (yakuzaishi.love)
Q:タミフルカプセルを脱カプセルするときの調製方法/計算方法を教えてください。 | 薬剤師の覚え書 (yakuzaishi.love)
タミフルドライシロップの限定出荷と厚労省からの依頼(2023年11月)
2023年11月8日にタミフルドライシロップは限定出荷となりました。
中外製薬株式会社 「限定出荷に関するご案内 抗インフルエンザウイルス剤 「タミフルⓇドライシロップ3%」」(2023年11月)
同日、厚生労働省医政局医薬産業振興・医療情報企画課が通知を出しています。
厚生労働省医政局医薬産業振興・医療情報企画課 「オセルタミビルリン酸塩ドライシロップの在庫逼迫に伴う協力依頼」(事務連絡 令和5年11月8日)
その翌日、沢井製薬は改めてオセルタミビルDS「サワイ」が限定出荷中であること、上記の通知についての案内を出しました。
(オセルタミビルDS「サワイ」は10月から限定出荷でした)
沢井製薬株式会社 「オセルタミビルDS3%「サワイ」の供給に関するお詫びとお願い」(2023年11月)
厚労省の通知に記載されている依頼内容は以下の通りです。
1.オセルタミビルリン酸塩ドライシロップについて、返品が生じないよう、過剰な発注は厳に控えていただき、当面の必要量に見合う量のみの購入をお願いしたいこと。
2.医療機関におかれては、オセルタミビルリン酸塩ドライシロップについて、吸入薬の利用が可能な5歳以上のインフルエンザ患者に対しては、吸入薬の処方を検討いただきたいこと。
3.医療機関及び薬局におかれては、オセルタミビルリン酸塩ドライシロップが不足している状況にあっても、当該品目を処方又は調剤する必要がある場合には、オセルタミビルリン酸塩カプセルを脱カプセルし、賦形剤を加えるなどの調剤上の工夫を行った上での調剤を検討いただきたいこと。
4.薬局におかれては、処方されたオセルタミビルリン酸塩ドライシロップについて、自らの店舗だけでは供給が困難な場合であっても、系列店舗や地域における連携により、可能な限り患者への供給ができるよう調整をしていただきたいこと。
参照:厚生労働省医政局医薬産業振興・医療情報企画課 「オセルタミビルリン酸塩ドライシロップの在庫逼迫に伴う協力依頼」(事務連絡 令和5年11月8日)
他の薬剤への切替
現在日本で承認されている抗インフルエンザ薬は以下の6成分です。
- オセルタミビル(タミフル®)
- ザナミビル(リレンザ®)
- ラニナミビル(イナビル®)
- ペラミビル(ラピアクタ®)
- バロキサビル マルボキシル(ゾフルーザ®)
- ファビピラビル※1(アビガン®)
- アマンタジン※2(シンメトレル®)
※1:ファビピラビル:RNAポリメラーゼ阻害剤。「新型又は再興型インフルエンザウイルス感染症が発生し、既存薬が無効又は効果が不十分な場合で、国が使用すると判断した場合のみ使用すること」になっているため、国が備蓄を行い、一般流通は行われていない
※2:アマンタジン:A型インフルエンザ ウイルス表面のM2蛋白の機能を阻害することでウイルスの増殖を抑制。耐性を持つウイルスが多く、ノイラミニダーゼ阻害薬が普及したことにより、現在は使用される機会は少ない
各薬剤(ファビピラビルとアマンタジンは除く)の適応となる年齢(と用量)をまとめてみます。
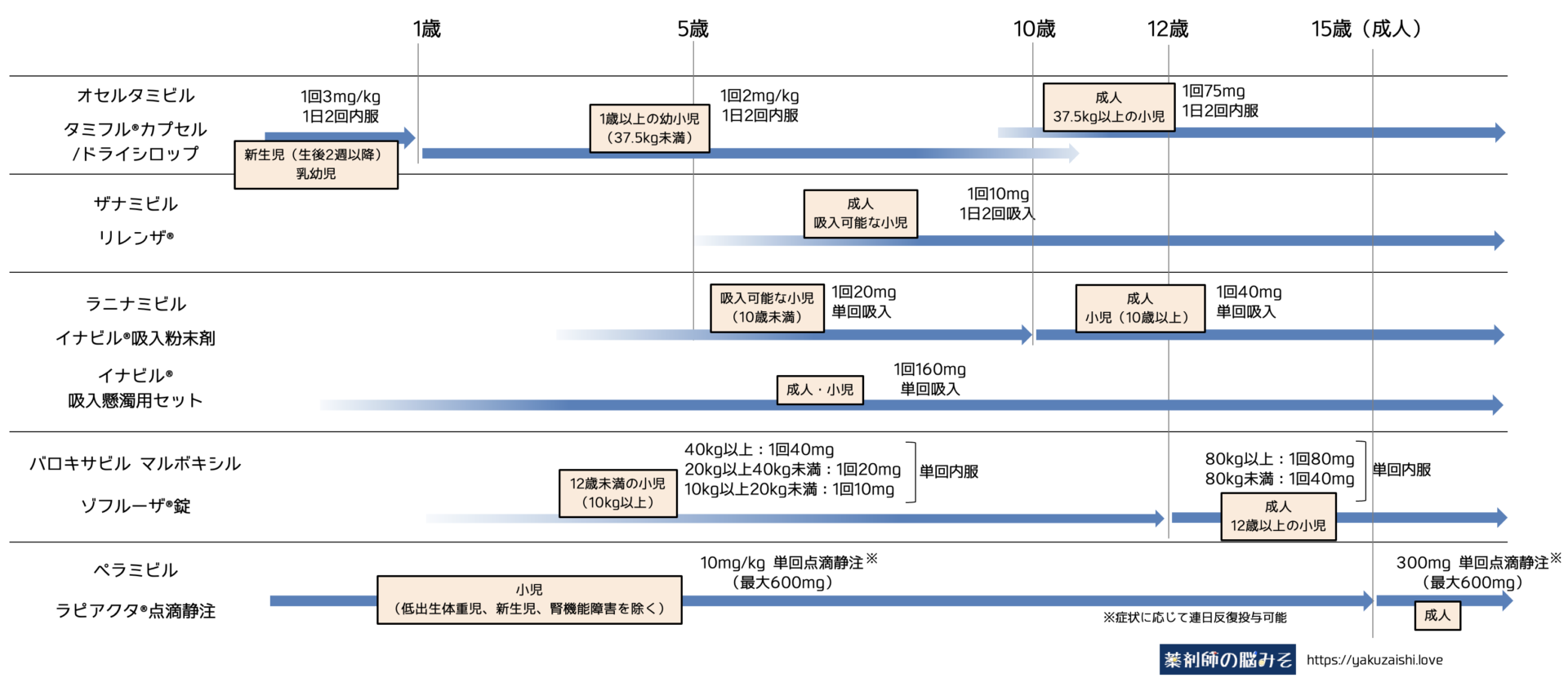
吸入薬への切替
最初に紹介した通り、事務連絡では以下の通り、吸入への切り替えが提案されています。
吸入可能な5歳以上のインフルエンザ患者においては、吸入薬の処方をご検討ください。
インフルエンザに対して適応を持つ吸入薬が存在するのはザナミビルとラニナミビル。
薬剤としてはリレンザ、イナビル吸入粉末剤、イナビル吸入懸濁用セットの3製剤です。
イナビル吸入懸濁用セット
イナビル吸入粉末剤の別剤形。
ジェット式ネブライザを用いて吸入を行うため、自発的に一定の吸気速度による吸入を行うことが難しい乳幼児にも使用可能なのですが、乳幼児に対する十分なデータがないことやエアロゾルを発生させてしまうことから現在の状況では推奨されていません。
2022/23 シーズンのインフルエンザ治療・予防指針 ―2022/23シーズンの流行期を迎えるにあたり(日本小児科学会 予防接種・感染症対策委員会)
リレンザとイナビル吸入粉末剤
どちらもドライパウダー型の吸入薬になります。
吸入を行うためには、一定の吸気速度による自発的な吸入が必要ですが、一般に5歳児以上であれば可能と言われています。
保険適応
リレンザについては添付文書上に以下の記載があるため保険適応が5歳以上です。
9.7 小児等
9.7.1 小児に対しては、本剤を適切に吸入投与できると判断された場合にのみ投与すること。
9.7.2 低出生体重児、新生児、乳児又は4歳以下の幼児を対象とした臨床試験は実施していない。
イナビルについては小児に対する年齢制限はありません。
9.7 小児等
9.7.1 本剤を適切に吸入投与できると判断された場合にのみ投与すること。
9.7.2 幼児へ投与する場合には、患者の状態を十分に観察しながら投与すること。
9.7.3 低出生体重児、新生児又は乳児に対する有効性及び安全性を指標とした臨床試験は実施していない。
どちらも5歳以上であれば保険適応可能ですが、吸入投与可能かどうかの判断が必要です。
イナビルについては吸入確認用笛が存在するので、投薬前に必要な吸入力があるかどうかを音で確認することが可能です。
操作方法
リレンザは吸入デバイスにディスクヘラーが採用されているため、操作が少し複雑です。
それに対してイナビルはシンプルな操作で吸入可能となっています。
投与期間
また、両薬剤では投与期間(吸入回数)が異なります。
- リレンザ:1回2ブリスター 1日2回 5日間(合計20回吸入)
- イナビル:1回2〜4吸入(1〜2キット) 単回吸入(合計2〜4吸入)
リレンザは毎回2吸入を1日2回、それを5日間続ける必要があります。
それに対して、イナビルは1回2吸入(10歳以上は4吸入)の単回で治療を完了できます。
どちらを使う?
これらを踏まえてどちらかを選択することになるのですが、一般的にはイナビルが選択されることが多いと思います。
ただし、イナビルは一回失敗してしまうと薬剤が失われてしまうため、複数回チャンスがあるリレンザを使用するという考えもあるようです。
個人的には吸入確認用笛を用いて、吸入力を確認し、薬剤師が適切な指導を行えばイナビルで問題ないと思いますが、新型コロナウイルスとの同時感染を考えて薬局での吸入を避け、自宅で使用してもらうのであれば、複数回投与可能なリレンザを選択肢に入れてもいいと思います。
イナビルを薬局で吸入してもらうのがベストだとは思いますが、自分たちは対策できても、他の患者さんの感染リスクをなくすことは難しいです。
どうしても待合室での滞在時間が増えてしまいますし、吸入を行ってもらうとなると飛沫が飛散してしまいます。
隔離室があれば話は別ですが、そうでなければ多くの患児を対応するのは難しそうです。
吸入薬以外の薬剤は選択肢に入らないのか?
オセルタミビル以外で小児が使用可能な薬剤としてペラミビル(ラピアクタ点滴静注用)とバロキサビル マルボキシル(ゾフルーザ錠)があります。
ペラミビルについては新生児を除く乳幼児(生後1ヶ月以降)に対して使用可能ですが、入院時の対応が基本とされ、外来診療で積極的に使用するには無理があります。
バロキサビル マルボキシルについてはデータの蓄積が不十分であること、小児については耐性化に対する懸念が払拭されていないため非推奨となっています。
ゾフルーザ顆粒が承認後に薬価収載されていないのはその辺りが確立されていないためだと思います。
2022/23 シーズンのインフルエンザ治療・予防指針 ―2022/23シーズンの流行期を迎えるにあたり(日本小児科学会 予防接種・感染症対策委員会)
脱カプセルによる調剤
「医療機関及び薬局におかれては、オセルタミビルリン酸塩ドライシロップが不足している状況にあっても、当該品目を処方又は調剤する必要がある場合には、オセルタミビルリン酸塩カプセルを脱カプセルし、賦形剤を加えるなどの調剤上の工夫を行った上での調剤を検討いただきたいこと。」
ということで、吸入薬がダメであればタミフルカプセル、もしくはオセルタミビルカプセル「サワイ」の脱カプセルを行い、散剤として投薬するしかありません。
タミフルカプセルの脱カプセルを行わざるを得なくなったのはこれが初めてではありません。
2009年にH1N1亜型 新型インフルエンザのパンデミックが起きた時にもタミフルドライシロップの供給が滞りました。
その頃はタミフルドライシロップの期限が短いこともあって、需要に対して供給が間に合わなかったと記憶しています。
(2009年9月までは有効期限は2年でしたが、その後、順次延長されています。)
タミフルドライシロップの有効期限延長
- 2009年9月7日:2年→3年(タミフルカプセル75、ドライシロップ3% 添加物変更並びに使用期限延長のご案内)
- 2011年12月2日:3年→4年(タミフルドライシロップ3% 使用期限延長のご案内)
- 2012年10月1日:4年→6年(タミフルドライシロップ3% 包装仕様変更および使用期限延長のご案内)
- 2013年11月1日:6年→7年(タミフルドライシロップ3% 使用期限延長および包装仕様変更のご案内)
※出荷開始に伴う再案内 2014年11月17日:(タミフルカプセル75、ドライシロップ3% 使用期限延長および包装仕様の変更のご案内) - 2017年1月13日:7年→10年(タミフルドライシロップ3% 使用期限延長のご案内)
2年しかなかった期限が今や10年に!企業努力の賜物ですね。
タミフルDS不足に伴う脱カプセルは自家製剤加算を算定可能
新型インフルエンザに関連する診療報酬の取扱いについて(事務連絡 平成21年5月26日)
今回も疑義解釈という形で同様の内容が案内されています。
疑義解釈資料の送付について(その60)(事務連絡 令和5年11月8日)
調剤報酬点数表関係
【自家製剤加算】
問1 インフルエンザが流行している状況下で、オセルタミビルリン酸塩のドライシロップ製剤の供給が限定されているため、保険薬局において同製剤が不足し、処方への対応が困難な際に、薬剤師が、処方医と相談の上、カプセル剤を脱カプセルし、賦形剤を加えるなどして調剤した場合、自家製剤加算を算定できるのか。(答)「オセルタミビルリン酸塩ドライシロップの在庫逼迫に伴う協力依頼」(令和5年11月8日付け厚生労働省医政局医薬産業振興・医療情報企画課事務連絡)の記の3において、「医療機関及び薬局におかれては、オセルタミビルリン酸塩ドライシロップが不足している状況にあっても、当該品目を処方又は調剤する必要がある場合には、オセルタミビルリン酸塩カプセルを脱カプセルし、賦形剤を加えるなどの調剤上の工夫を行った上での調剤を検討いただきたいこと。」とされているなか、やむをえず当該対応を実施した場合には、自家製剤加算を算定して差し支えない。なお、このような場合には、レセプトの摘要欄に「オセルタミビルリン酸塩ドライシロップ製剤の不足のため」等のやむを得ない事情を記載すること。 また、この場合の薬剤料については、オセルタミビルリン酸塩カプセルの実際の投与量に相当する分(例えば、5日間でオセルタミビルとして合計262.5mg投与する場合は、オセルタミビルリン酸塩カプセル75mgの3.5カプセル分)を請求するものとする。
ということで、オセルタミビルのドライシロップが不足している場合には脱カプセルを行って対応することで自家製剤加算を算定可能です。
ただし、以下の点に注意が必要です。
- レセプト摘要欄に「オセルタミビルリン酸塩ドライシロップ製剤の不足のため」と記載する
- 薬剤料として請求できるのは実際に投薬した分だけ(調製の際に生じるカプセルのロス分は請求できない)
タミフルカプセル75の脱カプセル
さて、実際にタミフルカプセルを脱capする際の考え方をまとめてみます。
濃度は自由に決めていいですが、調剤上のミスを減らすためにドライシロップに合わせた3%とするのが無難と思います。
計算をわかりやすくするため、オセルタミビルを合計300mg含有する3%の散剤を調整する場合を考えます。
タミフルカプセル75を脱カプセルしてオセルタミビルを3%含有する散剤を調製する方法
タミフルカプセル75 4カプセル = オセルタミビル300mg
有効成分を300mgを3%の散剤とするには全量10g(10000mg)とする必要がある
タミフルカプセル75を脱カプセルした際の内容物の重量は1カプセルあたり165mg(0.165g) → 4カプセルでは660mg(0.66g)
↑ Point! 先発のタミフルカプセル75と後発のオセルタミビルカプセル75mg「サワイ」では内容物の重量が異なります
10g − 0.66g = 9.340g
タミフルカプセル75 4カプセルを脱カプセルしたものに9.340gの乳糖を加えてしっかり混和することでオセルタミビルを3%含有する散剤10gを調製できる
- オセルタミビル1日量(力価)
- タミフルドライシロップ3%の1日量(用量)
- タミフルカプセル75の1日量(用量)
- タミフルカプセル75の総投与量(5日分)
- 脱capした際の内容物の総量(5日分)
- 3%に調製する際の乳糖の量(5日分)
- タミフルドライシロップ3%の5日間総量(調製後の5日間総量)
- オレンジ:処方箋記載
- 緑:タミフルカプセル
- 青:調製に必要な乳糖+分包前の最終秤量
1歳以上のタミフルカプセル75 脱カプセル 用量・調製量早見表
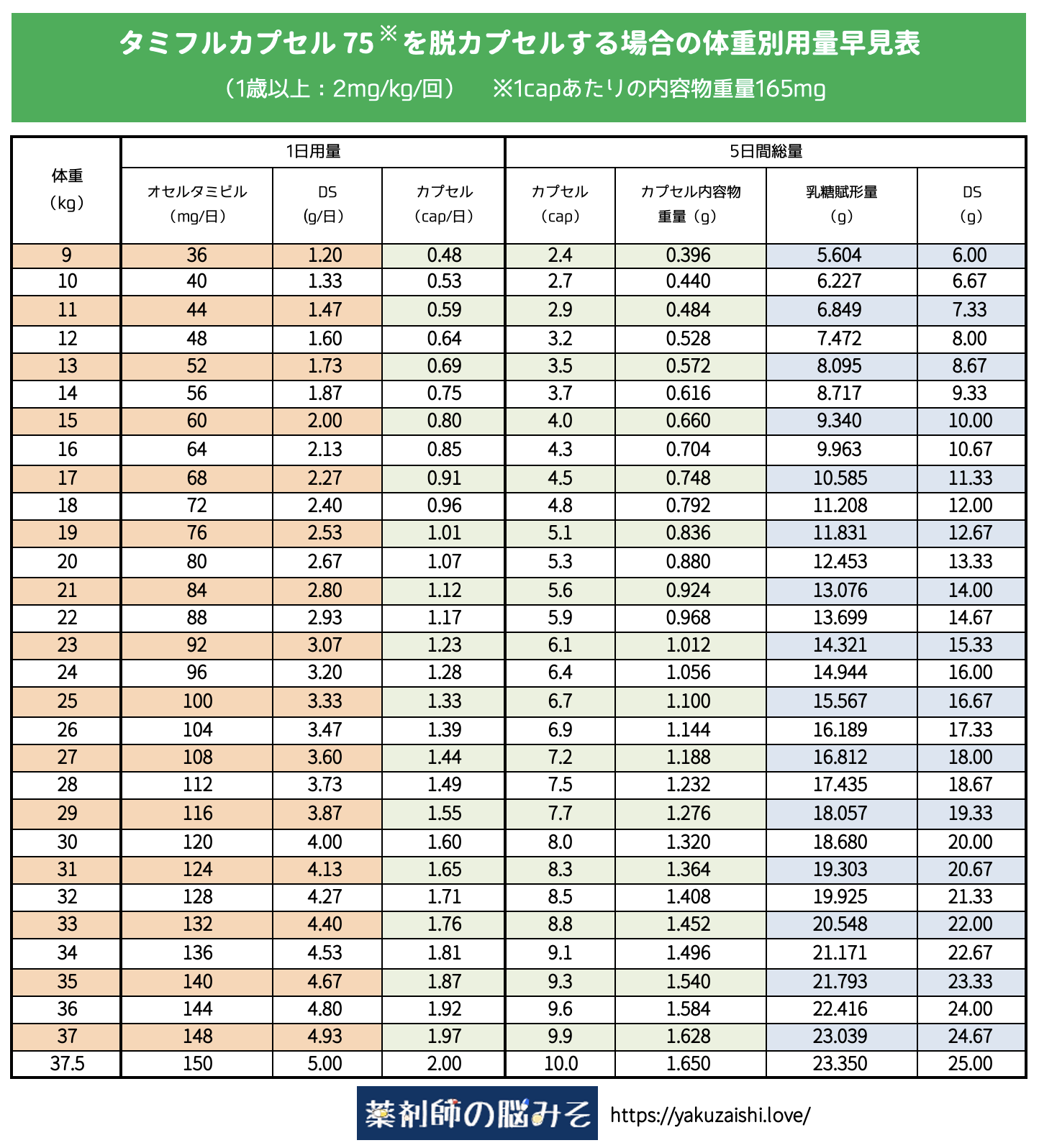
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
1歳未満のタミフルカプセル75 脱カプセル 用量・調製量早見表
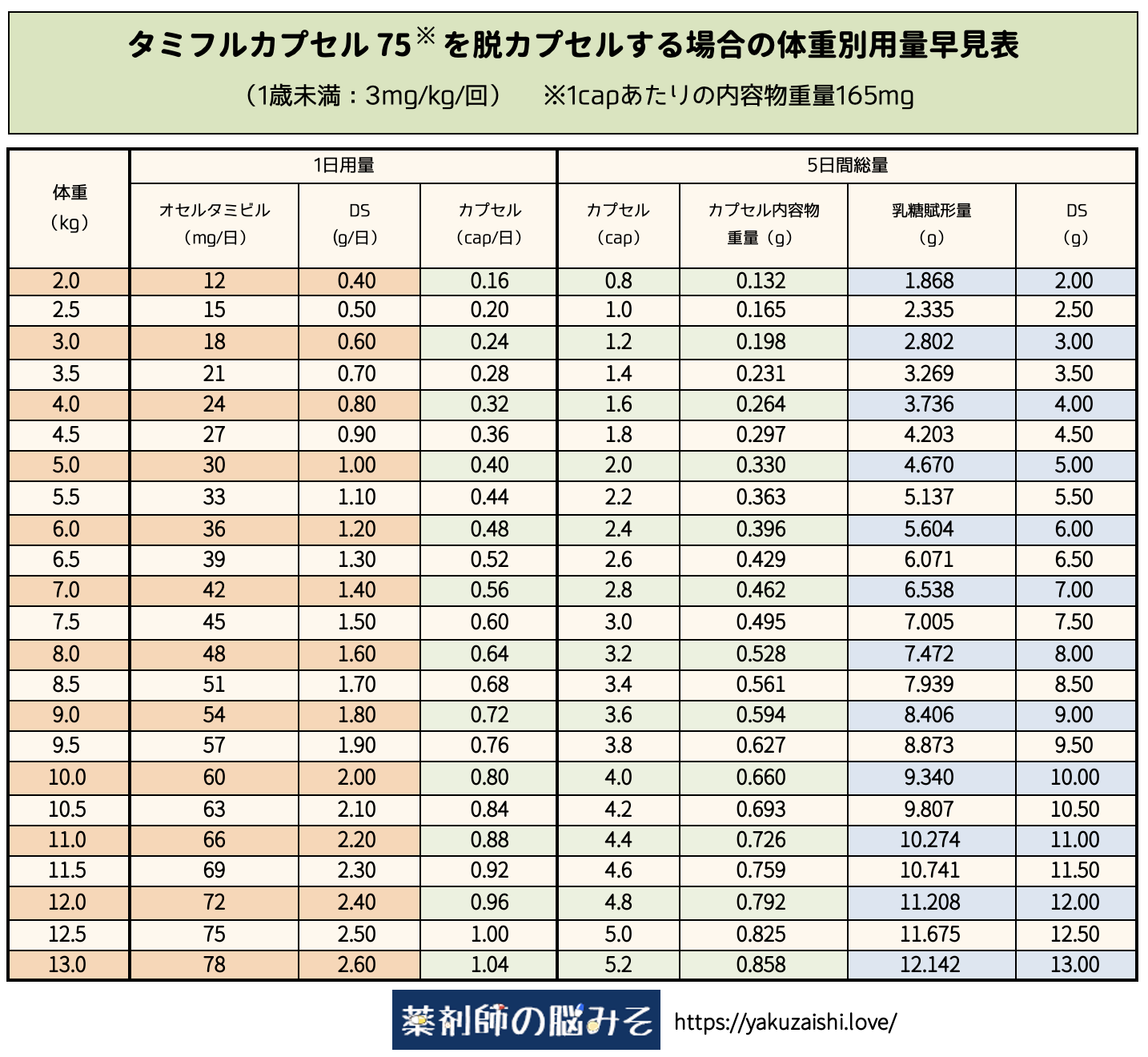
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
オセルタミビルカプセル75mg「サワイ」の脱カプセル
続いてタミフルカプセル75の後発品であるオセルタミビルカプセル75mg「サワイ」を脱capする際の考え方をまとめてみます。
タミフル同様に、オセルタミビルを合計300mg含有する3%の散剤を調整する場合を考えます。
オセルタミビルカプセル75mg「サワイ」を脱カプセルしてオセルタミビルを3%含有する散剤を調製する方法
オセルタミビルカプセル75mg「サワイ」 4カプセル = オセルタミビル300mg
有効成分を300mgを3%の散剤とするには全量10g(10000mg)とする必要がある
オセルタミビルカプセル75mg「サワイ」を脱カプセルした際の内容物の重量は1カプセルあたり130mg(0.13g) → 4カプセルでは520mg(0.52g)
↑ Point! 先発のタミフルカプセル75と後発のオセルタミビルカプセル75mg「サワイ」では内容物の重量が異なります
10g − 0.52g = 9.48g
オセルタミビルカプセル75mg「サワイ」 4カプセルを脱カプセルしたものに9.48gの乳糖を加えてしっかり混和することでオセルタミビルを3%含有する散剤10gを調製できる
1歳以上のオセルタミビルカプセル75mg「サワイ」 脱カプセル 用量・調製量早見表
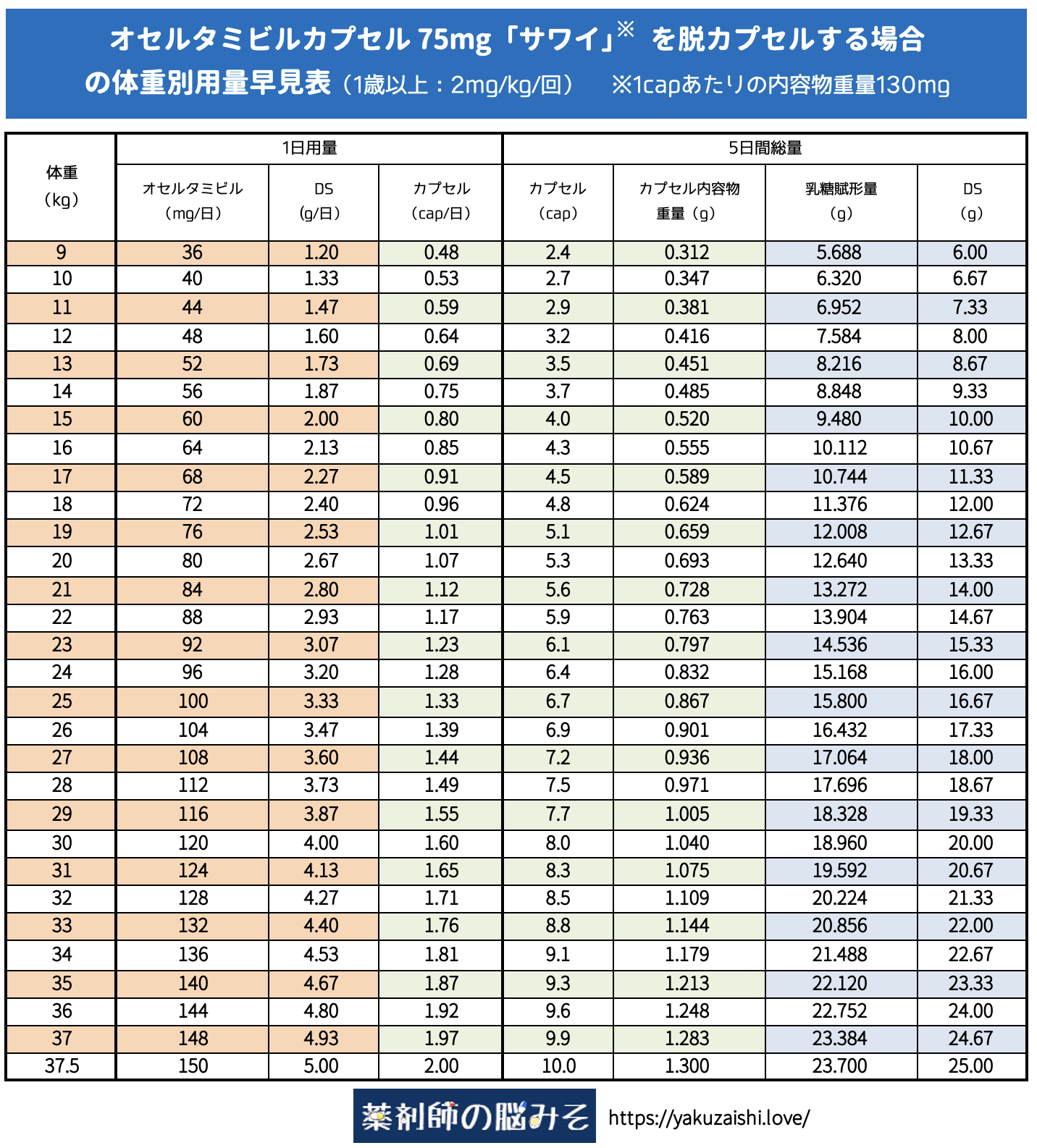
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
1歳未満のオセルタミビルカプセル75mg「サワイ」 脱カプセル 用量・調製量早見表
続いて1歳未満の場合です。
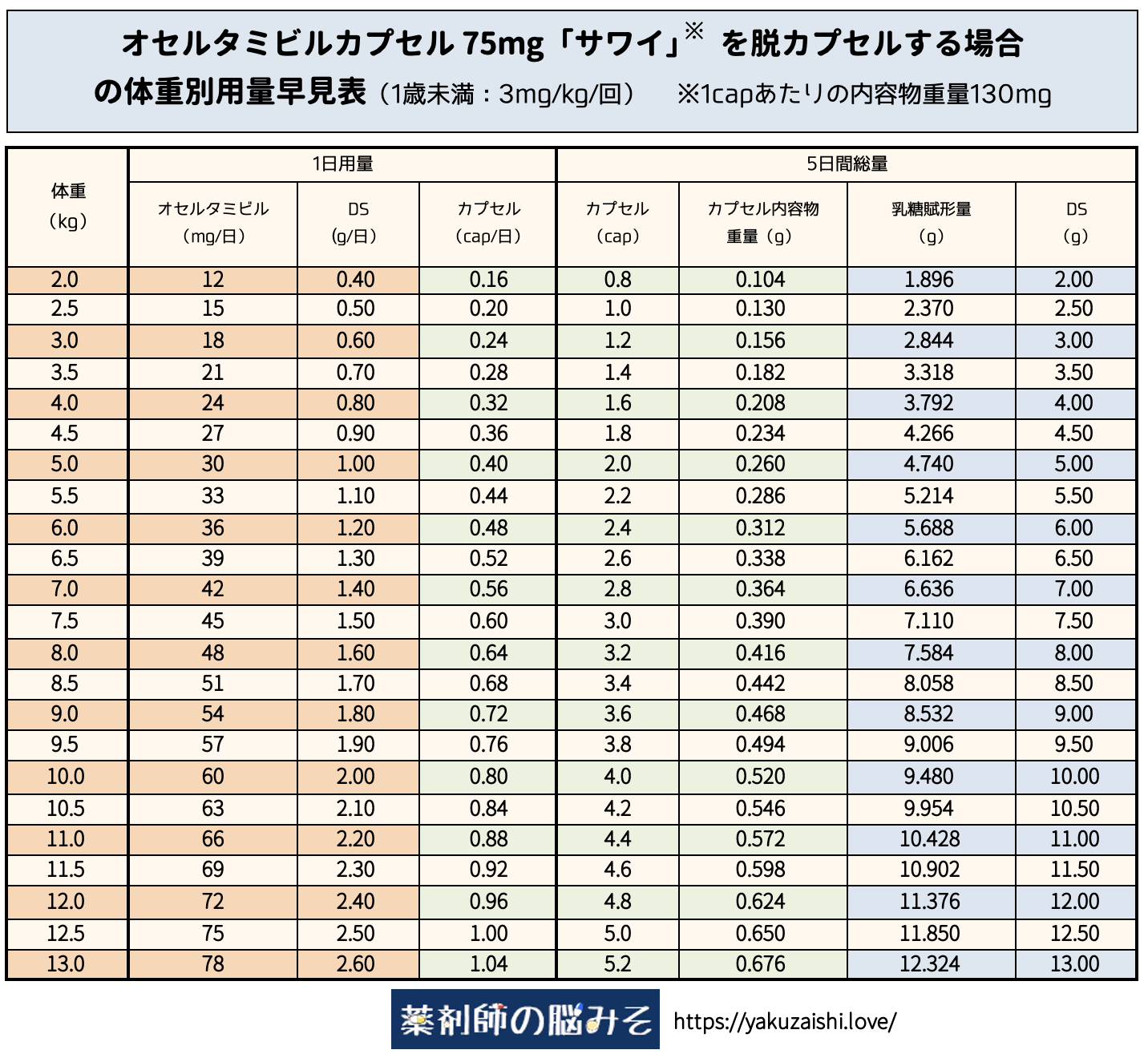
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
オセルタミビル錠75mg「トーワ」の脱カプセル
続いてタミフルカプセル75の後発品(剤形違い)であるオセルタミビル錠75mg「トーワ」を粉砕する際の考え方をまとめてみます。
タミフル同様に、オセルタミビルを合計300mg含有する3%の散剤を調整する場合を考えます。
オセルタミビル錠75mg「トーワ」を粉砕してオセルタミビルを3%含有する散剤を調製する方法
オセルタミビル錠75mg「トーワ」 4錠 = オセルタミビル300mg
有効成分を300mgを3%の散剤とするには全量10g(10000mg)とする必要がある
オセルタミビル錠75mg「トーワ」を粉砕した際の内容物の重量は1錠あたり144mg(0.144g) → 4錠では約580mg(0.58g)
10g − 0.58g = 9.42g
オセルタミビル錠75mg「トーワ」 4錠を粉砕したものに9.42gの乳糖を加えてしっかり混和することでオセルタミビルを3%含有する散剤10gを調製できる
粉砕するかどうかはあくまでも医療従事者の判断
1歳以上のオセルタミビル錠75mg「トーワ」 粉砕 用量・調製量早見表
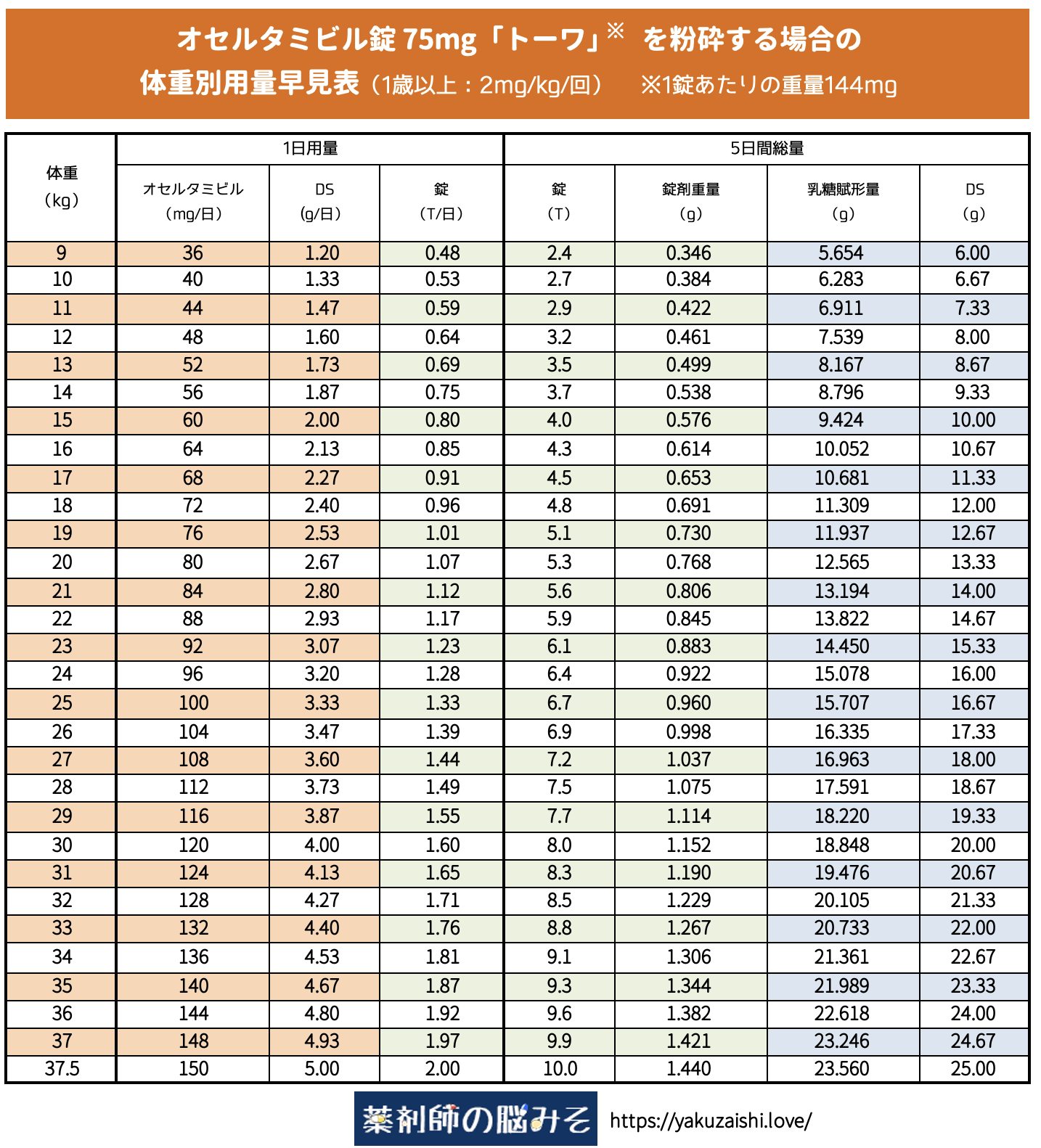
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
1歳未満のオセルタミビル錠75mg「トーワ」 粉砕 用量・調製量早見表
続いて1歳未満の場合です。
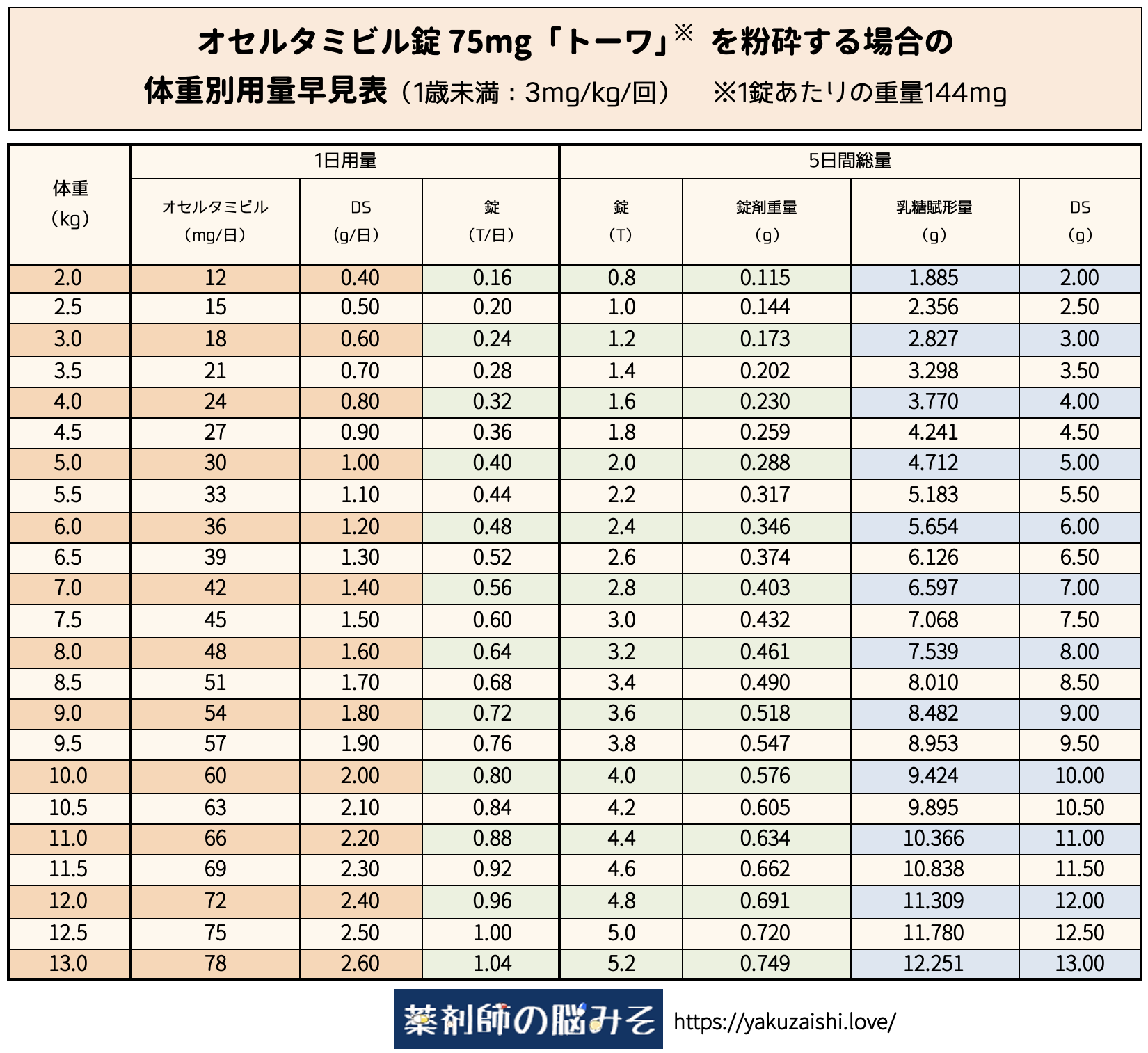
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
脱cap予製の早見表
処方量が多い場合、予製を作成することになると思います。
これについても、タミフルカプセル75、オセルタミビルカプセル75mg「サワイ」それぞれで早見表を作成してみました。
タミフルカプセル75 脱カプセル 予製早見表
次に先発品のタミフルカプセル75を脱カプセルする場合の早見表です。
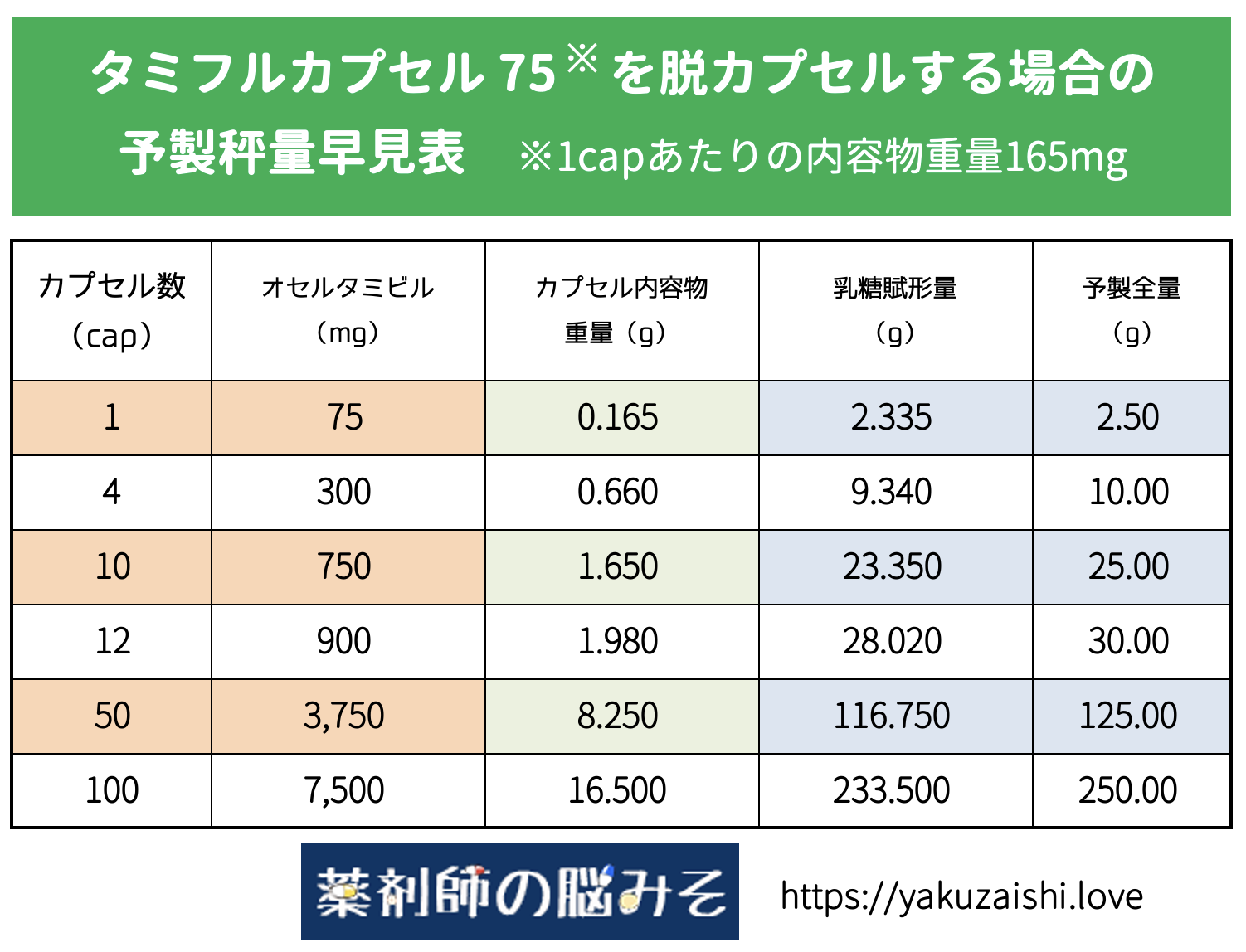
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
オセルタミビルカプセル75mg「サワイ」 脱カプセル 予製早見表
次に後発品のオセルタミビルカプセル75mg「サワイ」を脱カプセルする場合の早見表です。
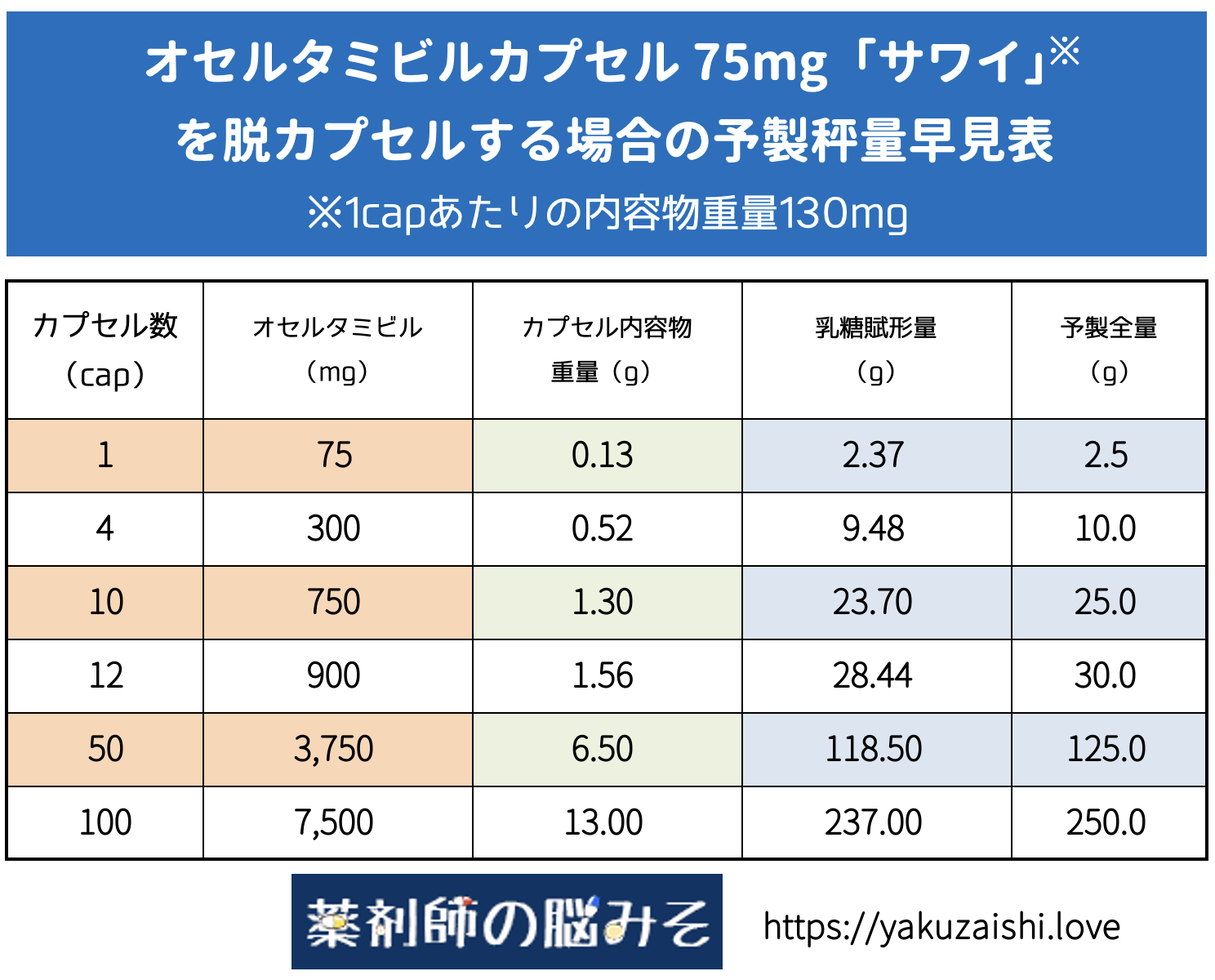
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
オセルタミビル錠75mg「トーワ」粉砕 予製早見表
次に後発品のオセルタミビル錠75mg「トーワ」を粉砕する場合の早見表です。
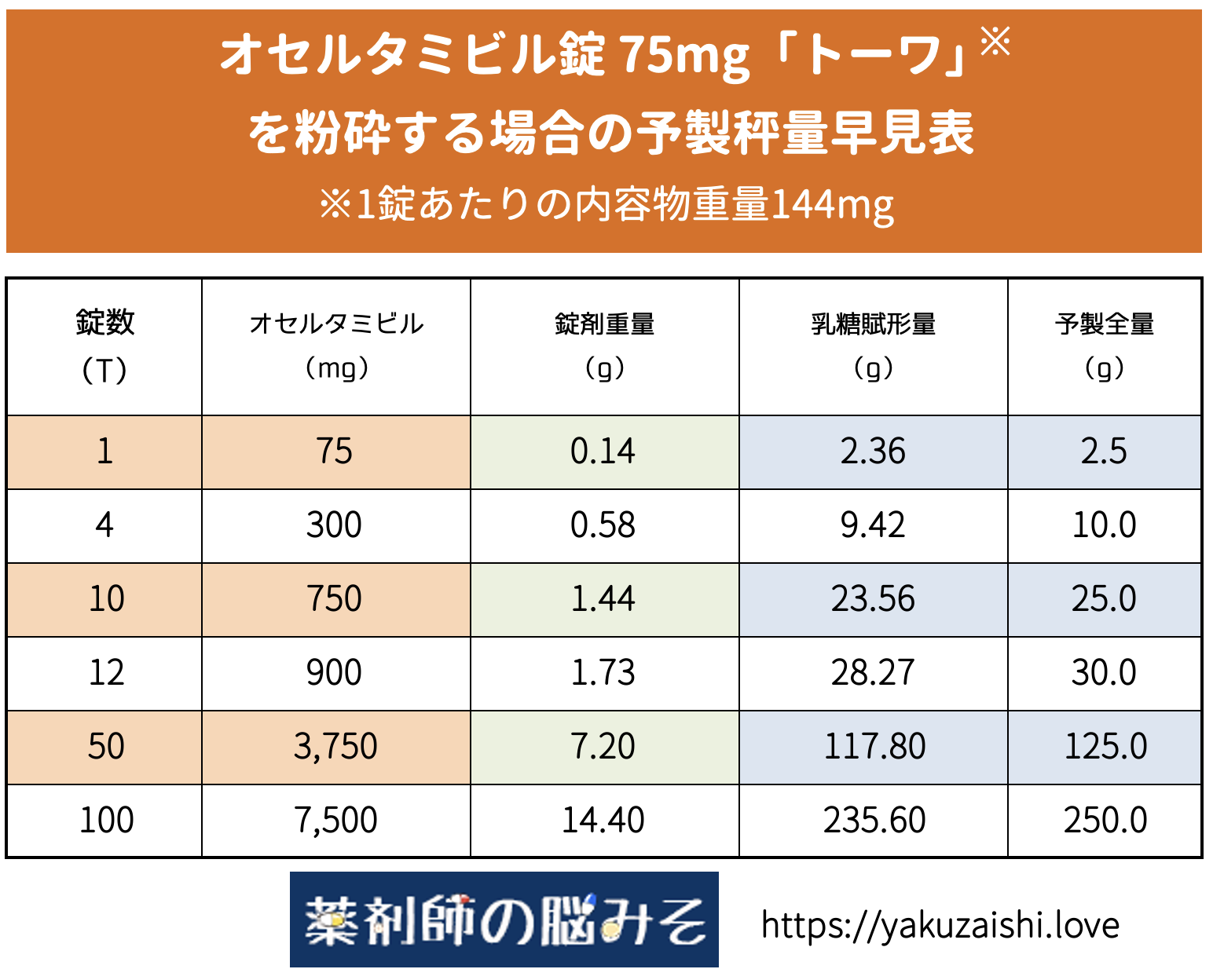
※十分確認を行っているつもりですが、使用する際には自己責任でお願いします
脱カプセルの苦味に対する対応
タミフルドライシロップやオセルタミビルDSが苦いことは広くしられているので、タミフル(オセルタミビル)を脱カプセルしたものが苦いことは想像できると思います。
実際に2009年に脱カプセルの対応が行われた際も苦味が問題となりました。
そこで苦味対策として用いられたのがミルクココアです。
ミルクココアと砂糖を混ぜることがオセルタミビルの苦味の緩和に有効と言われ、患者さんにミルクココアと混ぜることを勧めたり、薬局の調製段階でミルクココアを混ぜて準備する方法が実施されました。
千葉県薬剤師会ではタミフルカプセル75を脱カプセルしたものを白糖、ミルクココアと混和した場合の安定性試験を実施し、データを公開しています。
タミフルカプセル75 脱カプセル マニュアル|社団法人千葉県薬剤師会 薬事情報センター(平成21年11月17日)
個人的には調製段階でミルクココアを混ぜるのは、分包機を汚してしまうので避けたいところですが、薬局で適当な分量に分けて配布・販売する等を検討してもいいんじゃないかと思います。
ちなみに、立冬は「ココアの日」と定められています。(森永製菓株式会社)
2023年の立冬は11月8日・・・。
タミフルドライシロップ3%の限定出荷が発表され、厚労省がタミフル脱カプセル等の対応についての事務連絡を公開した日が「ココアの日」だなんて、なかなか笑えない話ですね。
まとめ
今回はタミフルドライシロップの供給不安に伴う、吸入薬・他薬への切替、脱カプセルの調製方法についてまとめてみました。
今後、タミフルドライシロップの出荷調整がどのくらい影響するかはインフルエンザの流行状況次第ではありますが、おそらく切り替えを検討する時はやってきそうですね。
最後に、厚生労働省の通知のうち、本文で触れなかったところ。
- 「返品が生じないよう、過剰な発注は厳に控えていただき、当面の必要量に見合う量のみの購入をお願いしたい」
- 「自らの店舗だけでは供給が困難な場合であっても、系列店舗や地域における連携により、可能な限り患者への供給ができるよう調整をしていただきたい」
これ、どちらも現在起きている供給不安の対応として、重大なテーマだと思うんです。
購入についてはどこの薬局・医療機関も自身の患者さんのために行なっていることですし、地域での供給についても同様の考えで進みにくいところがあると思います。
このあたりの考え方については、現場での自浄作用を促すだけでは限界があると思います。
なにか、一定の線引きが必要なんじゃないかと思うのですが・・・。
参考資料
中外製薬株式会社 「限定出荷に関するご案内 抗インフルエンザウイルス剤 「タミフルⓇドライシロップ3%」」(2023年11月)沢井製薬株式会社 「オセルタミビルDS3%「サワイ」の供給に関するお詫びとお願い」(2023年11月)厚生労働省医政局医薬産業振興・医療情報企画課 「オセルタミビルリン酸塩ドライシロップの在庫逼迫に伴う協力依頼」(事務連絡 令和5年11月8日)2022/23 シーズンのインフルエンザ治療・予防指針 ―2022/23シーズンの流行期を迎えるにあたり(日本小児科学会 予防接種・感染症対策委員会)
「臨床と研究」(2012;89[11];1606-10)
各製品添付文書/インタビューフォーム
新型インフルエンザに関連する診療報酬の取扱いについて(事務連絡 平成21年5月26日)
新型インフルエンザに係るタミフル等に関するQ&Aについて(事務連絡 平成21年11月6日)
疑義解釈資料の送付について(その60)(事務連絡 令和5年11月8日)
中外製薬 タミフルカプセル75 脱カプセル用量早見表(2023年11月)
沢井製薬 オセルタミビルカプセル75mg「サワイ」 脱カプセル用量早見表(2023年11月)








