令和3年6月1日、「ジョイクル関節注によるショック、アナフィラキシー」について安全性速報(ブルーレター)が発出されました。
ブルーレターが出されたのは、令和元年5月17日の「ベージニオ錠による重篤な間質性肺疾患」以来となります。
ジョイクル関節注は令和3年5月19日に薬価収載、販売開始されたばかりなので、発売から2週間を待たずにブルーレターが発出されてしまう事態となってしまいました。
今回、このブルーレターの内容と、それを受けて考えたことについてまとめたいと思います。
ジョイクル関節注とは?
ジョイクル関節注は、生化学工業独自の薬剤結合技術により、ヒアルロン酸にジクロフェナクを化学結合した薬剤(ジクロフェナクエタルヒアルロン酸ナトリウム)です。
2021年3月23日に生化学工業が製造販売承認を取得し、販売元は小野薬品となっています。
2021年5月19日に薬価収載され、即日販売開始となりました。
関節腔内に注射されたジクロフェナクエタルヒアルロン酸ナトリウムは局所に留まりながら加水分解を受けてジクロフェナクを放出します。
この特性により、ジョイクル間接注はヒアルロン酸による関節機能改善作用と、少しずつ放出されるジクロフェナクによる持続的な消炎鎮痛作用を発揮します。
ジョイクル関節注の適応は「変形性関節症(膝関節、股関節)」となっており、変形性膝関節症のみではなく、変形性股関節症に対しても使用可能です。
変形性股関節症に対する適応を有するヒアルロン酸製剤は、現時点ではジョイクル関節注のみとなっています。(2021年6月現在)
また、用法・用量が「通常、成人1回1シリンジ(ジクロフェナクエタルヒアルロン酸ナトリウムとして1回30mg)を4週間ごとに関節腔内に投与する。」となっていることからもわかるように、4週間に1回の注射で投与可能な初のヒアルロン酸製剤でもあります。(従来のヒアルロン酸製剤は週1回投与)
投与間隔が広がることで、患者さんの通院回数、注射回数を減らすことが可能となり。QOLの向上も期待されます。
関節腔内に注射されたジクロフェナクエタルヒアルロン酸ナトリウムはほとんどが関節腔内に貯留し、血中に移行するものはごくわずかです。
その結果、関節腔内のみでジクロフェナクの効果が発揮され、経口投与と比較して全身の副作用リスクを回避することが期待されます。
(最後にまとめますが、この期待を過大評価してしまったことが今回のブルーレター発出につながっているのではないかと考えます)
ちなみに名称の由来は『JOY「喜び、Joint(関節)、ヒアルロン酸ナトリウムとジクロフェナクとの Joint(結合)」と、CLU「来る、Diclofenac」から』だそうです。
ブルーレターの詳しい内容
まずはPmdaに掲載されている情報を整理します。
- 安全性情報(ブルーレター):ジョイクル関節注30mgによるショック、アナフィラキシーについて
- 「ジョイクル関節注30mg」を投与される患者様とご家族の皆様へ
- 関節機能改善剤「ジョイクル関節注30mg」投与患者におけるショック、アナフィラキシーに関する注意喚起について
(別添1:品目情報)
(別添2:ブルーレター)
(別添3:令和3年6月1日付通知「医薬品の「使用上の注意」の改訂及び安全性速報の配布等について」)
ショック・アナフィラキシーの症例数
今回のブルーレター発出にいたった段階での症例数は以下の通りです。
2021年3月23日の製造販売承認取得以降、5月28日までの間に、本剤使用患者において重篤なショック、アナフィラキシーの症例が 10例報告されています(推定使用患者数 約5,500人)。 このうち1例は、因果関係は不明ですが、死亡に至った症例として報告されています。
安全性情報(ブルーレター):ジョイクル関節注30mgによるショック、アナフィラキシーについて
添付文書の改訂指示
ブルーレターの発出にあわせてジョイクルの添付文書が改訂されています。
まず、警告が追加されています。(改訂前は警告なし)
1. 警告
本剤投与により重篤なショック、アナフィラキシーが発現することがあるので、本剤は、緊急時に十分な対応のできる準備をした上で投与し、投与後も十分な観察を行うこと。〔8.1、11.1.1 参照〕安全性情報(ブルーレター):ジョイクル関節注30mgによるショック、アナフィラキシーについて
次に重要な基本的注意に以下の内容が追記されています。
(8.1〜8.3だったところに8.1が挿入)
8. 重要な基本的注意
8.1 本剤投与により重篤なショック、アナフィラキシーが発現することがあるので、投与に際しては、緊急処置を取れる準備をすること。投与中及び投与後は患者の状態を十分に観察すること。 また、ショック、アナフィラキシーが発現する可能性があること、及びその徴候や症状について患者又は家族等に十分に説明し、異常が認められた場合には、速やかに医療機関を受診するよう、患者等を指導すること。[1、11.1.1 参照]安全性情報(ブルーレター):ジョイクル関節注30mgによるショック、アナフィラキシーについて
最後に、細かい部分ですが、重大な副作用のショック、アナフィラキシーの部分に上記2カ所の参照が加えられています。
11. 副作用
11.1 重大な副作用
11.1.1 ショック、アナフィラキシー(0.4%)〔1、8.1 参照〕安全性情報(ブルーレター):ジョイクル関節注30mgによるショック、アナフィラキシーについて
医療機関での対応
厚生労働省からの『関節機能改善剤「ジョイクル関節注30mg」投与患者におけるショック、アナフィラキシーに関する注意喚起について』には以下の通り記載されています。
【今回の医療関係者に対する注意喚起のポイント】
本剤使用患者において重篤なショック、アナフィラキシーの症例が報告されていることから、次の事項に十分に注意すること。
1.本剤の投与に際しては、緊急時に十分な対応のできる準備をした上で行うこと。
2.本剤の投与後少なくとも30分間は、医師の管理下で患者の状態を十分に観察すること。投与直後に限らず、医療機関から帰宅後に発現している症例も報告されている点に留意すること。
3.患者又は家族等に対して、ショック、アナフィラキシーが発現する可能性があること、及びその徴候や症状について十分に説明し、異常が認められた場合には、速やかに医療機関を受診するよう指導すること。関節機能改善剤「ジョイクル関節注30mg」投与患者におけるショック、アナフィラキシーに関する注意喚起について
患者さんへの案内
患者さんとそのご家族向けの案内も公開されています。
厚生労働省からの『関節機能改善剤「ジョイクル関節注30mg」投与患者におけるショック、アナフィラキシーに関する注意喚起について』には以下の通り記載されています。
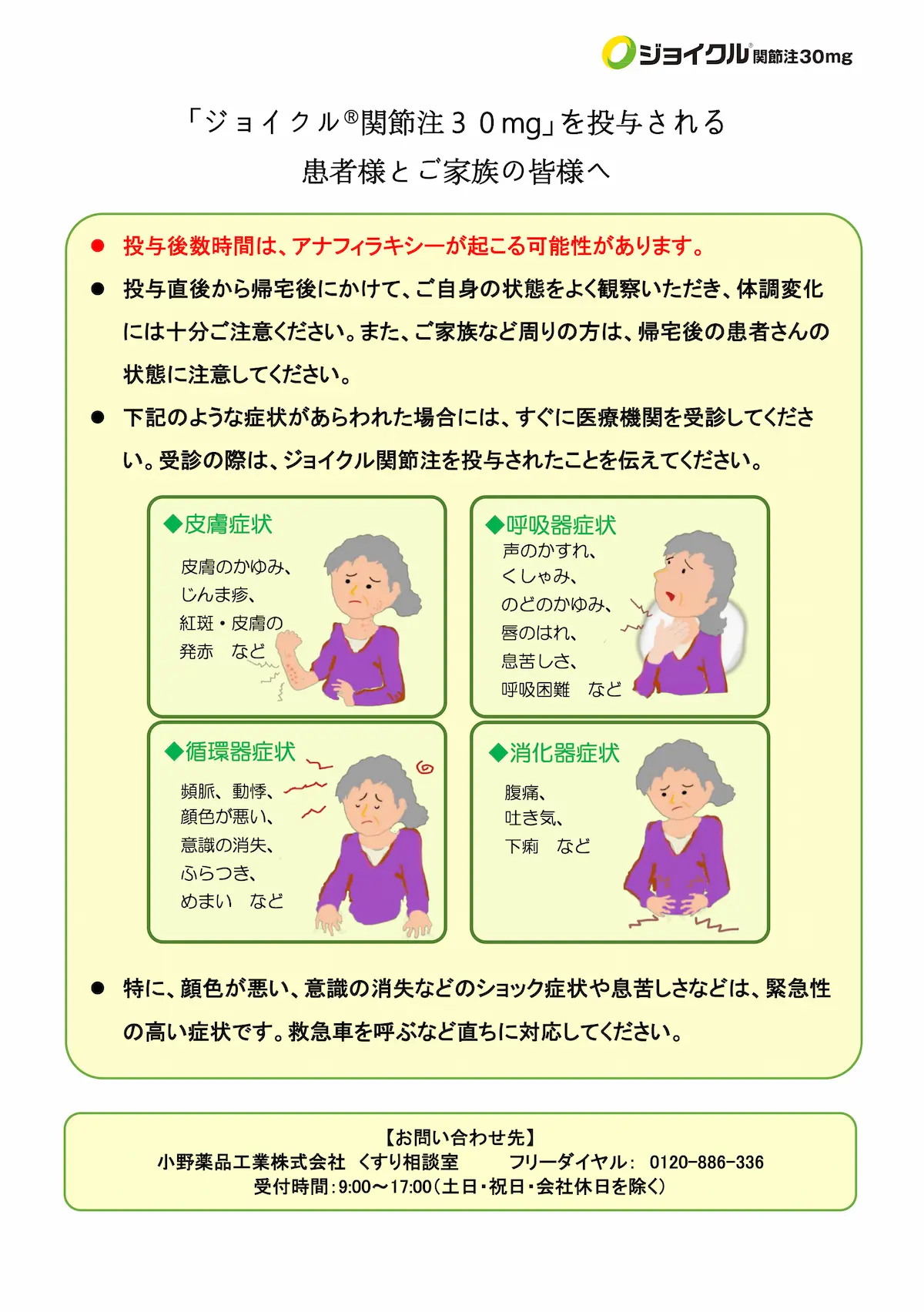
患者・家族向けのリーフレットの概要
○ 本剤投与後数時間は、アナフィラキシーが起こる可能性があること。
○ 投与直後から帰宅後にかけて、状態をよく観察いただき、体調変化には十分注意すること。
○ 異常が認められた場合には、すぐに医療機関を受診すること。受診の際は「ジョイクル関節注」の投与を受けたことを伝えること。
○ 特に顔色が悪い、意識の消失、息苦しさなどは緊急性の高い症状であり、救急車を呼ぶなど直ちに対応すること。関節機能改善剤「ジョイクル関節注30mg」投与患者におけるショック、アナフィラキシーに関する注意喚起について
ジョイクルのリスクについて考えてみる
今回のブルーレター発出を受け、当初は想定以上のアナフィラキシーやショックが報告されたのだと思ったのですが、添付文書(改訂前)を読んでみると想定外とは言えなかったことがわかります。
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
11.1.1 ショック、アナフィラキシー(0.4%)ジョイクル関節注30mg 添付文書 小野薬品工業
さらに、ショック、アナフィラキシーについてはRMP(リスク管理計画)の中で「重要な特定されたリスク」としてあげられています。
重要な特定されたリスクとした理由:
・ 本剤においては、国内第III相試験において、本剤群に、本剤との因果関係が否定できないアナフィラキシー(アナフィラキシー反応およびアナフィラキシーショック)が0.4%(2/532例)報告されている。
・ ショック、アナフィラキシーは発現した場合は重篤な転帰をたどる場合がある。
以上の理由により、「ショック、アナフィラキシー」を重要な特定されたリスクとし た。ジョイクル関節注30mgに係る医薬品リスク管理計画書 生化学工業株式会社
国内第Ⅲ相試験の段階でアナフィラキシーが0.4%(2/532例)報告されています。
ブルーレター発出の段階(製造販売承認取得2021年3月23日〜2021年5月28日)でのアナフィラキシーが0.18%(10/5500例 推定)なので、今回のアナフィラキシーは想定の範囲内と言えるのではないかと思われます。
臨床試験では症例数が532例中の2例と少ないため評価が難しいところだったと思いますが、この点についてはもっと追求してもよかったのではないかと思います。
と言っても自分自身、今回のブルーレターを受けてそれに気づけたわけですから、発売時にこれを重く見ることはできていませんでした。(ジョイクル関節注が薬局で採用することのない薬剤ということもありますが・・・)
0.4%という数値だけ見て2例という症例数を見ないと過大評価になってしまいますし、2例という症例数だけ見て0.4%という数値を軽く見ると過小評価になってしまうので、この数字の評価は非常に難しいところだとは思います。
また、アナフィラキシーという副作用に対する先入観もあるのではないかと考えます。
ショックやアナフィラキシーは死亡に繋がる可能性もある重大な副作用ですが、アレルギー性の有害事象であるため、ほとんどの薬剤で引き起こされる可能性があります。
そのため、特別な注意喚起がない限り、その頻度について評価しようとする意識が低くなってしまいがちです。
特にジョイクル関節注は「経口投与と比較してジクロフェナクの全身暴露量が少ない」ということを「安全性が高い」と置き換えて評価してしまったところがあるのではないかと思われます。
安全性を過大評価した結果が副作用の続出に繋がったケース
安全と思っていた新薬で次々と副作用が報告される・・・。
このケースは今回のジョイクル関節注がはじめてではありません。
一つ目の例がプラザキサカプセル75mg、プラザキサカプセル110mgによる重篤な出血についてです。
初のDOAC(NOAC)として登場したプラザキサですが、ワーファリンと比較して用量調節が容易というイメージが先行してしまった結果、腎機能の評価が十分に行われずに重篤な出血を引き起こしてしまった報告が相次ぎ、ブルーレターが発出されました。
また、ブルーレターの発出には至っていませんが、DPP-4阻害薬が発売された当初、SU薬との併用で低血糖が相次いだ結果、日本糖尿病協会と日本糖尿病学会が「インクレチンとSU薬の適正使用に関する委員会」を立ち上げ上げ、インクレチン関連薬とスルホニル尿素薬(SU薬)の適正使用についての勧告を公開しています。
DPP4阻害薬は従来の糖尿病薬と比較して低血糖リスクが極めて少ないというイメージが先行してしまった結果でした。
新薬登場時に薬剤師が果たすべき役割
個人的に、今回のジョイクルのアナフィラキシーについても上にあげたケースと同様、安全性に対する過大評価が引き起こしてしまったのではないかと考えています。
従来の薬剤と比較して安全性が期待される薬剤が登場した場合、どうしてもプロモーション上その特徴が説明され、その説明を聞いた医療従事者はその薬剤は安全なものとして認識してしまいがちです。
このような薬剤が登場した時こそ、薬剤師として、冷静・客観的な視点で薬剤を評価できるようになりたいと思います。
作用機序や特徴を理解することが客観的な評価を邪魔してしまうことがあるので注意したいと思いました。
今回のブルーレターをさらなる教訓に、医薬品の副作用とその頻度について、より具体的なイメージを持てるように心がけていきたいと思います。