平成31年2月20日、厚労省の中医協・総会で新規医薬品の薬価が決定しました。
同年2月25日に告示され、2月26日に薬価収載されました。
今回に薬価収載されたのは13製品です。
また、再生医療等製品として脊髄損傷治療に用いるステミラック注の薬価も収載されています。
ステミラック注の薬価は約1,500万円です・・・!!
参考資料
今回参考にした資料です。
- 中央社会保険医療協議会 総会(第409回)議事次第
- 新医薬品一覧表(平成31年2月26日収載予定)中医協 総-1-1 31.2.20
- 再生医療等製品の保険償還価格の算定について(中医協 総-2 31.2.20)
- 使用薬剤の薬価(薬価基準)の一部改正等について 保医発0225第9号 平成31年2月25日
新たに薬価収載された医薬品
新規に薬価収載された医薬品13製品についてまとめます。
新規有効成分を含む新医薬品
まずは新規有効成分を含有する医薬品として承認され、薬価収載が決定した医薬品についてまとめます。
今回の薬価収載では5品目が該当します。
セリンクロ錠
平成31年3月5日発売
新発売(薬価基準収載)のご案内
セリンクロ錠 添付文書
セリンクロ錠 インタビューフォーム
- 医薬品名と薬価
- セリンクロ錠10mg:296.40円/錠
- 成分名:ナルメフェン塩酸塩水和物
- 申請者:大塚製薬
- 効能・効果:アルコール依存症患者における飲酒量の低減
- 用法・用量:通常、成人にはナルメフェン塩酸塩として1回10mgを飲酒の1~2時間前に経口投与する。ただし、1日1回までとする。なお、症状により適宜増量することができるが、1日量は20mgを超えないこと。
- 1日薬価:296.40円
- 加算等:新薬創出等加算
日本初の飲酒量低減薬です。
μオピオイド受容体とδオピオイド受容体に対しては拮抗薬として作用し、κオピオイド受容体に対しては部分的作動薬(パーシャルアゴニスト)として作用することで、アルコール依存症で見られる飲酒時の過剰な多幸感と嫌悪感を低減することで効果を発揮します。
詳しくは過去記事にまとめています。
断酒補助薬であるレグテクト錠(薬価:49.40円/錠、1日薬価:296.40円)と同じ1日薬価となっていますね。
選択的オピオイド受容体調節作用という新規作用機序を有するため新薬創出等加算の対象にもなっています。
セリンクロ処方時の留意事項
使用薬剤の薬価(薬価基準)の一部改正等について(保医発0225第9号 平成31年2月25日)
2 薬価基準の一部改正に伴う留意事項について
(1)セリンクロ錠10mg
- 本製剤の効能・効果に関連する使用上の注意において「アルコール依存症治療の主体は心理社会的治療であることから、服薬遵守及び飲酒量の低減を目的とした心理社会的治療と併用すること。」とされているので、本製剤の薬剤料については、以下のすべての要件を満たした場合に限り算定できること。
- ア アルコール依存症の患者に対して、アルコール依存症に係る適切な研修を修了した医師が、アルコール依存症に係る適切な研修を修了した看護師、精神保健福祉士、公認心理師等と協力し、家族等と協議の上、詳細な診療計画を作成し、患者に対して説明を行うこと
- イ 必要に応じて患者の受入が可能な精神科以外の診療科を有する医療体制との連携体制があること
- ウ 心理社会的治療については、アルコール依存症に係る適切な研修を修了した医師によって行い、その要点及び診療時間を診療録に記載すること
なお、少なくとも本剤の初回投与時においては、30分を超えて当該治療を行うこと(本剤の初回投与までの診療時において30分を超えて当該治療を行った場合を除く)- エ ア及びウに定めるアルコール依存症に係る適切な研修は、「診療報酬の算定方法」(平成20年厚生労働省告示第59号)別表第一医科診療報酬点数表(以下「医科点数表」という。)区分番号「A231-3」重度アルコール依存症入院医療管理加算の算定にあたり医師等に求められる研修に準じたものであること
- 本製剤の効能・効果に関連する使用上の注意において「アルコール依存症の診断は、国際疾病分類等の適切な診断基準に基づき慎重に実施し、基準を満たす場合にのみ投与すること。」、「アルコール依存症に伴う精神・身体症状及び患者の意思を総合的に勘案し、断酒ではなく飲酒量低減を治療目標とすることが適切と判断された患者に対して本剤を投与すること。」及び「飲酒量低減治療の意思のある患者にのみ使用すること。」とされているので、投与に当たっては十分留意すること。
- 本製剤の用法・用量に関連する使用上の注意において「本剤の投与継続及び治療目標の見直しの要否について定期的に検討し、漫然と投与しないこと。」とされているので、3ヵ月ごとを目安に治療の評価を行うこと。
「重度アルコール依存症入院医療管理加算の算定にあたり医師等に求められる研修に準じたもの」を修了した医師が処方しないと薬剤料は算定不可というかなり厳しいハードルが課せられています。
これも詳しくは過去記事でまとめています。
タリージェ錠
平成31年4月15日発売
タリージェ錠2.5mg・錠5mg・錠10mg・錠15mg 新発売のご案内
タリージェ錠 添付文書
タリージェ錠 インタビューフォーム
- 医薬品名と薬価
- タリージェ錠2.5mg:78.0円/錠
- タリージェ錠5mg:107.70円/錠
- タリージェ錠10mg:148.70円/錠
- タリージェ錠15mg:179.60円/錠
- 成分名ミロガバリンベシル酸塩:
- 申請者:第一三共
- 効能・効果:末梢性神経障害性疼痛
- 用法・用量:通常、成人には、ミロガバリンとして初期用量1回5mgを1日2回経口投与し、その後1回用量として5mgずつ1週間以上の間隔をあけて漸増し、1回15mgを1日2回経口投与する。なお、年齢、症状により1回10mgから15mgの範囲で適宜増減し、1日2回投与する。
- 1日薬価:446.10円
と同じ電位依存性カルシウムチャネルα2δ(アルファ2デルタ)リガンドで、効果の持続時間の長さや副作用の少なさが期待される薬剤ですが、適応が末梢性神経障害性疼痛のみになっています。
(リリカは神経障害性疼痛、線維筋痛症に伴う疼痛)
詳しくは過去記事にまとめています。
同様の作用機序を有するリリカOD錠75mg(薬価:111.50円/錠、1日薬価:446.00円)の1日薬価を元にタリージェ錠10mgの薬価を決定、そこからリリカOD錠の規格間比を用いて各規格の薬価が決定されたようです。
ミネブロ錠
2019年5月13日発売
ミネブロ錠1.25mg・錠2.5mg・錠5mg 新発売のご案内
ミネブロ錠 添付文書
ミネブロ錠 インタビューフォーム
- 医薬品名と薬価
- ミネブロ錠1.25mg:46.90円/錠
- ミネブロ錠2.5mg:89.90円/錠
- ミネブロ錠5mg:134.90円/錠
- 成分名:エサキセレノン
- 申請者:第一三共
- 効能・効果:高血圧症
- 用法・用量:通常、成人にはエサキセレノンとして2.5mgを1日1回経口投与する。なお、効果不十分な場合は、5mgまで増量することができる。
- 1日薬価:89.90円
- 加算等:
- 有用性加算(Ⅱ)(A=5%)
- 新薬創出等加算
選択的ミネラルコルチコイド受容体拮抗薬に分類されるミネブロはセララと同じく鉱質コルチコイド受容体(アルドステロン受容体)を遮断することでレニン-アンジオテンシン・アルドステロン系(RAAS*1)の最終産物であるアルドステロンの働きを阻害し、降圧作用を発揮します。
詳しくは過去記事にまとめています。
同様の作用機序を有するセララ錠50mg(薬価:85.60円/錠、1日薬価:85.60円)の薬価を元にミネブロ錠2.5mgの薬価が決定されていますが、セララでは禁忌となっている「中等度腎機能障害合併高血圧症患者」、「アルブミン尿を有する糖尿病合併高血圧患者」に対しても治験を実施し、投与可能としていることから有用性加算(Ⅱ)(A=5%)が適用されています。
デムサーカプセル
平成31年2月26日発売
チロシン水酸化酵素阻害剤「デムサー®カプセル250mg」新発売のお知らせ
デムサーカプセル 添付文書
デムサーカプセル インタビューフォーム
- 医薬品名と薬価
- デムサーカプセル250mg:5,853.50円/カプセル
- 成分名:メチロシン
- 申請者:小野薬品工業
- 効能・効果:褐色細胞腫のカテコールアミン分泌過剰状態の改善
- 用法・用量:通常、成人及び12歳以上の小児にはメチロシンとして1日500mgから経口投与を開始する。
効果不十分な場合は、経過を十分に観察しながら3日間以上の間隔をおいて1日250mg又は500mgずつ漸増し、患者の尿中カテコールアミン量及び症状の十分な観察のもと、適宜増減する。
ただし、1日最高用量は4,000mg、1回最高用量は1,000mg、投与間隔は4時間以上とし、1日500mgは1日2回、1日750mgは1日3回、1日1,000mg以上は1日4回に分割する。 - 加算等:
- 有用性加算(Ⅱ)(A=5%)
- 市場性加算(Ⅰ)(A=10%)
- 新薬創出等加算
有効成分であるメチロシンはチロシン水酸化酵素を阻害することでカテコールアミン(カテコラミン)の生合成を抑制します。
褐色細胞腫によって引き起こされるカテコールアミンの過剰産生を抑制することを可能とする新規作用機序の薬剤で、カテコラミン過剰症による症状を緩和し、生活の質(QOL*2)を改善することが期待されます。
類似の薬理作用・化学構造を持つ医薬品が存在しないため、原価計算方式で薬価が検討されています。また、新規作用機序を有することから有用性加算(Ⅱ)(A=5%)が適用され、希少疾患用医薬品の指定を受けていることから市場性加算(Ⅰ)(A=10%)がて適用されています。
デムサーカプセル処方時の留意事項
2 薬価基準の一部改正に伴う留意事項について
(2)デムサーカプセル250mg
本製剤の効能・効果に関連する使用上の注意において、「既存の交感神経受容体遮断薬による治療では十分な治療効果が得られていない」及び「外科手術前の処置、外科手術が適応とならない患者の管理、悪性褐色細胞腫患者の慢性的治療を目的とする」のいずれも満たす場合に使用することとされているので、使用に当たっては 十分留意すること。
引用元:使用薬剤の薬価(薬価基準)の一部改正等について(保医発0225第9号 平成31年2月25日)
つまりは第一選択にはならないので注意ということですね。
レルミナ錠
平成31年3月1日発売
GnRHアンタゴニスト「レルミナ錠40mg」新発売のお知らせ
レルミナ錠 添付文書
- 医薬品名と薬価
- レルミナ錠40mg:905.70円/錠
- 成分名:レルゴリクス
- 申請者:武田薬品工業
- 効能・効果:子宮筋腫に基づく諸症状(過多月経、下腹痛、腰痛、貧血)の改善
- 用法・用量:通常、成人にはレルゴリクスとして40mgを1日1回食前に経口投与する。なお、初回投与は月経周期1~5日目に行う。
- 1日薬価:905.70円
下垂体の性腺刺激ホルモン放出ホルモン(GnRH*3)受容体を阻害することで、下垂体からの黄体形成ホルモン(LH*4)、卵胞刺激ホルモン(FSH*5)の分泌を阻害します。
その結果、卵巣からの性ホルモン(エストロゲン、プロゲステロン)の放出が抑制され、子宮筋腫の主な症状である過多月経、下腹痛、腰痛などの症状を改善することは期待されています。
スプレキュアMP皮下注用1.8(薬価:27,448円/筒、1日薬価:960.40円)の1日薬価を元に類似薬効比較方式(I)で薬価が決定したようです。
ビジンプロ錠
平成31年3月1日発売
EGFR遺伝子変異陽性非小細胞肺がん治療薬「ビジンプロ®錠15mg、同45mg」(一般名:ダコミチニブ水和物)本日発売~EGFR肺がんに新たな一次治療の選択肢、長期生存を目指して~
ビジンプロ錠 添付文書
ビジンプロ錠 インタビューフォーム
- 医薬品名と薬価
- ビジンプロ錠15mg:3,850.60円/錠
- ビジンプロ錠45mg:10,748.00円/錠
- 成分名:ダコミチニブ水和物
- 申請者:ファイザー
- 効能・効果:EGFR遺伝子変異陽性の手術不能または再発非小細胞肺がん
- 用法・用量:通常、成人にはダコミチニブとして1日1回45mgを経口投与する。なお、患者の状態により適宜減量する。
- 1日薬価:10,748.00円
有効成分のダコミチニブは国内5番目のEGFR*6チロシンキナーゼ阻害薬です。
その中でも、第二世代EGFR*7チロシンキナーゼ阻害薬に分類されます。
各世代ごとの薬剤をまとめると以下のようになります。
- 第1世代:ゲフィチニブ(イレッサ®︎)、エルロチニブ(タルセバ®︎)
- 第2世代:アファチニブ(ジオトリフ®︎)、ダコミチニブ(ビジンプロ®︎)
- 第3世代:オシメルチニブ(タグリッソ®︎)
すでに第三世代EGFRチロシンキナーゼ阻害薬であるオシメルチニブ(タグリッソ®︎)が発売されているのにこのタイミングで第二世代?と思ってしまいますが、国内での開発段階で時間がかかったのでしょうか?
ちなみに、世代ごとの違いは以下の通りです。
- 第一世代:EGFRのみに作用
- 第二世代:EGFR(ErbB1)のみでなくErbBファミリーすべてに作用
- 第三世代:EGFRチロシンキナーゼ阻害薬に耐性を持つがん細胞にも有効
以前はタグリッソは第一選択として使用できなかったのですが、昨年8月(平成30年8月21日付)に一変承認を受け、第一選択として使用することが可能となっています。
ダコミチニブの副作用の多さを考えると使い所はどうなるんでしょうか?(詳しくないのであまりよくわかりません)
同じ第2世代EGFRチロシンキナーゼ阻害薬であるジオトリフ錠20mg(薬価:5,574.70円、1日薬価:11,149.40円の1日薬価を元に類似薬効比較方式(II)で薬価が決定したようです。
ビラフトビカプセル
平成31年2月26日発売
BRAF阻害剤「ビラフトビ®カプセル50mg」およびMEK阻害剤「メクトビ®錠15mg」新発売のお知らせ
ビラフトビカプセル 添付文書
ビラフトビカプセル インタビューフォーム
- 医薬品名と薬価
- ビラフトビカプセル50mg:3,180.70円/カプセル
- 成分名:エンコラフェニブ
- 申請者:小野薬品
- 効能・効果:BRAF遺伝子変異を有する根治切除不能な悪性黒色腫
- 用法・用量:ビニメチニブとの併用において、通常、成人にはエンコラフェニブとして450mgを1日1回経口投与する。なお、患者の状態により適宜減量する。
- 1日薬価:28,626.30円
- 加算等:新薬創出等加算
ビラフトビカプセルはMEK阻害薬であるメクトビ錠と併用する薬剤です。
有効成分であるエンコラフェニブはBRAF*8阻害剤です。
悪性黒色腫のうち20〜30%で、細胞増殖経路である(MAPK*9経路上で重要な役割を果たすBRAF V600遺伝子に変異が生じていると言われています。
変異型BRAFがキナーゼ活性が高くなっており、シグナル伝達の有無にかかわらず、下流のMEKやERKを活性化し、細胞の異常増殖や生存助長を促してしまいます。
エンコラフェニブは、ヒトBRAF V600Eのキナーゼ活性を阻害、BRAFの下流に存在するシグナル伝達分子であるMEKとERKのリン酸化を阻害することで、MAPKシグナル伝達が過剰に進んでしまうのを抑え、がん細胞の過剰増殖を抑えます。
同じBRAF阻害薬であるタフィンラーカプセル75mg(薬価:7,156.50円/カプセル、1日薬価:28,626.00円)の1日薬価を元に類似薬効比較方式(I)で薬価が決定しています。
希少疾患用医薬品として指定されているため新薬創出等加算の対象です。
ビラフトビカプセル処方時の留意事項
2 薬価基準の一部改正に伴う留意事項について
(3)ビラフトビカプセル50mg
本製剤の効能・効果に関連する使用上の注意において、「十分な経験を有する病理医又は検査施設における検査により、BRAF遺伝子変異が確認された患者に投与すること。」とされているので、BRAF遺伝子変異を確認した検査の実施年月日を診療報酬明細書の摘要欄に記入すること。
なお、当該検査を実施した月のみ実施年月日を記載すること。ただし、本剤の初回投与に当たっては、必ず実施年月日を記載すること。
引用元:使用薬剤の薬価(薬価基準)の一部改正等について(保医発0225第9号 平成31年2月25日)
初回の処方では「BRAF遺伝子変異を確認した検査の実施年月日」をレセプトに記載しなければいけません。
メクトビ錠と共通の留意事項です。
メクトビ錠
平成31年2月26日発売
BRAF阻害剤「ビラフトビ®カプセル50mg」およびMEK阻害剤「メクトビ®錠15mg」新発売のお知らせ
メクトビ錠 添付文書
メクトビ錠 インタビューフォーム
- 医薬品名と薬価
- メクトビ錠15mg:4,836.80円/錠
- 成分名:ビニメチニブ
- 申請者:小野薬品工業
- 効能・効果:BRAF遺伝子変異を有する根治切除不能な悪性黒色腫
- 用法・用量:エンコラフェニブとの併用において、通常、成人にはビニメチニブとして1回45mgを1日2回経口投与する。なお、患者の状態により適宜減量する。
- 1日薬価:29,020.80円
- 加算等:新薬創出等加算
メクトビ錠はBRAF阻害薬であるビラフトビカプセルと併用する薬剤です。
有効成分であるビニメチニブはMEK*10阻害薬です。
MAPK経路の下流に存在するMEK1/MEK2の活性化とそのキナーゼ活性を阻害し、さらにその下流に存在するERKのリン酸化を阻害ことで、MAPKシグナル伝達が過剰に進んでしまうのを抑え、がん細胞の過剰増殖を抑えます。
同じMEK阻害薬であるメキニスト錠2mg(薬価29,021.00円/錠、1日薬価:29,021.00円)の1日薬価を元に類似薬効比較方式(I)で薬価が決定しています。
希少疾患用医薬品として指定されているため新薬創出等加算の対象です。
メクトビ錠処方時の留意事項
2 薬価基準の一部改正に伴う留意事項について
(4)メクトビ錠15mg
本製剤の効能・効果に関連する使用上の注意において、「十分な経験を有する病理医又は検査施設における検査により、BRAF 遺伝子変異が確認された患者に投与すること。」とされているので、BRAF遺伝子変異を確認した検査の実施年月日を診療報酬明細書の摘要欄に記入すること。
なお、当該検査を実施した月のみ実施年月日を記載すること。ただし、本剤の初回投与に当たっては、必ず実施年月日を記載すること。
引用元:使用薬剤の薬価(薬価基準)の一部改正等について(保医発0225第9号 平成31年2月25日)
当然ですがビラフトビカプセルと同じですね。
初回の処方では「BRAF遺伝子変異を確認した検査の実施年月日」をレセプトに記載しなければいけません。
エプクルーサ配合錠
平成31年2月26日発売
「エプクルーサ®配合錠」新発売
エプクルーサ配合錠 添付文書
エプクルーサ配合錠 インタビューフォーム
- 医薬品名と薬価
- エプクルーサ配合錠:60,154.50円/錠
- 成分名:ソホスブビル/ベルパタスビル
- 申請者:ギリアド・サイエンシズ
- 効能・効果:
- 前治療歴を有するC型慢性肝炎又はC型代償性肝硬変におけるウイルス血症の改善
リバビリンとの併用において、通常、成人には、1日1回1錠(ソホスブビルとして400mg及びベルパタスビルとして100mg)を24週間経口投与する。 - C型非代償性肝硬変におけるウイルス血症の改善
通常、成人には、1日1回1錠(ソホスブビルとして400mg及びベルパタスビルとして100mg)を12週間経口投与する。
- 前治療歴を有するC型慢性肝炎
- C型代償性肝硬変におけるウイルス血症の改善
- C型非代償性肝硬変におけるウイルス血症の改善
- 前治療歴を有するC型慢性肝炎又はC型代償性肝硬変におけるウイルス血症の改善
- 用法・用量:
- 1日薬価:60,154.50円
- 加算等:
- 有用性加算(Ⅱ)(A=10%)
- 新薬創出等加算
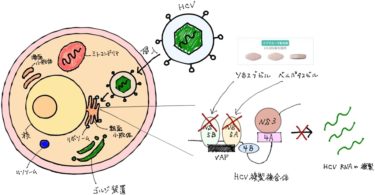
C型肝炎ウイルス(HCV*11)に対するIFN*12フリー、直接作用型抗ウイルス療法(DAAs*13)治療薬です。
すでにソバルディやハーボニーとして発売されているソホスブビルはNS5B阻害薬、新規有効成分であるNS5A複製複合体阻害薬ベルパタスビルの配合剤です。
これまで肝移植が主な治療法だったC型非代償性肝硬変に対して効果を発揮する初のDAAsです。
まら、既存のDAAsで不成功だったケースにも使用できる薬剤です。
詳しくは過去記事にまとめています。
同じくソホスブビルを含むHCV治療薬ハーボニー配合錠(薬価:54,685.90円/錠、1日薬価:54,685.90円)の1日薬価を元に類似薬効比較方式(I)で薬価を計算、C型非代償性肝硬変に対する初の薬剤であることから有用性加算(Ⅱ)(A=10%)が適用されています。
加算適用のため、新薬創出等加算に該当します。
エプクルーサ配合錠処方時の留意事項
2 薬価基準の一部改正に伴う留意事項について
(5)エプクルーサ配合錠
本製剤の効能・効果は「前治療歴を有するC型慢性肝炎又はC型代償性肝硬変におけるウイルス血症の改善」及び「C型非代償性肝硬変におけるウイルス血症の改善」であることから、以下の患者には使用しないこと。
- 前治療歴のないC型慢性肝炎ウイルス感染者又はC型代償性肝硬変患者
- 慢性肝炎を発症していないC型肝炎ウイルス感染者
まあ、当然ですね。
イベニティ皮下注シリンジ
平成31年3月4日発売
イベニティ皮下注105mgシリンジ 新発売のご案内
イベニティ皮下注 添付文書
イベニティ皮下注 インタビューフォーム
- 医薬品名と薬価
- イベニティ皮下注105mgシリンジ:24,720.00円/筒
- 成分名:ロモソズマブ(遺伝子組換え)
- 申請者:アステラス・アムジェン・バイオファーマ
- 効能・効果:骨折の危険性の高い骨粗鬆症
- 用法・用量:通常、成人にはロモソズマブ(遺伝子組換え)として210mgを1ヵ月に1回、12ヵ月皮下投与する。
- 1日薬価:1,625円
- 加算等:
- 有用性加算(Ⅱ)(A=5%)
- 新薬創出等加算
有効成分のロモソズマブはヒト抗スクレロスチンモノクローナル抗体です。
骨細胞で産生されるスクレロスチンは骨芽細胞のWnt‒βカテニンシグナル伝達を阻害することで骨形成を抑制する糖タンパク質です。
ロモソズマブがスクレロスチンに結合してWnt(ウィント)シグナル伝達が進むことによって、骨形成は促進、骨吸収は抑制されます。
現在使用されている骨形成促進薬と比較した場合、半分程度の投与期間で骨折抑制効果が認められます。
フォルテオ皮下注キット600μg(薬価:43,334円/キット、1日薬価:1,548円)の1日薬価を元に薬価を計算、有用性加算(Ⅱ)(A=5%)が適用されています。
加算適用のため、新薬創出等加算に該当します。
効能・効果の「骨折の危険性の高い骨粗鬆症」の基準について明確化が求められ、留意事項が出されています。
イベニティ皮下注処方時の留意事項
2 薬価基準の一部改正に伴う留意事項について
(6)イベニティ皮下注105mgシリンジ
- 本製剤の効能・効果に関連する使用上の注意に、「本剤の適用にあたっては、低骨密度、既存骨折、加齢、大腿骨頸部骨折の家族歴等の骨折の危険因子を有する患者を対象とすること。」と記載されているので、使用に当たっては十分留意すること。
- 本製剤の用法・用量に「1ヵ月に1回、12ヵ月皮下投与する」とされ、これに関連する使用上の注意に、「本剤の骨折抑制効果は12ヵ月の投与で検証されており、12ヵ月を超えた投与では検討されていない。また、本剤投与終了後に原則として適切な骨粗鬆症薬による治療を継続すること。」と記載されているので、使用に当たっては十分留意すること。
- 本製剤を12ヵ月投与した後に本製剤を再投与する場合、再投与開始に当たっては、次の事項を診療報酬明細書の摘要欄に記載すること。
- ア 骨折の危険性が高いと判断した理由
- イ 本製剤を再投与するまでに投与した骨粗鬆症治療薬の品名
「低骨密度、既存骨折、加齢、大腿骨頸部骨折の家族歴等の骨折の危険因子を有する患者」は特に具体的に明記されていません。
基本的に12ヶ月の使用になり、再投与についてはレセプトへの記載が必要となります。
ザバクサ配合点滴静注用
ザバクサ配合点滴静注用 添付文書ザバクサ配合点滴静注用 インタビューフォーム
- 医薬品名と薬価
- ザバクサ配合点滴静注用:6,335.00円/瓶
- 成分名:セフトロザン硫酸塩/タゾバクタムナトリウム
- 申請者:MSD
- 効能・効果:
- 〈適応菌種〉
本剤に感性のレンサ球菌属、大腸菌、シトロバクター属、クレブシエラ属、エンテロバクター属、プロテウス属、緑膿菌 - 〈適応症〉
膀胱炎、腎盂腎炎、腹膜炎、腹腔内膿瘍、胆嚢炎、肝膿瘍
- 〈適応菌種〉
- 用法・用量:通常、成人には1回1.5g(タゾバクタムとして0.5g/セフトロザンとして1g)を1日3回60分かけて点滴静注する。
なお、腹膜炎、腹腔内膿瘍、胆嚢炎、肝膿瘍に対しては、メトロニダゾール注射液と併用すること。
新規セフェム薬であるセフトロザン硫酸塩1.0gにβラクタマーゼ阻害剤であるタゾバクタムナトリウム0.5gを配合した注射用抗菌薬です。
セフトロザンは第四世代セファロスポリンに分類されます。
基礎疾患等に起因する複雑性尿路感染症、複雑性腹腔内感染症に対する薬剤として期待されています。
ゾバクタム/ピペラ シリン水和物(ゾシン、タゾピペ)以降、類似の薬剤が登場していないため、原価計算方式で薬価が決定していますね。
既存の有効成分を用いた医薬品
ビムパットの新剤形が2種類登場しています。
ビムパットドライシロップ
平成31年3月11日発売
ビムパットドライシロップ10%・点滴静注200mg 新発売のご案内
ビムパットドライシロップ 添付文書
ビムパットドライシロップ インタビューフォーム
- 医薬品名と薬価
- ビムパットドライシロップ10%:386.20円/g
- 成分名:ラコサミド
- 申請者:ユーシービージャパン
- 効能・効果:てんかん患者の部分発作(二次性全般化発作を含む)
- 用法・用量:
- 成人
通常、成人にはラコサミドとして1日100mg(ドライシロップとして1g)より投与を開始し、その後1週間以上の間隔をあけて増量し、維持用量を1日200mg(ドライシロップとして2g)とするが、いずれも1日2回に分けて用時懸濁して経口投与する。なお、症状により1日400mg(ドライシロップとして4g)を超えない範囲で適宜増減するが、増量は1週間以上の間隔をあけて1日用量として100mg(ドライシロップとして1g)以下ずつ行うこと。 - 小児
通常、4歳以上の小児にはラコサミドとして1日2mg/kg(ドライシロップとして20mg/kg)より投与を開始し、その後1週間以上の間隔をあけて1日用量として2mg/kg(ドライシロップとして20mg/kg)ずつ増量し、維持用量を体重30kg未満の小児には1日6mg/kg(ドライシロップとして60mg/kg)、体重30kg以上50kg未満の小児には1日4mg/kg(ドライシロップとして40mg/kg)とする。いずれも1日2回に分けて用時懸濁して経口投与する。なお、症状により体重30kg未満の小児には1日12mg/kg(ドライシロップとして120mg/kg)、体重30kg以上50kg未満の小児には1日8mg/kg(ドライシロップとして80mg/kg)を超えない範囲で適宜増減するが、増量は1週間以上の間隔をあけて1日用量として2mg/kg(ドライシロップとして20mg/kg)以下ずつ行うこと。ただし、体重50kg以上の小児では、成人と同じ用法・用量を用いること。
- 成人
- 1日薬価:772.40円
- 加算等:新薬創出等加算
ビムパッド錠の剤形追加ということで、ビムパット錠100mg(薬価:351.30円/錠、1日薬価:702.60円)を元にした類似薬効比較方式(I)で薬価が決定しています。(イーケプラ錠500mgとイーケプラドライシロップ50%の剤形間比を利用)
新薬創出等加算を受けている製剤の剤形追加のため新薬創出等加算に該当しています。
ビムパット点滴静注
平成31年3月25日発売
ビムパットドライシロップ10%・点滴静注200mg 新発売のご案内
ビムパット点滴静注 添付文書
ビムパット点滴静注 インタビューフォーム
- 医薬品名と薬価
- ビムパット点滴静注200mg:4,252円/瓶
- 成分名:ラコサミド
- 申請者:ユーシービージャパン
- 効能・効果:一時的に経口投与ができない患者におけるてんかんの部分発作(二次性全般化発作を含む)の治療に対するラコサミド経口製剤の代替療法
- 用法・用量:
- 成人
通常、成人にはラコサミドとして1日100mgより投与を開始し、その後1週間以上の間隔をあけて増量し、維持用量を1日200mgとするが、いずれも1日2回に分け、1回量を30分から60分かけて点滴静脈内投与する。
成人では1日最高投与量は400mgを超えないこととし、増量は1週間以上の間隔をあけて1日用量として100mg以下ずつ行う。 - 小児
通常、4歳以上の小児にはラコサミドとして1日2mg/kgより投与を開始し、その後1週間以上の間隔をあけて1日用量として2mg/kgずつ増量し、維持用量を体重30kg未満の小児には1日6mg/kg、体重30kg以上50kg未満の小児には1日4mg/kgとする。いずれも1日2回に分け、1回量を30分から60分かけて点滴静脈内投与する。ただし、体重50kg以上の小児では、成人と同じ用法・用量を用いること。
4歳以上の小児のうち体重30kg未満の小児では1日12mg/kg、体重30kg以上50kg未満の小児では1日8mg/kgを超えないこととし、増量は1週間以上の間隔をあけて1日用量として2mg/kg以下ずつ行う。ただし、体重50kg以上の小児では、成人と同じ1日最高投与量及び増量方法とすること。
- 成人
- 1日薬価:4,252円
- 加算等:新薬創出等加算
イーケプラ点滴静注500mg(薬価:1,972円/瓶、1日薬価:3,944円)を元に類似薬効比較方式(I)で薬価が決定しています。
新薬創出等加算を受けている製剤の剤形追加のため新薬創出等加算に該当しています。
再生医療等製品
再生医療等製品としては3品目となるステミラックが薬価収載されています。
ステミラック注
- 医薬品名と薬価
- ステミラック注:14,957,755円/回
- 成分名:ヒト(自己)骨髄由来間葉系幹細胞
- 申請者:ニプロ
- 効能・効果:脊髄損傷に伴う神経症候及び機能障害の改善。ただし、外傷性脊髄損傷で、ASIA機能障害尺度がA、B又はCの患者に限る。
- 用法・用量:骨髄液の採取は、患者の全身状態等を考慮した上で、脊髄損傷受傷後31日以内を目安に実施する。また、製品が製造され次第、可能な限り速やかに投与する。
- 本品の原料採取時に行う事項
- 患者から末梢血を採取する。採取した末梢血は採血キットの構成体である容器(ニプロセルトリー 血清用)に入れ密封する。末梢血の入った容器は製造販売業者の指定する施設へ運搬する。
- 患者から骨髄液を採取する。採取した骨髄液は、骨髄採取キットの構成体である骨髄希釈液DMEMとともに容器(ニプロセルトリー 骨髄用)に入れ、混合して密封する。骨髄液の入った容器は製造販売業者の指定する施設へ運搬する。
- 本品を患者に適用する際に行う事項
自己骨髄間葉系幹細胞として1回0.5×108~2.0×108個(最大投与量は体重1kgあたり3.34×106個)を、生理食塩液で3倍以上に希釈しながら、本品の流量0.7~1.0 mL/分を目安に点滴静注する。
- 本品の原料採取時に行う事項
資料を見るとどんな治療方法が掲載されています。
使用目的
本品は、患者本人から採取した骨髄液中の間葉系幹細胞を体外で培養して増殖させた後、 凍結保存バッグに充填して凍結保存したものを主構成体とする再生医療等製品である。
脊髄損傷に伴う神経症候及び機能障害の改善を目的とし、医薬品と同様に薬理的な作用 による治療効果を期待して、点滴で静脈内に投与される。
引用元:再生医療等製品の保険償還価格の算定について(中医協 総-2 31.2.20)
なんと驚きの薬価1495万円・・・。およそせんごひゃくまんえん・・・。
すごい時代になりましたねえ・・・。
ステミラック注処方時の留意事項
2 薬価基準の一部改正に伴う留意事項について
(7)ステミラック注
- 本製品の原料採取に伴い、患者から末梢血を採取した場合は、医科点数表区分番号「K920」輸血の3(自己血貯血)のイ(6歳以上の患者の場合(200mLごとに) の(1)(液状保存の場合)を算定できるものであること。
なお、本算定は原則として4回までとする。- 本製品の原料採取に伴い、患者から骨髄液を採取した場合は、医科点数表区分番号「K921」造血幹細胞採取(一連につき)の1(骨髄採取)のロ(自家移植の場合)を算定できるものであること。
幹細胞を末梢血から作るか骨髄液から作るかで算定できる内容が変わるってことですね。
雑感
薬価収載即発売開始は以下の4製品ですね。
- デムサー
- ビラフト
- メクトビ
- エプクルーサ
デムサー、ビラフト、メクトビと3製品を一気に出す小野薬品はすごいですね。
第一三共のタリージェは4月、ミネブロに至っては元号が変わった5月発売です。
第一三共エスファのユリーフAG(シロドシン錠「DSEP」)もそうですが、最近発売開始までに時間をかけすぎじゃないですかね?
そして驚きの薬価のステミラック注。
素晴らしい治療法だとは思いますが・・・医療費はどうなっちゃうんでしょうね?
*1:Renin-Angiotensin-Aldosterone System
*2:Quality Of Life
*3:GoNadotropin-releasing hormone
*4:Luteinizing Hormone
*5:Follicle Stimulating Hormone
*6:Epidermal Growth Factor Receptor
*7:Epidermal Growth Factor Receptor
*8:B-Raf(rapidly accelerated fibrosarcoma) kinase
*9:RAS/RAF/MEK/ERK
*10:Mitogen-activated Extracellular signal-regulated Kinase
*11:Hepatitis C Virus
*12:InterFeroN
*13:Direct Acting Antivirals