2022年12月23日、アルツハイマー型認知症治療剤 アリドネパッチ(ドネペジル)が承認されました。
多剤の経口服薬、嚥下困難や寝たきり患者のアドヒアランス向上、介護者等による患者への投薬管理を容易にすることを期待して、帝國製薬が開発し製造販売承認を取得、販売は興和が担います。
- 日本初のドネペジル経皮吸収型製剤「アリドネ®パッチ27.5mg/アリドネ®パッチ55mg」に関する製造販売承認取得のお知らせ(帝國製薬)
- 日本初のドネペジル経皮吸収型製剤「アリドネ®パッチ27.5mg/アリドネ®パッチ55mg」に関する製造販売承認取得のお知らせ(興和)
アリドネパッチは現時点では薬価収載されていませんが、2023年3月に収載される予定です。
アルツハイマー型認知症はAD(Alzheimer’s disease)またはATD(Alzheimer-Type Dementia)と略されますが、今回の記事ではADに統一したいと思います。
- 製品名(洋名):アリドネパッチ27.5mg/アリドネパッチ55mg(ALLYDONE Patches)
- 成分名:ドネペジル
- 製造販売元(販売元):帝國製薬(興和)
- 作用分類:経皮吸収型コリンエステラーゼ阻害薬
- 命名の由来:ALLYDONE の”Ally”(仏語読み)は、味方・仲間・協力者・支持者を、“done”は有効成分名に由来する。
- 効能・効果:アルツハイマー型認知症における認知症症状の進行抑制
- 用法・用量:通常、軽度~中等度のアルツハイマー型認知症患者にはドネペジルとして、1日1回27.5mgを貼付する。高度のアルツハイマー型認知症患者にはドネペジルとして、27.5mgで4週間以上経過後、55mgに増量する。なお、症状により1日1回27.5mgに減量できる。
本剤は背部、上腕部、胸部のいずれかの正常で健康な皮膚に貼付し、24時間毎に貼り替える。 - 製造販売承認年月日:2022年12月23日
- 薬価基準収載年月日:未収載
ポイントだけ押さえたいかたは「3、まとめ」だけ読んでください。
アリドネの特性と承認背景
かつてはアルツハイマー病(AD)は治療を行うことが不可能な病といわれてきましたが、コリン仮説に基づいた研究が進んだ結果、コリンエステラーゼ阻害薬の開発に繋がり、薬物による対症療法を行うことが可能となりました。
アルツハイマー型認知症(AD)とは?
認知症と同様に記憶障害の症状を引き起こすものに「加齢に伴う記憶障害」がありますが、これは認知症とは異なります。
「認知症の記憶障害」と「加齢に伴う記憶障害」はしばしば混同されてしまうので注意が必要です。
一般的な違いとして、「加齢に伴う記憶障害」では物忘れの自覚があり、体験したことの一部分だけを忘れているだけで、日常生活には大きな影響はないことが多いですが、「認知症による記憶障害」では物忘れの自覚がなく、体験したこと自体を忘れてしまい、判断力の低下等日常生活にも大きな影響があることが多いです。
アルツハイマー型認知症(AD)は認知症の一つです。
認知症は以下のように4つに分類されます。
- アルツハイマー型認知症(AD)
- 血管性認知症
- レビー小体型認知症
- 前頭側頭型認知症
この中で最も多いのがADで、認知症の7割近くをADが占めているといわれています。
ADの原因については、様々な研究が行われていますが、現時点では、脳の神経に「アミロイドβ」や「タウタンパク質」が蓄積することで発症するという説が有力とされています。
これらのタンパク質が脳内に蓄積されていくことで神経細胞を萎縮させてしまい、その結果、ADが発症すると考えられています。
ADの症状と治療
ADの症状は大きく2つに分けられます。
- 中核症状(認知機能障害によるもの):記銘力障害、失見当識、判断力低下、失語、失行、失認など
- 周辺症状(行動および心理症状):興奮、叫声、不穏、焦燥、徘徊、社会文化的に不適切な行動、性的脱抑制、収集癖、暴言、つきまとい、不安、抑うつ、妄想、幻覚など
※BPSD(Behavioral and Psychological Symptoms of Dementia)と呼ばれる
中核症状に対してはアセチルコリンエステラーゼ阻害薬(AChE-I)やNMDA受容体拮抗薬が使用され、BPSDに対しては、陽性症状に対して抗精神病薬や気分安定薬(抗てんかん薬)が、陰性症状に対して脳循環・ 代謝改善薬や抗うつ薬が使用されます。
BPSDに対しては抑肝散等の漢方薬が使用されることもあります。
AD治療薬承認の歴史
認知症治療薬の歴史を振り返ってみます。
- 1993年:ChE阻害薬タクリンがFDAで承認(肝機能障害の副作用のため広くは使用されず)
- 1996年:アリセプト(ドネペジル塩酸塩)が米国で世界初のアルツハイマー型認知症治療薬として承認
- 1999年:アリセプト錠3mg/5mg(ドネペジル塩酸塩)が日本で承認
- 2001年:アリセプト(ドネペジル塩酸塩)に細粒0.5%の剤形追加
- 2004年:アリセプト(ドネペジル塩酸塩)にD錠(口腔内崩壊錠)の剤形追加
- 2007年:
アリセプト(ドネペジル塩酸塩)が「高度アルツハイマー型認知症」の適応を取得
アリセプト錠10mg/D錠10mg(ドネペジル塩酸塩)の規格が追加 - 2009年:アリセプト(ドネペジル塩酸塩)に内服ゼリーの剤形追加
- 2011年:
レミニール錠/OD錠/内用液(ガランタミン)が日本で承認
メマリー錠(メマンチン)が日本で承認
イクセロンパッチ/リバスタッチパッチ(リバスチグミン)が日本で承認
アリセプト(ドネペジル塩酸塩)の後発品が承認 - 2013年:アリセプト(ドネペジル塩酸塩)にドライシロップの剤形追加
- 2013年:メマリー(メマンチン)にOD錠の剤形追加
- 2014年:アリセプト(ドネペジル塩酸塩)が「レビー小体型認知症」の適応を取得
- 2015年:イクセロンパッチ/リバスタッチパッチ(リバスチグミン)に1ステップ漸増法の用法追加
- 2018年:メマリー(メマンチン)にドライシロップの剤形追加
- 2019年:イクセロンパッチ/リバスタッチパッチ(リバスチグミン)の基剤変更品が承認
- 2020年:
レミニール(ガランタミン)の後発品が承認
メマリー(メマンチン)の後発品が承認
イクセロン/リバスタッチ(リバスチグミン)の後発品が承認 - 2021年:
世界初のAD進行抑制薬アデュヘルム(アデュカヌマブ)がFDAで条件付き承認
日本でアデュヘルム(アデュカヌマブ)の承認見送り - 2022年:アリドネパッチ(ドネペジル)が日本で承認
- 2023年:FDAで抗アミロイドβプロトフィブリル抗体 レケンビ(レカネマブ)が迅速承認
アリドネパッチの作用機序
AD治療薬は大きく以下の3種類に分けられます。(アリドネパッチ(ドネペジル)はAChE-Iに該当します。)
- アセチルコリンエステラーゼ阻害薬(AChE-I):中核症状の抑制
- NMDA受容体拮抗薬:中核症状の抑制
- 抗アミロイドβ抗体:AD進行の抑制
大脳新皮質や海馬にはACh作動性神経経路が存在しますが、ADではアセチルコリン合成酵素であるコリンアセチルトランスフェラーゼ(ChAT:Choline AcetylTransferase)やアセチルコリンエステラーゼ(AChE:AcetylCholine Esterase)の活性が低下していることが報告されています。
このことを元に、ADの病態において脳内のコリン作動性神経の障害が重要であるという考えがコリン仮説です。
コリン仮説に基づき、脳内のアセチルコリン活性を高めることで、ADによる症状を緩和させることを目的に開発されたのがアセチルコリンエステラーゼ阻害剤(AChE-I:AcetylCholine Esterase Inhibitor)であるドネペジルです。
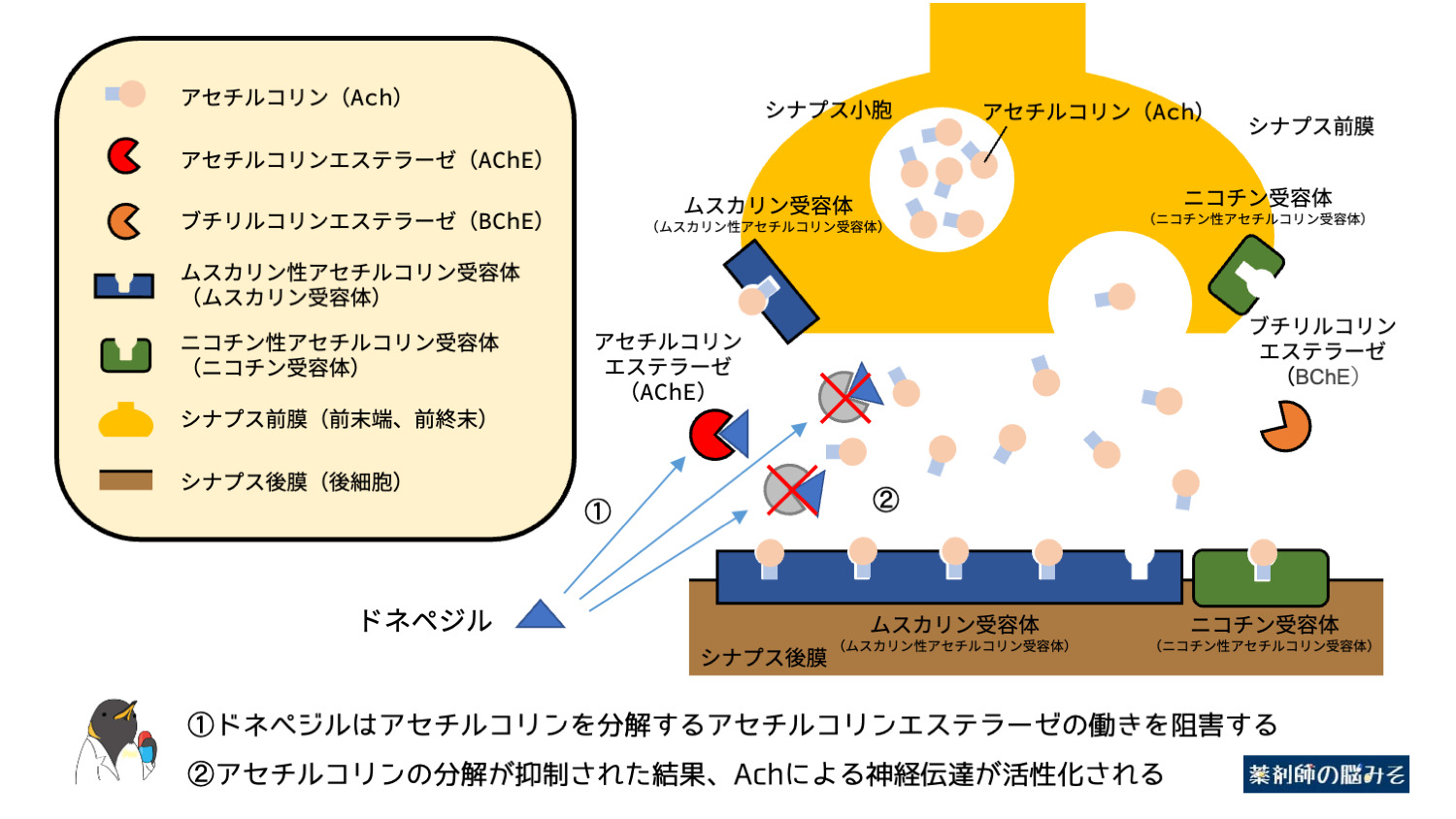
ドネペジルはシナプス間隙において効果を発揮します。
シナプス前膜から放出されたアセチルコリンを分解するAchEの働きを阻害し、シナプス間隙のAch濃度を高めることで、Achによる神経伝達を活性化させ、ADの症状を緩和すると考えられています。
他のAChE-I の作用
経皮吸収型ドネペジル製剤であるアリドネパッチには適応はありませんが、ドネペジル塩酸塩経口製剤であるアリセプトはレビー小体型認知症に対する適応も取得しています。
レビー小体型でもAD同様にAch神経の働きが低下していることが報告されており、それに基づく研究により効果が確認されています。
ADに対して使用されるAChE-Iにはそれぞれ特徴があります。
- ドネペジル:AChE阻害作用が強く(AChEに対する選択性が最も高い)、剤形が豊富
経口:錠剤/口腔内崩壊錠/細粒/ゼリー/ドライシロップ
貼付剤(アリドネパッチ) - ガランタミン(経口製剤のみ):AChE阻害作用に加えてニコチン性ACh受容体の作用を増強する効果(APL作用:アロステリック活性化リガンド作用)を持つ
- リバスチグミン(経皮吸収型製剤のみ):AChEとブチリルコリンエステラーゼ(BuChE)の両方を阻害する
これらの性質の違いによる効果を期待して各薬剤が選択されることも少なくありません。
アリドネの添付文書を読み解く!
それではアリドネの添付文書を読み解いていきます。
効能・効果(レビー小体型認知症に対する適応はない)
4. 効能又は効果
アルツハイマー型認知症における認知症症状の進行抑制
アリセプト(ドネペジル経口製剤)の効能・効果は「アルツハイマー型認知症及びレビー小体型認知症における認知症症状の進行抑制」となっていますが、承認時点でアリドネパッチはADに対する適応のみでレビー小体型認知症に対する適応はありません。
5. 効能又は効果に関連する注意
5.1 本剤がアルツハイマー型認知症の病態そのものの進行を抑制するという成績は得られていない。
5.2 アルツハイマー型認知症以外の認知症性疾患において本剤の有効性は確認されていない。
5.3 他の認知症性疾患との鑑別診断に留意すること。
5.4 本剤は、アルツハイマー型認知症と診断された患者にのみ使用すること。
注意点に関してはアリセプト(ドネペジル経口製剤)と同じです。
他の認知症治療薬との比較
認知症に対する適応を取得する他のコリンエステラーゼ阻害薬と適応を比較してみます。
表は左右にスクロール可能です
| 医薬品名 | (成分名) | アルツハイマー型認知症 | レビー小体型認知症 | ||||
|---|---|---|---|---|---|---|---|
| 軽度 | 中等度 | 重度 | |||||
| AChE阻害薬 | アリセプト | (ドネペジル塩酸塩経口製剤) | ◯ | ◯ | ◯ | ◯ | |
| レミニール | (ガランタミン臭化水素酸塩) | ◯ | ◯ | ー | ー | ||
| イクセロン/リバスタッチ | (リバスチグミン) | ◯ | ◯ | ー | ー | ||
| アリドネ (ドネペジル経皮吸収型製剤) | ◯ | ◯ | ◯ | ー | |||
| NMDA受容体阻害薬 | メマリー | (メマンチン) | ー | ◯ | ◯ | ー | |
用法・用量
6. 用法及び用量
通常、軽度~中等度のアルツハイマー型認知症患者にはドネペジルとして、1日1回27.5mgを貼付する。高度のアルツハイマー型認知症患者にはドネペジルとして、27.5mgで4週間以上経過後、55mgに増量する。なお、症状により1日1回27.5mgに減量できる。
本剤は背部、上腕部、胸部のいずれかの正常で健康な皮膚に貼付し、24時間毎に貼り替える。
アリドネパッチ27.5mgはドネペジル塩酸塩経口製剤5mgに相当します。
ドネペジル塩酸塩経口製剤は、消化器系副作用の発現を抑える目的で3mgで投与を開始し、1〜2週間後に5mgに増量しますが、アリドネにおいては内服3mgに相当する開始用量が存在しません。
ドネペジル塩酸塩経口製剤10mgに相当する55mgへの増量は27.5mgで4週間以上経過後になっています。
アリドネパッチのインタビューフォームには以下のように記載されています。
I. 概要に関する項目
1.開発の経緯
ドネペジル塩酸塩経口製剤1日1回投与と同等のドネペジルのAUC0-24hを得られる1日1回貼付の経皮吸収型製剤を開発した。
ということで、AUCはドネペジル塩酸塩経口製剤と同等にも関わらずローディングドーズを必要としない。
ドネペジル塩酸塩経口製剤の記載を踏まえると、アリドネパッチでは消化器症状が増えてしまいそうなのですが、臨床試験の結果を見る限りそうでもなさそうです。
これが経口投与と経皮吸収による差なのかは気になるところです。
7. 用法及び用量に関連する注意
7.1 55mg/日に増量する場合は、消化器系副作用に注意しながら使用すること。
7.2 他のコリンエステラーゼ阻害作用を有する同効薬(ドネペジル塩酸塩、リバスチグミン、ガランタミン)と併用しないこと。
7.3 医療従事者、家族などの管理のもとで使用すること。
7.1と7.3はドネペジル塩酸塩経口製剤にも記載されている内容です。(ただし、55mg→10mg)
7.2に関してはアリドネが貼付剤の形をとっていることから追加されたものと思われます。
貼付剤としての注意点
8. 重要な基本的注意
8.5 本剤の貼り替えの際、貼付している製剤を除去せずに新たな製剤を貼付すると過量投与となるおそれがあるため、貼り替えの際は先に貼付している製剤を除去したことを十分確認するよう患者及び介護者等に指導すること。
まあ、これは当然ですよね。他の貼付剤も同様です。
ただ、きちんと説明しないと、過去に剥がさずにどんどん貼ってしまったケースに遭遇したことがあります。
14. 適用上の注意
14.2 薬剤貼付部位に関する注意
14.2.1 本剤は、背部、上腕部又は胸部の正常で健康な皮膚で、清潔で乾燥した体毛が少ない、衣服を着用してもこすれにくい部位に貼付すること。
貼付部位:背部、上腕部、胸部
はイクセロンパッチ/リバスタッチパッチと同じですね。首から下、肘から上の、いわゆるホクナリン部位です。(そんなことは言わない)
正常で健康な皮膚で、清潔で乾燥した体毛が少ない、衣服を着用してもこすれにくい部位ってのも、まあ、意味はわかるんですが、なかなか難しいですよね。
14. 適用上の注意
14.3 薬剤貼付時の注意
14.3.1 原則、1回につき1枚のみ貼付すること。また、貼付24時間後に新しい製剤に貼り替えること。
14.3.2 本剤が剥がれた場合は、その時点で新しい製剤に貼り替え、予定していた次の貼り替え時間に改めて新しい製剤に貼り替えること。
14.3.3 貼付部位を外部熱(過度の直射日光、あんか、サウナ等のその他の熱源)に曝露させないこと。貼付部位の温度が上昇すると本剤からのドネペジルの吸収量が増加し、血中濃度が上昇するおそれがある。
14.3.4 包装袋は手で破り開封し、本剤を取り出すこと。
剥がれた場合は新しいものに貼り替えて、予定通りの貼付時間になったら再び貼り替えるという対応になっているので、単純に剥がれた分だけ薬剤がロスしていくことになりますね。
ちなみにこれが続いたため、早めに受診・処方箋発行ってなるのは保険適応上問題ないんですよね?(ないよね?)
貼付部位を温めると吸収が増加するので注意が必要です。
入浴時点での貼り替えが望ましいんでしょうけど、高齢者の場合、お風呂に入る時間に合わせて貼り替えというのは難しいケースがあるので、介護者等には事前にこのことを伝えておかないといけませんね。
14. 適用上の注意
14.4 薬剤貼付後の注意
14.4.1 貼付24時間後も本剤の成分が残っているため、使用済みの製剤は接着面を内側にして折りたたみ、小児の手及び目の届かない所に安全に廃棄すること。
14.4.2 本剤を扱った後は、手に付着した薬剤を除去するため、手を洗うこと。手洗い前に目に触れないこと。
廃棄時の注意は経皮吸収型製剤としては当然のものですが、高齢者が管理する場合は難しいかもしれませんね。
認知症治療薬としての注意点
8. 重要な基本的注意
8.1 定期的に認知機能検査を行う等患者の状態を確認し、本剤使用で効果が認められない場合、漫然と使用しないこと。
8.2 アルツハイマー型認知症では、自動車の運転等の機械操作能力が低下する可能性がある。また、本剤により、意識障害、めまい、眠気等があらわれることがあるので、自動車の運転等危険を伴う機械の操作に従事しないよう患者等に十分に説明すること。
漫然投与になりがちな薬剤なので、避けるよう注意していきたいですね。
AD自体の症状にも、ドネペジルの服用でも、集中力の低下が見られるため、「運転禁止薬」となっています。
ここは注意が必要ですが、現実的にはどうでしょうね?
皮膚障害について
経皮吸収型製剤と聞いて一番気になるのが皮膚障害です。
ですので、他の注意事項とはわけて解説したいと思います。
イクセロンパッチ/リバスタッチパッチ(リバスチグミンテープを含む)の調剤を行っていれば、皮膚障害での離脱も経験していると思います。
イクセロンパッチ/リバスタッチパッチは皮膚障害を軽減するために基剤の変更を行なったくらいです。
イクセロンパッチ/リバスタッチパッチの「適用部位紅斑、適用部位そう痒感、適用部位浮腫」副作用発現頻度は5%以上となっています。
皮膚障害の発現頻度
まずはアリドネパッチの皮膚障害発現頻度を見てみます。
その他の副作用に「適用部位障害」として記載されています。
11. 副作用
11.2 その他の副作用
適用部位障害
3%以上:適用部位そう痒感(24.9%)、適用部位紅斑(24.3%)、接触皮膚炎(12.6%)
1~3%未満:適用部位小水疱、適用部位丘疹、適用部位変色
1%未満:適用部位浮腫、適用部位皮膚剥脱、適用部位びらん、適用部位発疹、適用部位乾燥、適用部位湿疹、適用部位蕁麻疹、適用部位ざ瘡
ということで、貼付に関しては適用上の注意で細かい指示が記載されています。
14. 適用上の注意
14.2 薬剤貼付部位に関する注意
14.2.2 皮膚の損傷又は湿疹・皮膚炎等がみられる部位には貼付しないこと。
14.2.3 貼付部位にクリーム、ローション又はパウダー等を塗布しないこと。
14.2.4 貼付部位の皮膚を拭い、清潔にしてから本剤を貼付すること。
14.2.5 皮膚刺激を避けるため、貼付部位を毎回変更し、同一部位への貼付は、7日以上の間隔をあけること。
14.2.1〜12.4に記載されている内容はイクセロンパッチ/リバスタッチパッチと同様のものです。
ただ、14.2.5の記載についてはイクセロンパッチ/リバスタッチパッチにはない「7日間以上」の間隔が指定されています。
8. 重要な基本的注意
8.3 本剤の貼付による皮膚症状を避けるため、貼付部位を毎回変更すること。皮膚症状があらわれた場合には、ステロイド軟膏又は抗ヒスタミン外用剤等を使用するか、本剤の一時休薬、あるいは使用を中止するなど適切な処置を行うこと。
8.4 本剤を同一部位に連日貼付・除去を繰り返した場合、皮膚角質層の剥離等が生じ、血中濃度が増加するおそれがあるため、貼付部位を毎回変更すること。
アリドネパッチのサイズ
ここで気になるのがアリドネパッチのサイズです。
- 27.5mg:81mm×81mm(薬物層67mm×67mm、面積63cm2)
- 55mg:89mm×134mm(薬物層75mm×120mm、面積115cm2)
表は左右にスクロール可能です
| 医薬品名 | イクセロンパッチ18mg | リバスタッチパッチ18mg | リバスチグミン | テープ18mg「久光」 | フランドル | テープ40mg | ネオキシテープ | 73.5mg | アリドネパッチ | 27.5mg | モーラステープ | 20mg | アリドネパッチ | 55mg | モーラステープ | L40mg |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 小 | 大 | |||||||||||||||
| 全長 | 直径(約)3.6cm | 54.8mm×54.8mm | 63.5mm×63.5mm | 73.0mm×73.0mm | 81mm×81mm | 70mm×100mm | (7cm×10cm) | 89mm×134mm | 100mm×140mm | (10cm×14cm) | ||||||
| 面積 | (約)10cm2 | 30cm2 | 40cm2 | 52.5cm2 | 63cm2 | 70cm2 | 115cm2 | 140cm2 | ||||||||
リバスチグミンテープ「久光」の製剤設計の件があるので、面積が大きい=皮膚障害を起こしやすいというわけではないとは思います。
ですが、あまり大きいと患者さんの抵抗感に繋がりそうだなと思います。同じ場所への貼付を避けるのも難しくなるので、7日間間隔をあけるとなるとなかなか厳しいですね。
皮膚障害の対策は?
イクセロンパッチ/リバスタッチパッチでは、前日〜1週間前からヘパリン類似物質等の保湿剤を塗布することで皮膚障害の発現を予防できるという報告があります。
アリドネパッチに関しても同様の対策を試みる価値はありそうですね。
参考:工藤千秋,山川伸隆,中村 祐,塩原哲夫:保湿剤の塗布が リバスチグミン貼付剤の皮膚症状を軽減させる~皮脂欠乏症 を伴う認知症患者に保湿剤を貼付 1 週間前から塗布する有効 性の検討~.日早期認知症会誌,2013;6:98–102.
光線過敏症のリスク
「重要な基本的注意」に以下の記述があります。
8. 重要な基本的注意
8.6 光線過敏症が発現するおそれがあるので、衣服で覆う等、貼付部位への直射日光を避けること。また、本剤を剥がした後も、貼付していた部位への直射日光を避けること。
ドネペジルで光線過敏症・・・のイメージはなかったので少し気になりました。
「その他の注意」に根拠が記載されています。
15. その他の注意
15.2 非臨床試験に基づく情報
15.2.2 本剤を用いた動物実験(モルモット)で、皮膚光感作性が確認されている。
「適用上の注意」には以下のように記載されています。
14. 適用上の注意
14.2 薬剤貼付部位に関する注意
14.2.6 本剤を剥がした後は、貼付部位への直射日光を3週間は避けるよう指導すること。
RMPでは「重要な潜在的リスク」にあげられており、通常の医薬品安全性監視活動に加えて一般使用成績調査を実施することとなっています。
重要な潜在的リスクとした理由:
動物実験(モルモット)で皮膚光感作性が認められているが、本剤の国内臨床試験では、光線過敏症の発現は認められていない。 しかしながら、製造販売後の日常診療下においては、本剤の使用状況により光線過敏症が発現する可能性は否定できず、貼付製剤として、ベネフィット・リスクバランスに影響を及ぼす要因になり得ることより重要な潜在的リスクとした。
臨床試験で光線過敏症の発現はありませんが、皮膚症状の一つとして注意が必要とは思います。ただ、そもそも薬剤貼付部位を直射日光に晒すことは少ないと思います。
処方監査時の注意点
ここからは監査時にチェックしておきたい注意事項を整理していきます。
基本的にアリセプト(ドネペジル経口製剤)と同じと考えていいです。
相互作用(アリセプトと同様)
10. 相互作用
本剤は、主として薬物代謝酵素CYP3A4及び一部CYP2D6で代謝される。
アリドネパッチには併用禁忌は存在しておらず、併用注意のみになっています。
また、その内容もドネペジル経口製剤と同様となっています。
心疾患関連の注意事項
まず「特定の背景を有する患者に関する注意」の記載です。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 心疾患(心筋梗塞、弁膜症、心筋症等)を有する患者、電解質異常(低カリウム血症等)のある患者
QT延長、心室頻拍(torsade de pointesを含む)、心室細動、洞不全症候群、洞停止、高度徐脈、心ブロック(洞房ブロック、房室ブロック)等があらわれることがある。
9.1.2 洞不全症候群、心房内及び房室接合部伝導障害等の心疾患のある患者
迷走神経刺激作用により、徐脈あるいは不整脈を起こす可能性がある。
次に「副作用」の記載。
11. 副作用
11.1 重大な副作用
11.1.1 QT延長(1~3%未満)、心室頻拍(torsade de pointesを含む)、心室細動、洞不全症候群、洞停止、高度徐脈(いずれも頻度不明)、心ブロック(洞房ブロック、房室ブロック)(0.1~1%未満)、失神(頻度不明)
心停止に至ることがある。
11.1.2 心筋梗塞、心不全(いずれも頻度不明)
いずれもドネペジル塩酸塩経口製剤と同様の記載です。
実際、ドネペジル塩酸塩経口製剤において心臓関連の副作用で投与中止に至る経験をしている方も少なくないと思います。
RMPでは「重要な特定されたリスク」として「徐脈、心ブロック、洞不全症候群、洞停止、QT 延長、心室頻拍(torsade de pointes を含む)、心室細動、失神」、「心筋梗塞、心不全」があげられています。
徐脈、心ブロック、洞不全症候群、洞停止、QT 延長、心室頻拍(torsade de pointes を含む)、心室細動、失神
重要な特定されたリスクとした理由:
本剤のアルツハイマー型認知症患者を対象に実施した国内臨床試験において、心電図QT延長が1.3%(5/382例)、心室性期外収縮が0.5%(2/382例)、房室ブロック、徐脈、結節性調律、洞性不整脈、洞性徐脈、上室性期外収縮及び頻脈が各0.3%(1/382例)認められている。また、ドネペジル塩酸塩経口製剤の国内製造販売後において報告が集積されており、本剤の薬理作用からも発症が予測され、発現した場合に重篤な転帰を辿ると考えられることから重要な特定されたリスクとした。心筋梗塞、心不全
重要な特定されたリスクとした理由:
本剤の国内臨床試験において、心筋梗塞、心不全に該当する副作用は認められていない。しかしながら、ドネペジル塩酸塩経口製剤の国内製造販売後において報告が集積されており、発現した場合に重篤な転帰を辿ると考えられるため重要な特定されたリスクとした。
アセチルコリンの増加が心血管系の迷走神経を刺激し、慢性心不全に対して保護的に作用する可能性を示唆する研究もありますが、現時点ではQT延長等のリスクを重視して対応すべきと考えます。
参考:Li M, Zheng C, Kawada T, Inagaki M, Uemura K, Shishido T, Sugimachi M. Oral donepezil markedly suppresses the progression of cardiovascular remodeling and improves the prognosis in spontaneously hypertensive rats with myocardial infarction. ESC Congress 2018.
消化器関連の注意事項
まず「特定の背景を有する患者に関する注意」の記載です。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.3 消化性潰瘍の既往歴のある患者
胃酸分泌の促進及び消化管運動の促進により、消化性潰瘍を悪化させる可能性がある。
次に「副作用」の記載。
11. 副作用
11.1 重大な副作用
11.1.3 消化性潰瘍(胃・十二指腸潰瘍)、十二指腸潰瘍穿孔、消化管出血(いずれも頻度不明)
本剤のコリン賦活作用による胃酸分泌及び消化管運動の促進によって消化性潰瘍(胃・十二指腸潰瘍)、十二指腸潰瘍穿孔、消化管出血があらわれることがある。
11.2 その他の副作用
下痢、食欲不振(1~3%未満)
いずれもドネペジル塩酸塩経口製剤と同様の記載です。
ドネペジルといえば・・・な副作用なので説明の必要はないですね。
RMPにも「重要な特定されたリスク」として「消化性潰瘍、十二指腸潰瘍穿孔、消化管出血」、「消化器症状(食欲減退、悪心、嘔吐、下痢等)」があげられています。
消化性潰瘍、十二指腸潰瘍穿孔、消化管出血
重要な特定されたリスクとした理由:
本剤の国内臨床試験において、消化性潰瘍、十二指腸潰瘍穿孔及び消化管出血に該当する副作用は認められていない。しかしながら、ドネペジル塩酸塩経口製剤の国内製造販売後において報告が集積されており、本剤の薬理作用からも発症が予測され、発現した場合に重篤な転帰を辿ると考えられることから重要な特定されたリスクとした。
消化器症状(食欲減退、悪心、嘔吐、下痢等)
重要な特定されたリスクとした理由:
本剤のアルツハイマー型認知症患者を対象に実施した国内臨床試験において、下痢が1.3%(5/382例)、食欲減退が1.0%(4/382例)、胃炎、悪心及び嘔吐が各0.5%(2/382例)、腹部不快感、慢性胃炎、消化不良、胃食道逆流性疾患及び軟便が各0.3%(1/382例)認められている。ドネペジル塩酸塩経口製剤の国内製造販売後において報告が集積されており、本剤の薬理作用からも発症が予測されることから重要な特定されたリスクとした。
妊娠・授乳に関する注意
「特定の背景を有する患者に関する注意」の記載です。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療での有益性が危険性を上回ると判断される場合にのみ使用すること。ドネペジル塩酸塩経口製剤において、動物実験(ラット経口10mg/kg)で出生率の減少、死産児頻度の増加及び生後体重の増加抑制が報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
ラットに14C-ドネペジル塩酸塩を経口投与したとき、乳汁中へ移行することが認められている。
薬剤の性質上、妊婦・授乳婦に投与するケースは少ないと思いますが、頭の片隅においておきましょう。
そのほかRMP記載事項
そのほかでRMP「重要な特定されたリスク」に記載されているものは以下の通りです。
・パーキンソン症状
・肝炎、肝機能障害、黄疸
・脳性発作、脳出血、脳血管障害
・悪性症候群
・横紋筋融解症
・呼吸困難
・急性膵炎
・急性腎障害
・血小板減少
まとめ
アリドネパッチについてポイントをまとめたいと思います。
- ドネペジルの経皮吸収型製剤で内服と同等のAUCになるよう設計
- アリドネ27.5mg≒アリセプト5mg
- アリドネ55.5mg≒アリセプト10mg
- 55mg(経口製剤10mgに相当)への増量は27.5mgで4週間以上経過後
(経口製剤3mg相当のローディングドーズは存在しない) - パッチのサイズはかなり大きめ
- 27.5mgはモーラステープ20mgより少し小さい程度
- 55mgはモーラステープ20mgとL40mgの中間より少し大きいサイズ
- 背部・上腕部・胸部のいずれかに24時間ごとに貼付
- 同一部位への貼付は7日以上の間隔をあける
- 皮膚障害の頻度はかなり高い(約25%)
- 皮膚障害以外の注意事項はアリセプト(ドネペジル経口製剤)とほぼ同じ
経皮吸収製剤を得意とする帝國製薬が開発したドネペジルの新剤形。
このタイミングで登場する意味を考えてみたのですが、これだ!という処方例が思い浮かばなかったです。
リバスチグミン貼付剤の調剤を多く行っている方が実感されていると思うのですが、ほとんどの患者さんは他にも内服を行っているケースがほとんどのため、ChE-Iのみが貼付剤となったところでQOLの向上には繋がりにくいところがあります。
また、一つだけ貼付剤となることでかえって介護者の手間がかかってしまう問題もあります。
そして一番気になるのは皮膚障害とそれに伴い同一部位への貼付に7日以上の間隔が必要なことですね。
ドネペジル内服ではなくアリドネパッチじゃないといけない!ってケースがあればいいのですが・・・。
参考資料
- アリドネパッチ27.5mg/アリドネパッチ55mg 添付文書・IF(帝國製薬)
- アリドネパッチ27.5mg/アリドネパッチ55mgに係る医薬品リスク管理計画書(RMP)
- 新医薬品の「使用上の注意」の解説 アリドネパッチ27.5mg/アリドネパッチ55mg(帝國製薬)
- 認知症疾患診療ガイドライン2017(日本神経学会)
- アルツハイマー病の治療―現状と解決すべき諸問題(下濱俊:日本薬理学雑誌.2008;131(5):351-356)
- アルツハイマー病治療薬の基礎(山西嘉晴ほか:日本薬理学雑誌.2007;130(6):489-493)
- 公益社団法人日本医師会:超高齢社会におけるかかりつけ医のための適正処方の手引き 2.認知症.2018年4月
- アリセプト錠 添付文書(エーザイ)
- イクセロンパッチ/リバスタッチパッチ 添付文書
- 新規アルツハイマー型認知症治療薬ガランタミン(レミニール®)の薬理学的特性および臨床試験成績(日薬理誌(Folia Pharmacol. Jpn.)138,122~126(2011))