2021年1月22日に承認された腎性貧血を適応とするマスーレッド錠(成分名:モリデュスタット)についてまとめた記事です。 マスーレッドはHIF-PH阻害薬と呼ばれる薬剤で、内因性エリスロポエチンの増加作用等により腎性貧血を改善する薬剤です。 これまで腎性貧血にはネスプ(成分名:ダルベポエチン アルファ)やミルセラ(成分名:エポエチン ベータ ペゴル)などのESA製剤が使用されてきましたが、HIF-PH阻害薬はそれに代わる薬剤(ポストネスプとも呼ばれます)として期待されています。 マスーレッド錠は5剤目のHIF-PH阻害薬になります。
マスーレッドについて
まずはマスーレッド錠の承認の背景について簡単にまとめます。
マスーレッド錠(モリデュスタットナトリウム)は腎性貧血に対する適応を有するHIF-PH阻害薬(HIF-PHI*1)と呼ばれる薬剤です。
腎性貧血は腎機能の低下に伴いエリスロポエチン(EPO*2)の産生が低下することによって生じる貧血です。
これまでは腎性貧血の治療にはEPOの補給を行うためにネスプ(成分名:ダルベポエチン アルファ)やミルセラ(成分名:エポエチン ベータ ペゴル)などの赤血球造血刺激因子製剤(ESA*3製剤)が投与されてきました。
それに対してHIF-PH阻害薬は、HIFプロリン水酸化酵素(HIF-PH*4)を阻害することで、HIF経路を活性化させ、内因性EPOの産生を増やし、腎性貧血を改善する薬剤です。(このメカニズムの解明は2019年のノーベル医学・生理学賞を受賞しています)
その作用機序からHIF-PH阻害薬、HIF安定化薬、HIF活性化薬と呼ばれています。
これまで腎性貧血に対して使用されてきたESA製剤とは異なり、経口投与の薬剤のため透析を行っていない(透析と同時にESA製剤を投与できない)保存期CKDの患者さんのQOL改善が期待されています。
最初に登場したHIF-PH阻害薬だったエベレンゾの適応は透析期の腎性貧血のみでした(2020年11月27日に「透析施行中の腎性貧血」→「腎性貧血」に適応拡大)が、その後、ダーブロックとバフセオ、エナロイという保存期CKDに対しても使用可能な薬剤が登場しています。
この記事では5剤目のHIF-PH阻害薬になるマスーレッドの特性や注意点などについて詳しく解説します。
マスーレッドの基本情報
基本情報をまとめます。
| 医薬品名 | マスーレッド錠5mg マスーレッド錠12.5mg マスーレッド錠25mg マスーレッド錠50mg(薬価未収載) マスーレッド錠75mg |
| 開発コード | BAY85-3934(遊離塩基) BAY1053048(ナトリウム塩) |
| 成分名 | モリデュスタットナトリウム |
| 英語名 | MUSREDO tablets(Molidustat Sodium) |
| 製造販売元 | バイエル薬品株式会社 |
| 命名の由来 | 特になし |
| 効能・効果 | 腎性貧血 |
| 用法・用量 | 〈保存期慢性腎臓病患者〉 赤血球造血刺激因子製剤で未治療の場合 通常、成人にはモリデュスタットとして1回25mgを開始用量とし、1日1回食後に経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1回200mgとする。赤血球造血刺激因子製剤から切り替える場合 通常、成人にはモリデュスタットとして1回25mg又は50mgを開始用量とし、1日1回食後に経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1回200mgとする。〈透析患者〉 通常、成人にはモリデュスタットとして1回75mgを開始用量とし、1日1回食後に経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1回200mgとする。 |
| 指定等 | なし |
| 審議 | 2020年12月2日付 薬食審第一部会(web審議) |
| 承認日 | 2021年1月22日 |
| 薬価収載日 収載時薬価 | 2021年4月21日 マスーレッド錠5mg:44.30円/錠、マスーレッド錠12.5mg:93.70円/錠、マスーレッド錠25mg:165.10円/錠、マスーレッド錠75mg:405.30円/錠 ※マスーレッド錠50mgは薬価未収載 |
| 薬価算定方式 | 類似薬効比較方式(II)で、過去6年間の薬理作用類似薬(HIF-PH阻害薬)の最低一日薬価(457.00円)を元にマスーレッド錠75mgの薬価を算出 ※ESA前治療ありの成人血液透析患者を対象とした国内第III相試験での平均投与量に基づき1日薬価を計算 その他の規格についてはダーブロック錠4mgと同錠6mgの規格間比(0.8173)を利用して算出 |
| 販売開始 | 2021年4月23日 |
| 新医薬品の投与日数制限 | 対象 2022年4月末日まで |
腎性貧血とマスーレッドの作用機序
まず、腎性貧血について簡単に説明してからマスーレッドの作用機序について説明していきます。
腎性貧血とは?
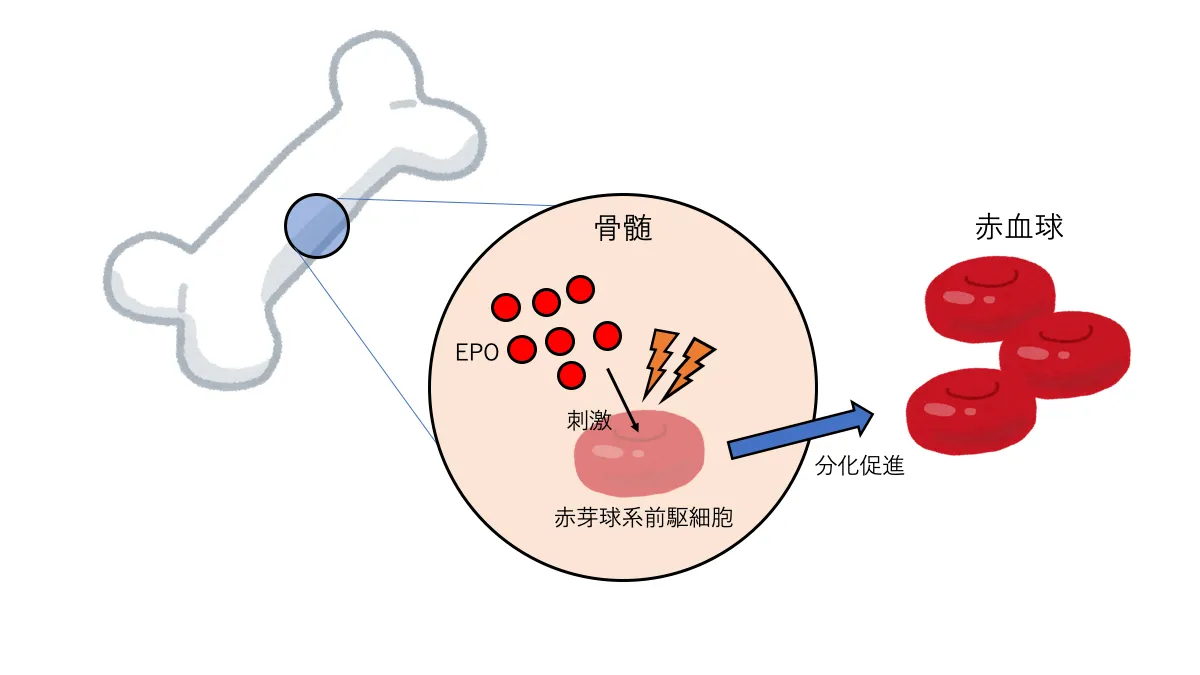
腎性貧血とは慢性腎臓病(CKD*5)の進行に伴い生じる貧血で、その主な原因は腎臓でエリスロポエチン(EPO)が十分に産生されなくなることです。EPOは赤血球の産生を促進する造血因子の一つで、骨髄中の赤芽球系前駆細胞を刺激し、赤血球への分化と増殖を促進します。
CKDの基礎とeGFR
日本でのCKD患者数は1,330万人(成人の8人に1人)と考えられており、新たな国民病の一つと言われています。
CKDの原因は多岐に渡りますが、腎炎などの腎疾患だけでなく、自己免疫疾患、加齢、生活習慣病(糖尿病、高血圧など)、薬の副作用など様々なものがあります。
その定義は「腎臓の構造または機能の異常が3カ月を超える場合」とされています。
・尿検査※1、画像診断、血液検査、病理などで腎障害の存在が明らか
・eGFR※2 < 60ml/分/1.73㎡
※1:タンパク尿 ≧ 0.15g/gCr(アルブミン尿 ≧ 30mg/gCr) ※2:eGFR(ml/分/1.73㎡) = 194×Cr-1.094×年齢(歳)-0.287(女性は×0.739)
CKDが進行することで末期腎不全(ESKD*6)となり透析や腎移植が必要となってしまいます。
ですが、CKD患者ではESDKに移行するリスクよりも死亡リスクの方が高くなっており、その多くが心血管疾患(CVD*7)による死亡です。
そのため、CKDではCVDによる死亡を回避するために、腎機能だけでなく新血管リスクまでを考慮していくことが重要となります。(もう少し後で心腎貧血症候群という概念を説明します)
CKDの重症度は、原疾患(Cause)、腎機能(GFR)、蛋白尿・アルブミン尿(Albuminuria)の頭文字をとったCGA分類で評価しますが、腎性貧血においては以下の表に示すeGFRによるステージ分類が目安となります。
| CKDステージ | 1 | 2 | 3 | 4 | 5 |
| eGFR値 | 90以上 | 60〜89 | 30〜59 | 15〜29 | 15未満 |
| 腎臓病の程度 | 正常 | CKD | ESKD | ||
| 軽度低下 | 中程度低下 | 高度低下 | |||
| 治療法 | 予防 | 食生活の改善・薬物療法 | 透析・腎移植 | ||
腎性貧血の発症機序
腎性貧血は「腎臓においてヘモグロビン(Hb)の低下に見合った十分量のエリスロポエチン(EPO)が産生されないことによって引き起こされる貧血であり、貧血の主因が腎障害(CKD)以外に求められないもの」と定義されています。
CKDステージ3以降に腎性貧血の頻度が増加しますが、合併症などによっては早期から貧血を起こす場合もあります。
日本人における腎性貧血の診断基準値は以下のようになっています。
| 性別 | 60歳未満 | 60歳以上 70歳未満 | 70歳以上 |
| 男性 | Hb<13.5g/dL | Hb<12.0g/dL | Hb<11.0g/dL |
| 女性 | Hb<11.5g/dL | Hb<10.5g/dL | Hb<10.5g/dL |
腎性貧血の原因は主にEPOの産生不足とされていますが、他にも様々な原因が考えられます。
- 赤血球の造血抑制
- EPO産生不足
- 尿毒症性毒素による造血抑制
- 高サイトカイン血症によるEPO感受性低下
- 赤血球寿命の短縮(尿毒素)
- 鉄代謝の障害(高ヘプシジン血症)
- 透析回路における残血、出血
- 栄養障害(ビタミン、葉酸など)
JSDT腎性貧血ガイドライン2015
貧血は心不全を悪化させる原因となり、腎性貧血が進行するほど末期腎不全への移行や死亡率が上昇します。(RENAAL試験のサブ解析)
貧血による虚血や酸化ストレスが体液貯留や炎症を引き起こすことで、心臓病や腎臓病の病態悪化に関与すると考えられており、心腎貧血症候群という概念として提唱されています。
腎性貧血の治療
腎性貧血と診断されたからと言って、必ずしもすぐに治療が必要となるわけではなく、治療開始は個々の状態によって判断されます。
特に腎性貧血においては健常者と同等のHb=13g/dl以上を目指した場合、有害事象が増え、予後が改善されないことが明らかになっています。(CREATE 研究、CHOIR研究)
そのためガイドラインでは、HD*8(血液透析)・PD*9(腹膜透析)・ND*10(保存期CKD)それぞれの場合において、死亡リスクの上昇、QOL低下のエビデンスを元に開始基準となるHb値と共に目標Hb値が定められています。
第 2 章 腎性貧血治療の目標Hb値と開始基準 CQ1.腎性貧血治療において維持すべき目標 Hb 値と開始基準は何か? ステートメント 1
- 成人の血液透析(HD)患者の場合,維持すべき目標Hb値は週初めの採血で10g/dL以上12g/dL未満とし,複数回の検査でHb値10g/dL未満となった時点で腎性貧血治療を開始することを推奨する.(1C)
- 成人の保存期慢性腎臓病(CKD)患者の場合,維持すべき目標Hb値は11g/dL以上13g/dL未満とし,複数回の検査でHb値11g/dL未満となった時点で腎性貧血治療を開始することを提案する.(2C) ただし,重篤な心・血管系疾患(CVD)の既往や合併のある患者,あるいは医学的に必要のある患者にはHb値12g/dLを超える場合に減量・休薬を考慮する.(not graded)
- 成人の腹膜透析(PD)患者の場合,維持すべき目標Hb値は11g/dL以上13g/dL未満とし,複数回の検査でHb値11g/dL未満となった時点で腎性貧血治療を開始することを提案する.(2D) PD患者のESA投与方法は,基本的に保存期CKD患者に準じて考えることが望ましい.(not graded)
- HD,PD,保存期CKD患者のいずれにおいても,実際の診療においては個々の症例の病態に応じ,上記数値を参考として目標Hb値を定め治療することを推奨する.(1C)
慢性腎臓病患者における腎性貧血治療のガイドライン2015
HDを受けている場合、日本では週初め(月曜日or火曜日:中2日)の透析前に採血する施設がほとんどです。 その場合、循環血が除水を受ける直前なので、Hb値が最も低い(Hb濃度が薄い)状態での数値になるため、HDの場合のHb値はPD、NDの場合よりも低くなっています。
鉄補充療法を選択する場合
JSDT腎性貧血ガイドライン2015では、それまでESA投与が基本とされていた腎性貧血の治療が「ESA投与」と「鉄補充療法」のいずれか適切な方法で行うように変更されました。
当然ですが、鉄欠乏の状態だといくらEPOによる刺激があっても正常な赤血球が増加できないので貧血は改善しません。
その場合は鉄欠乏の治療を行う、もしくは鉄補給と同時にESA投与(HIF-PH阻害薬の投与)が必要となります。
参考までに鉄補充療法を選択する場合についてJSDT腎性貧血ガイドライン2015では以下のように記載されています。
第 4 章 鉄の評価と補充療法 CQ2:鉄の評価はどのような方法が推奨されるか? ステートメント 2
- 貧血を合併するCKD患者は鉄欠乏・鉄過剰となることがあるため定期的な鉄評価を行う(鉄投与中は月1回,非投与時には3か月に1回程度).(not graded)
- 鉄評価には血清フェリチン値,TSATを用いることを推奨する.(1C)
CQ3:鉄剤の投与・中止基準は何か? ステートメント 3-1
- ESA製剤も鉄剤も投与されておらず目標Hb値が維持できない患者において,血清フェリチン値が50ng/mL未満の場合,ESA投与に先行した鉄補充療法を提案する.(2D)
- ESA投与下で目標Hb値が維持できない患者において,血清フェリチン値が100ng/mL未満かつTSATが20%未満の場合,鉄補充療法を推奨する.(1B)
ステートメント 3-2※
- ESA投与下で目標Hb値が維持できない患者において,以下の両者を満たす場合には鉄補充療法を提案する.(2C)
- 鉄利用率を低下させる病態が認められない場合
- 血清フェリチン値が100ng/mL未満またはTSATが20%未満の場合
- 血清フェリチン値が300ng/mL以上となる鉄補充療法は推奨しない.(2D)
※このステートメントは,作成ワーキンググループ会議にて全会一致ではなく2/3以上の合意をもって採択された 唯一の記載である.したがって,この内容に関してはまだ議論が多く残されていると考えている. 慢性腎臓病患者における腎性貧血治療のガイドライン2015
HIF-PH阻害薬の作用機序
いよいよここからはマスーレッドの作用機序についてまとめていきたいと思います。
マスーレッドの有効成分モリデュスタットはPHDを阻害することでHIF経路を活性化(HIF-PH阻害薬)し、腎性貧血に対して効果を発揮します。
中心となるのはエリスロポエチン(EPO)産生促進ですが、HIFの活性化による様々な作用により腎性貧血を改善します。
- EPO産生促進
- 腸管の鉄吸収促進に関わる遺伝子の転写促進
- トランスフェリン・トランスフェリン受容体遺伝子の転写促進
- ヘプシジンの産生・放出の抑制
腎性貧血の治療で従来使用されてきたESA製剤に置き換わる薬剤となります。
HIF経路によるエリスロポエチン産生
HIF-PH阻害薬によるEPO産生促進のメカニズムを知るために、まずは腎臓でHIFがどのように働いてEPOが産生されるかについて解説します。
エリスロポエチンは主に腎臓の近位尿細管周辺の間質に存在する繊維芽細胞様細胞(EPO産生細胞)で生成されます。
貧血により腎血流量が低下し酸素供給が低下すると、EPO産生細胞の酸素分圧が低下します。
この酸素分圧の低下に呼応してEPOの産生が高まるのですが、そこで中心的な役割を果たすのが低酸素誘導因子(HIF)です。
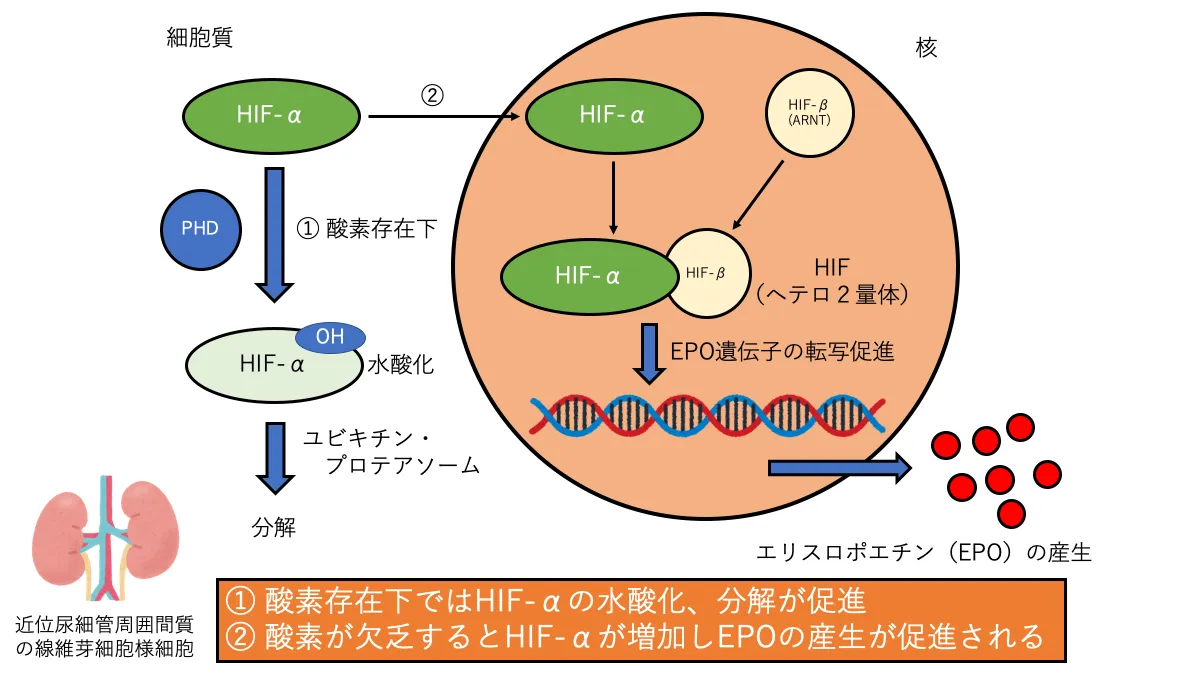
HIFはαサブユニット(HIFα)とβサブユニット(HIFβ、ARNT*11)からなる2量体の転写因子です。
HIFはEPO遺伝子の転写を促進する働きを持っています。
※HIFにはHIF1、HIF2、HIF3が存在し、それぞれのαサブユニットとしてHIF1α、HIF2α、HIF3αが存在しますが、この記事の中では特に区別していません。
HIFαは細胞質に存在し、核内でHIFβと結合して2量体(HIF)となり、EPO遺伝子の転写を促進します。
細胞質にはHIFαのプロリンを水酸化するプロリン水酸化酵素(PHD*12)が存在しています。
PHDはHIFαのプロリンを水酸化し、プロリンが水酸化されたHIFαは細胞質内のユビキチン・プロテアソームにより分解されてしまいます。
PHDは酸素存在化で活性化される酵素です。そのため、貧血によりEPO産生細胞の酸素分圧が低下(酸素が不足)するとEPOの産生量が増加して貧血が改善されます。
このように、HIF経路によるEPO産生ではPHDが酸素センサーの役割を果たし、EPOの産生量を調整しています。
腎障害時のHIF経路
ですが、腎障害時にはHIF経路がうまく機能してくれません。
正常な腎臓では尿細管でのNa再吸収が活発に行われることで酸素が消費されています。
そのため、酸素供給が低下すると、酸素消費と酸素供給のバランスが崩れて酸素分圧が低下(酸素が不足)します。
酸素がない環境ではPHDが抑制されるため、HIFが活性化しEPOの産生が増加します。
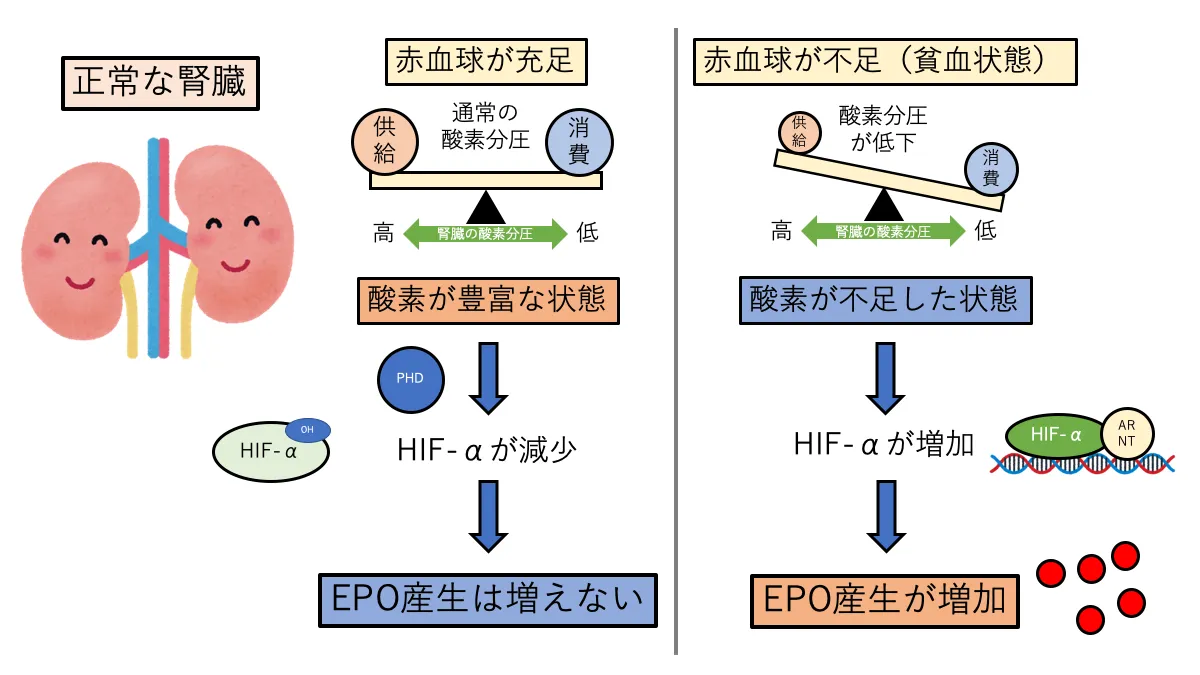
腎機能が低下した場合は、尿細管の機能が低下しているため、酸素の消費量が減少しています。
酸素消費量が少ない場合、酸素供給量が低下しても酸素分圧がそれほど低下しない(酸素が不足しない)ため、PHDの働きは低下せず、EPOの産生は増加しません。
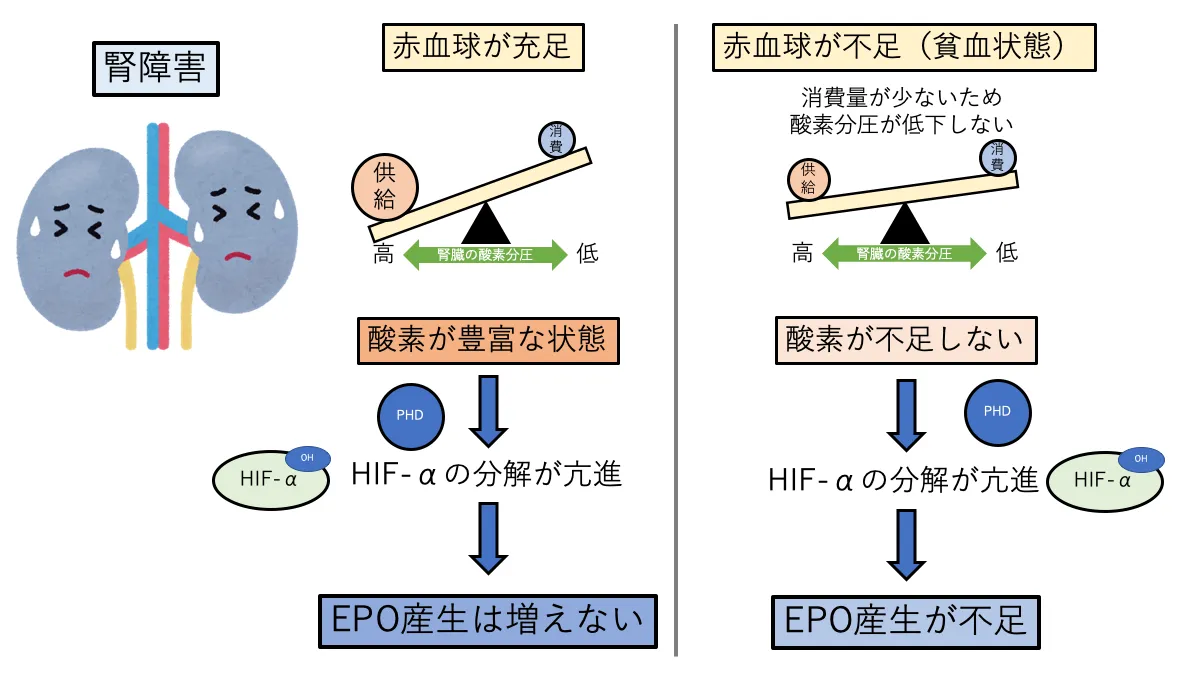
腎機能が低下した状態では、何らかの理由で赤血球数が減少してもEPO産生増加によるフィードバックが機能しないため、EPOの相対的欠乏により貧血を起こしてしまいます。
これが腎性貧血の主な原因と考えられています。
HIF活性化によるEPO産生促進
酸素濃度によって調節されているHIF経路ですが、HIF-PH阻害薬はPHDを直接阻害することで、酸素分圧に関係なくHIFを活性化します。
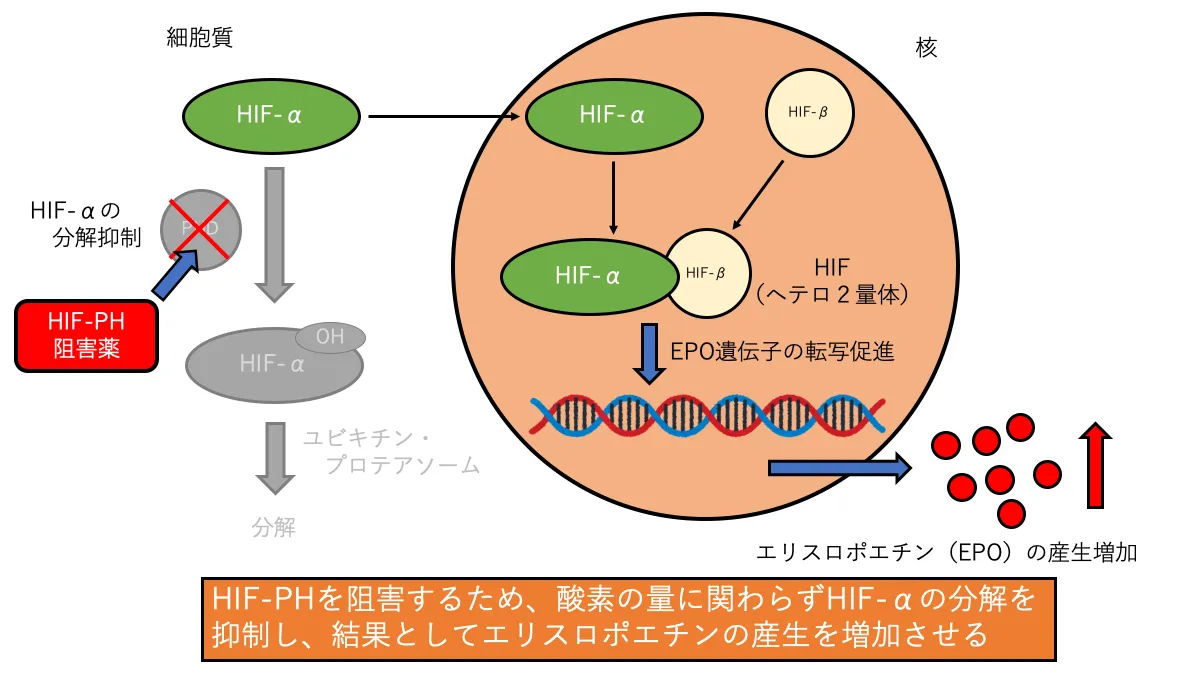
活性化されたHIFによりEPO遺伝子の転写行われ、EPO産生を促進します。
この内因性EPOの増加作用こそがHIF-PH阻害薬が腎性貧血を改善する主たる作用になりますが、そのほかにも腎性貧血の改善に繋がる作用が期待されています。
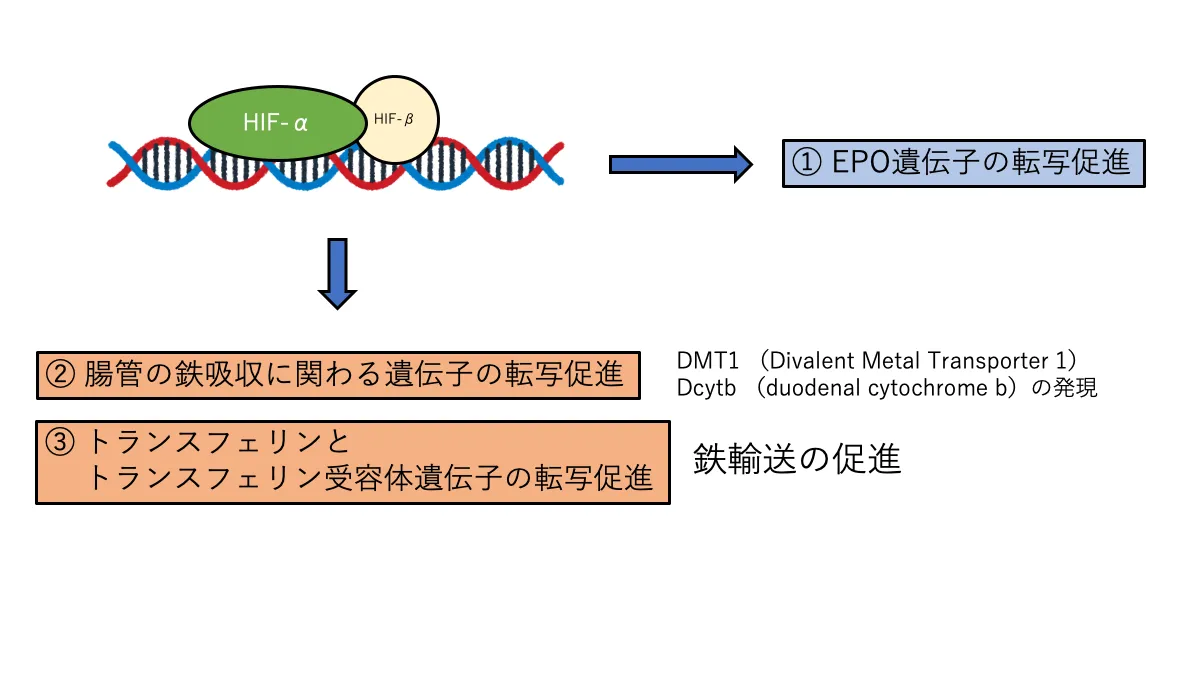
HIF活性化による鉄吸収の促進
HIFは腸管での鉄吸収に関与するDMT1*13遺伝子やDcytb*14遺伝子の転写も促進します。さらに、体内での鉄輸送を担うトランスフェリンの産生やトランスフェリン受容体の産生に関わる遺伝子の転写も促進します。
そのため、HIF-PH阻害薬によりHIFが活性化されることで体内の鉄吸収や鉄輸送が促進されます。
HIF活性化による高ヘプシジン血症の改善
腎性貧血の原因の一つに高ヘプシジン血症があります。
ヘプシジンは血清鉄濃度の恒常性を担うホルモンです。
ヘプシジンは血清鉄濃度が上昇することで肝臓から放出され様々な作用で血清鉄濃度を低下させます。
- 肝臓からの貯蔵鉄の放出抑制
- 小腸上部での鉄吸収抑制
- マクロファージによる老化赤血球からの鉄回収抑制
腎性貧血ではEPOによる赤血球への分化が不足しているため、鉄の利用が低下し、血清鉄濃度が上昇しています。
また、慢性的な炎症(CKD)により高IL-6血症を起こしているため、IL-6によるヘプシジンの産生が促進されています。
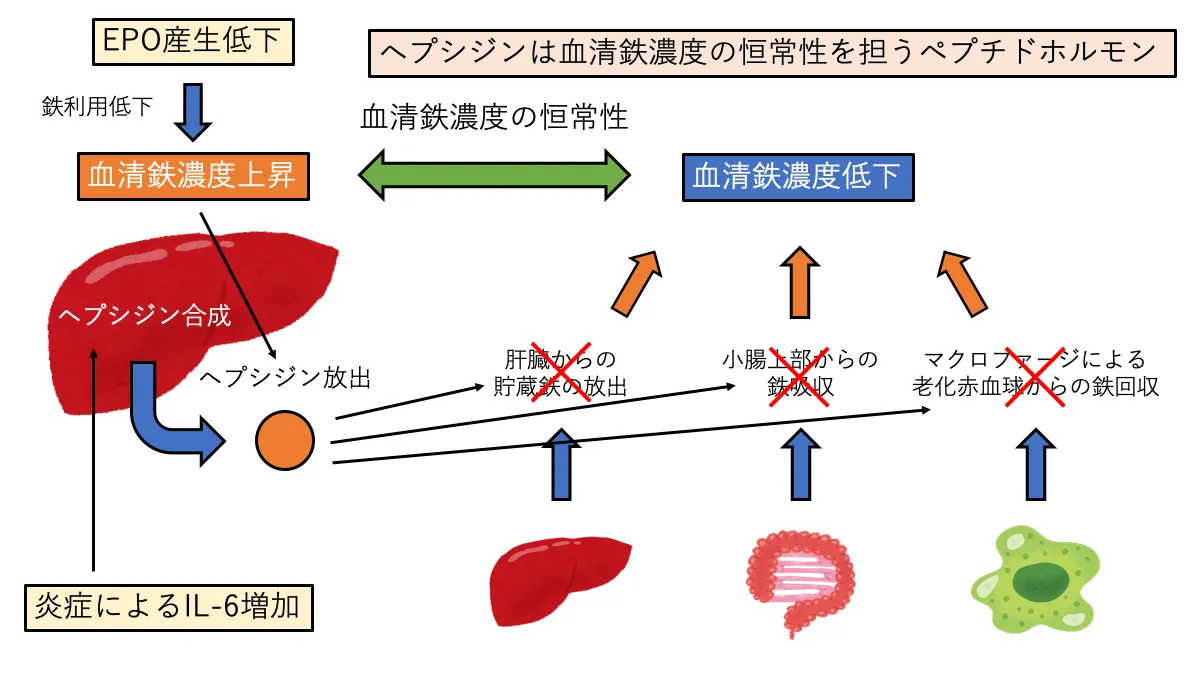 このように、高ヘプシジン血症により血清鉄濃度が低下してしまうのも腎性貧血の原因となっています。
このように、高ヘプシジン血症により血清鉄濃度が低下してしまうのも腎性貧血の原因となっています。
HIF活性化によりEPOが産生、鉄利用が促進することでヘプシジンの放出が抑制されると同時に、HIF自体がヘプシジンの産生を抑制する効果もあると考えられています。
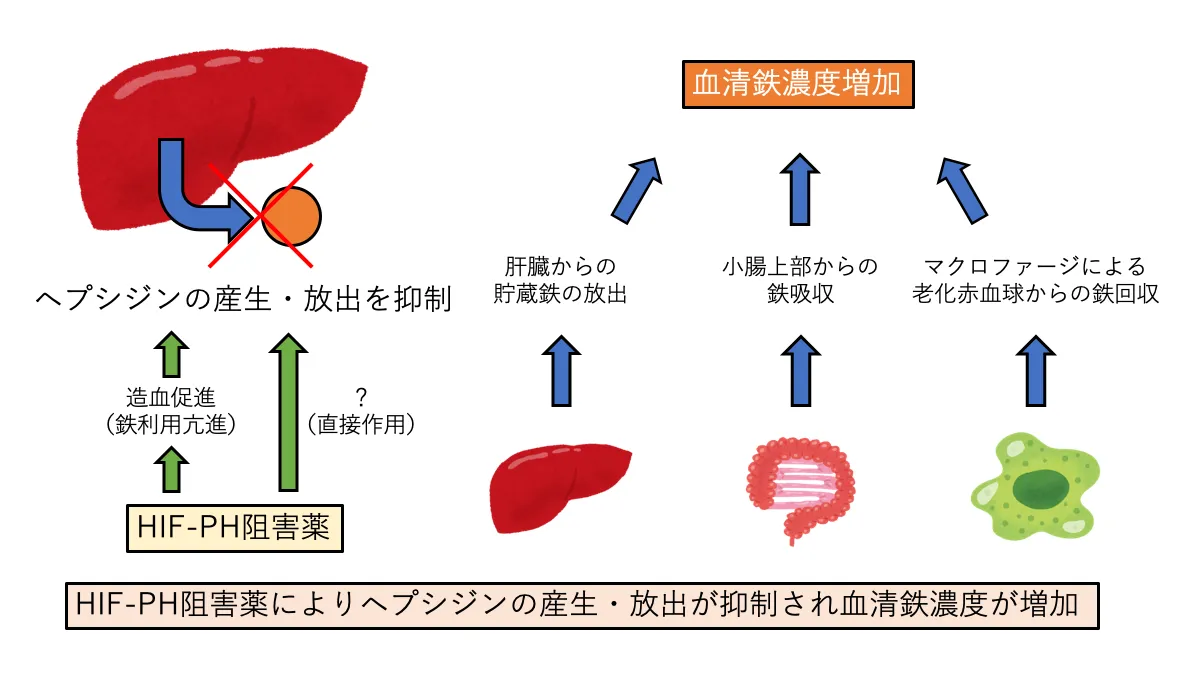 このようにHIF-PH阻害薬は高ヘプシジン血症を改善することでも腎性貧血に対する効果を発揮できると期待されています。
このようにHIF-PH阻害薬は高ヘプシジン血症を改善することでも腎性貧血に対する効果を発揮できると期待されています。
そのほか期待される効果
HIF経路は他にも様々な働きに関与していることが知られています。
・嫌気的解糖に関連する酵素の誘導(酸素不足化のエネルギー供給改善)
・cytochrome oxidaseサブユニットの発現調節(好気的解糖の調節)
このあたりの作用もHIF-PH阻害薬の効果に影響していると言われています。
EPO抵抗性貧血に対する効果
腎性貧血の中にはESA製剤に対して低反応性の、EPO抵抗性を有する腎性貧血も存在します。
ESA抵抗性については様々な理由が考えられますが、内因性EPOの増加だけでなく様々な貧血改善作用を持つHIF-PH阻害薬が効果を発揮する可能性があるため期待されています。
また、極めて稀とは言われていますが、ESA製剤では抗エリスロポエチン抗体による赤芽球癆(PRCA*15)が報告されています。
HIF-PH阻害薬であればPRCAも回避できるはずなので、それも大きなメリットとなりそうです。
マスーレッド錠のDI
ここからはマスーレッド錠の添付文書、インタビューフォーム、RMP、審査結果報告書から得ることのできる情報についてまとめていきたいと思います。
警告
血栓塞栓症に関して警告が記載されています。
RMPにも記載されていますが、HIF-PH阻害薬では血栓塞栓症が最も重要なリスクになります。
1. 警告
本剤投与中に、脳梗塞、心筋梗塞、肺塞栓等の重篤な血栓塞栓症があらわれ、死亡に至るおそれがある。本剤の投与開始前に、脳梗塞、心筋梗塞、肺塞栓等の合併症及び既往歴の有無等を含めた血栓塞栓症のリスクを評価した上で、本剤の投与の可否を慎重に判断すること。また、本剤投与中は、患者の状態を十分に観察し、血栓塞栓症が疑われる徴候や症状の発現に注意すること。血栓塞栓症が疑われる症状があらわれた場合には、速やかに医療機関を受診するよう患者を指導すること。
マスーレッド錠 添付文書 バイエル薬品株式会社
インタビューフォームには下記の通り警告の理由が記載されています。
VIII.安全性(使用上の注意等)に関する項目
1.警告内容とその理由
(解説)
国内第III相臨床試験5試験(試験19349、19350、19351、19352、19353)の併合データにおいて、本剤との因果関係が関係ありと判断された有害事象(副作用)として「ラクナ梗塞」1/393例(0.3%)が認められた。 また、国内第III相臨床試験実薬対照3試験(試験19349、19350、19352)の併合データにおいて、血栓塞栓症関連の有害事象(治験薬との因果関係を問わない)の発現割合は、ダルベポエチン アルファ群と比較してモリデュスタット群で高い傾向が認められ、重篤な有害事象の発現割合についてもモリデュスタット群で高い傾向が認められた(表1、表2)。
モリデュスタット投与中に、脳梗塞、心筋梗塞、肺塞栓等の重篤な血栓塞栓症があらわれ、死亡に至るおそれがあることから、本剤の使用に際しては、以下の点に十分に注意すること。
- モリデュスタットの投与開始前に、脳梗塞、心筋梗塞、肺塞栓等の合併症及び既往歴の有無等を含めた血栓塞栓症のリスクを評価した上で、モリデュスタットの投与の可否を慎重に判断すること。
- モリデュスタット投与中は、患者の状態を十分に観察し、血栓塞栓症が疑われる徴候や症状の発現に注意すること。
- 血栓塞栓症が疑われる症状があらわれた場合には、速やかに医療機関を受診するよう患者を指導すること。
マスーレッド錠 インタビューフォーム バイエル薬品株式会社
あとで紹介する重要な基本的注意やRMP(重要な特定されたリスク)に記載されていますが、HIF-PH阻害薬ではHb値の上昇に伴い血液粘稠度が増すことで血栓塞栓症が発現する恐れがあるため、定期にHbを測定して投与量を調節する必要があります。
同様の機序で血栓塞栓症のリスクが知られているESA製剤では警告記載はありませんが、これはHIF-PH阻害薬は経口投与であるため、(1年後には)長期投与となり、Hb測定が疎かになった結果、血栓塞栓症が発生することがないように注意が必要なためではないかと考えます。
また、注射剤に抵抗があり治療を躊躇っていた境界域の患者さんでも使用可能になるケースが多く、使用する患者さんが多くなる可能性が高いことも警告記載の理由かもしれません。
妊婦への投与は禁忌
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 妊婦又は妊娠している可能性のある女性
マスーレッド錠 添付文書 バイエル薬品株式会社
過敏症の既往歴は当然のとことながら、マスーレッドは妊娠中の投与が禁忌となっています。
現在(R3.3.10時点)で承認されているHIF-PH阻害剤5剤のうち、マスーレッド以外ではエナロイとエベレンゾが妊娠中の投与が禁忌です。
| 禁忌 | エベレンゾ | ダーブロック | バフセオ | エナロイ | マスーレッド |
| 過敏症 | × | × | × | × | × |
| 妊娠 | × | – | – | × | × |
妊娠可能な年齢の女性は避妊を促す必要あり
妊娠中の投与に関しては「9. 特定の背景を有する患者に関する注意」にもう少し詳しく記載されています。
9. 特定の背景を有する患者に関する注意
9.4 生殖能を有する者
妊娠可能な女性には、本剤投与中及び投与終了後一定期間は適切な避妊を行うよう指導すること。ラットにおいて、臨床最大用量投与時の非結合型曝露量(AUCu)の3.1倍の曝露量で着床後死亡の増加と生存胎児数減少が報告されている。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。ラットにおいて、臨床最大用量投与時の非結合型曝露量(AUCu)の1.2倍以上の曝露量で着床後死亡の増加、平均生存児数の減少、死産児の増加等が観察されている。また、臨床最大用量投与時の非結合型曝露量(AUCu)の7.3倍の曝露量で眼球奇形の発生率の増加が報告されている。
マスーレッド錠 添付文書 バイエル薬品株式会社
ここにも記載されているように、非臨床試験(ラットに対する投与)で、さらに最大投与量を超えた場合のデータではありますが、着床後死亡の増加、平均生存児数の減少、死産児の増加、眼球奇形の発生率の増加等が認められたことが禁忌の理由です。
妊婦やその可能性がある場合のみではなく、妊娠可能な年齢にある女性に対しては適切な避妊を行うように指導することが求められています。
効能・効果:腎性貧血(保存期・透析期に関わらず使用可能)
マスーレッド錠の効能・効果は「腎性貧血」です。
マスーレッド錠は他のHIF-PH阻害薬と同様に腎性貧血であれば透析期・保存期の区別なく使用可能です。
(用法・用量については透析の有無などで分かれているので後で解説します)
腎性貧血治療開始の目安
効能・効果には以下の注意書きが加えられています。
5. 効能又は効果に関連する注意
赤血球造血刺激因子製剤で未治療の場合の本剤投与開始の目安は、保存期慢性腎臓病患者及び腹膜透析患者ではヘモグロビン濃度で11g/dL未満、血液透析患者ではヘモグロビン濃度で10g/dL未満とする。
マスーレッド錠 添付文書 バイエル薬品株式会社
腎性貧血の説明で紹介したJSDT腎性貧血ガイドライン2015の治療開始基準に従って投与を開始します。
| 状態 | 治療開始のHb値 | 目標Hb値 |
| ND(保存期CKD) | 11g/dL未満 | 11g/dL以上13g/dL未満 |
| PD(腹膜透析) | ||
| HD(血液透析) | 10g/dL未満 | 10g/dL以上12g/dL未満 |
用法・用量(保存期・腹膜透析と血液透析で開始用量が変化)
6. 用法及び用量
〈保存期慢性腎臓病患者〉
赤血球造血刺激因子製剤で未治療の場合
通常、成人にはモリデュスタットとして1回25mgを開始用量とし、1日1回食後に経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1回200mgとする。
赤血球造血刺激因子製剤から切り替える場合
通常、成人にはモリデュスタットとして1回25mg又は50mgを開始用量とし、1日1回食後に経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1回200mgとする。
〈透析患者〉
通常、成人にはモリデュスタットとして1回75mgを開始用量とし、1日1回食後に経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1回200mgとする。
マスーレッド錠 添付文書 バイエル薬品株式会社
用法・用量は保存期か透析かで変化します。
さらに保存期の場合、ESA製剤からの切り替えかどうかで変化します。
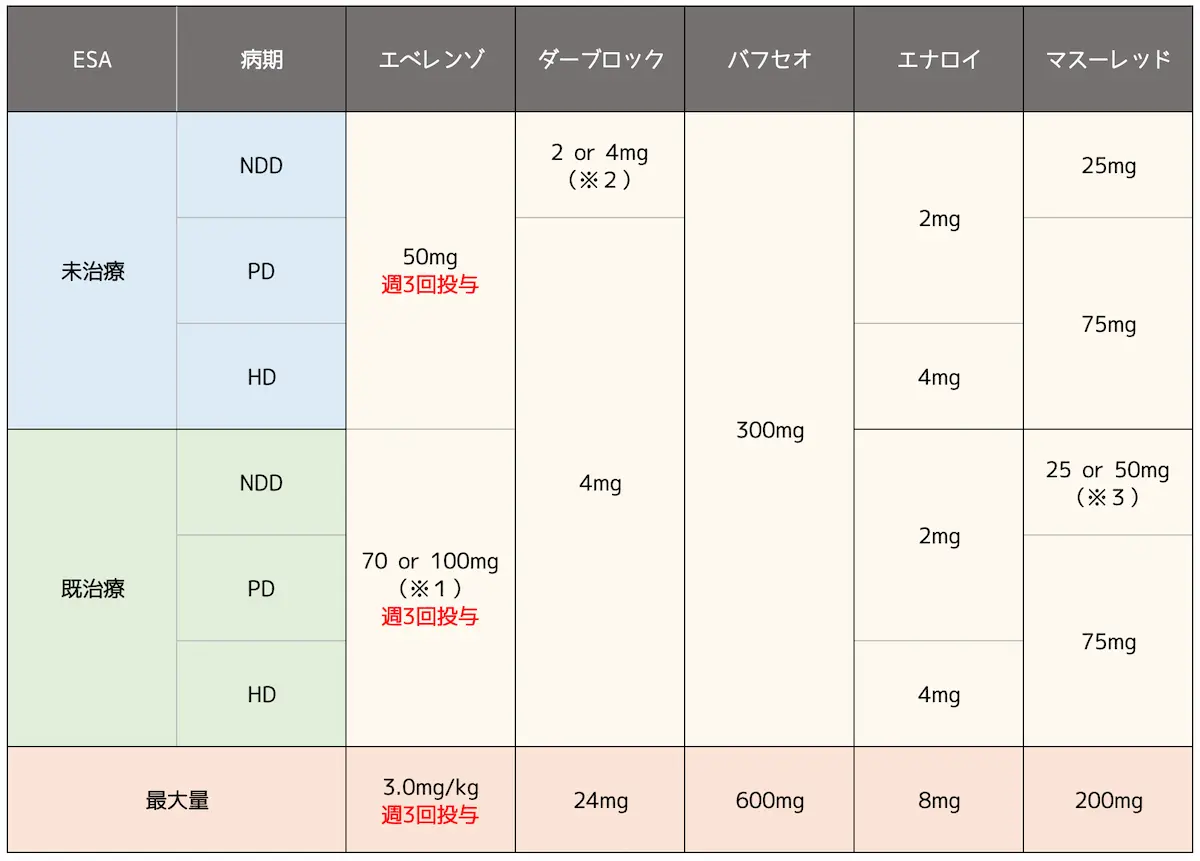
保存期CKDに対して使用可能な他のHIF-PH阻害薬とあわせて用法・用量をまとめてみます。
※2:Hb≧9.0g/dL 2mg、Hb<9.0g/dL 4mg
食事の影響(食後投与が必要)
16.2 吸収
16.2.2 食事の影響
日本人健康男性被験者に本剤50mgを空腹時又は食後に経口投与したとき、食後投与では空腹時投与と比べてAUC(0-∞)及びCmaxはそれぞれ23.3%及び41.1%低下し、tmaxは1時間遅延した。
マスーレッド錠 添付文書 バイエル薬品株式会社
増量・減量に関する注意点
増量・減量の段階について以下のように記載されています。
7. 用法及び用量に関連する注意
7.2 投与量調節が必要な場合には、下表を参考に1段階ずつ投与量を増減すること。
段階 1 2 3 4 5 6 7 8 本剤投与量 5mg 12.5mg 25mg 50mg 75mg 100mg 150mg 200mg 赤血球造血刺激因子製剤で未治療の場合、本剤投与開始4週後は[4週時投与量増減表]を、それ以降は[投与量増減表]を参考に投与量を増減すること。
赤血球造血刺激因子製剤から切り替える場合、[投与量増減表]を参考に投与量を増減すること。なお、増量は原則として4週間以上の間隔をあけて行うこと。休薬した場合は、1段階低い用量で投与を再開すること。
マスーレッド錠 添付文書 バイエル薬品株式会社
| 4週間のHb値上昇 | Hb値 | 用量調節 | |
| 保存期慢性腎臓病患者及び腹膜透析患者 | 血液透析患者 | 1段階増量 | |
| 0.5g/dL未満 | 10.5g/dL未満 | 9.5g/dL未満 | 同じ用量を維持 |
| 10.5g/dL以上 | 9.5g/dL以上 | ||
| 0.5g/dL以上1.0g/dL未満 | すべての値 | ||
| 1.0g/dL以上2.0g/dL以下 | 11.0g/dL以下 | 10.0g/dL以下 | |
| 11.0g/dL超 | 10.0g/dL超 | 1段階減量 | |
| 2.0g/dL超 | すべての値 | ||
| 用量調節 | 1段階増量 | 同じ用量を維持注1) | 1段階減量 | 休薬注2) | |
| Hb値 | 保存期慢性腎臓病患者 及び 腹膜透析患者 | 11.0g/dL未満 | 11.0g/dL以上 12.5g/dL未満 | 12.5g/dL以上 13.0g/dL未満 | 13.0g/dL以上 |
| 血液透析患者 | 10.0g/dL未満 | 10.0g/dL以上 12.0g/dL未満 | 12.0g/dL以上 13.0g/dL未満 | ||
注1):血栓塞栓症(心筋梗塞、肺血栓塞栓症、出血性脳卒中を除く脳卒中、及び急性下肢虚血)の既往のある患者では、Hb値が12g/dLを超えた場合、投与量を1段階減量してもよい。
注2):休薬後の再開の目安は、Hb値が保存期慢性腎臓病患者及び腹膜透析患者で12.5g/dL未満、血液透析患者で12.0g/dL未満になった時点とする。
また、重要な基本的注意には以下の通り、用量に関する注意が記載されています。
8. 重要な基本的注意
8.1 本剤投与開始後、ヘモグロビン濃度が目標範囲で安定するまでは、2週に1回程度ヘモグロビン濃度を確認すること。
8.2 本剤投与中はヘモグロビン濃度等を4週に1回程度確認し、必要以上の造血作用があらわれないように十分注意すること。赤血球造血刺激因子製剤の臨床試験において、ヘモグロビン濃度の目標値を高く設定した場合に、死亡、心血管系障害及び脳卒中の発現頻度が高くなったとの報告がある。
8.3 ヘモグロビン濃度が、4週以内に2.0g/dLを超える等、急激に上昇した場合は速やかに減量又は休薬する等、適切な処置を行うこと。
8.4 赤血球造血刺激因子製剤から本剤への切替え後にヘモグロビン濃度が低下する傾向が認められていることから、切替え後のヘモグロビン濃度の低下に注意すること。
マスーレッド錠 添付文書 バイエル薬品株式会社
Hb値の目標は以下の通りです。
保存期CKD、PD:11g/dL以上13g/dL未満(重篤なCVD合併:12g/dL未満)
HD:10g/dL以上12g/dL未満
この数値を目標に安定するまでは2週間ごとに検査、安定後は4週間ごとに検査する必要があります。
患者背景に関わる注意点
合併症など患者の状態による注意点をまとめます。
鉄剤投与の必要性
8. 重要な基本的注意
8.6 造血には鉄が必要なことから、必要に応じて鉄の補充を行うこと。
マスーレッド錠 添付文書 バイエル薬品株式会社
腎性貧血の治療方法についての部分でも解説しましたが、鉄欠乏により貧血が起きている場合には鉄剤の投与が必要となります。
JSDT腎性貧血ガイドライン2015に記載されている鉄欠乏についての基準を表にまとめておきます。
| 血清フェリチン値 | TSAT | その他 | |
| ESA投与前 | 50ng/mL未満 | – | – |
| ESA投与中 | 100ng/mL未満 | 20%未満 | – |
| 100ng/mL未満 | – | 鉄利用率を低下させる 病態が認められない | |
| – | 20%未満 |
※血清フェリチン値が300ng/mL 以上となる鉄補充療法は推奨しない。
HIF-PH阻害薬投与中の鉄欠乏については、ESA投与中と同様に「フェリチン<100ng/mLまたはTSAT<20%」で判断するべきと考えます。
血栓塞栓症の既往がある患者
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 脳梗塞、心筋梗塞、肺塞栓等の患者、又はそれらの既往歴を有する患者
本剤投与により血栓塞栓症を増悪あるいは誘発するおそれがある。
マスーレッド錠 添付文書 バイエル薬品株式会社
警告にも記載されていたように、造血作用を持つHIF-PH阻害薬(ESA製剤も)では血栓症のリスク増加が知られています。
そのため、脳梗塞、心筋梗塞、肺塞栓等については既往を含めて注意が必要となります。
高血圧を合併する患者
8. 重要な基本的注意
8.5 本剤投与により血圧が上昇するおそれがあるので、血圧の推移に十分注意しながら投与すること。
マスーレッド錠 添付文書 バイエル薬品株式会社
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.2 高血圧症を合併する患者
血圧上昇があらわれるおそれがある。
マスーレッド錠 添付文書 バイエル薬品株式会社
これも、造血作用を持つHIF-PH阻害薬(ESA製剤も)のリスクです。
同じように、過度もしくは急激な造血作用により高血圧が発症、憎悪することが知られています。
そのため、高血圧を合併している場合は注意が必要です。
血管新生によるリスク
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.3 悪性腫瘍を合併する患者
本剤の血管新生亢進作用により悪性腫瘍を増悪させるおそれがある。
9.1.4 増殖糖尿病網膜症、黄斑浮腫、滲出性加齢黄斑変性症、網膜静脈閉塞症等を合併する患者
本剤の血管新生亢進作用により網膜出血があらわれるおそれがある。
マスーレッド錠 添付文書 バイエル薬品株式会社
作用機序の部分で少し触れましたがHIFの活性化はEGFRを増加させ、血管新生を促進します。
そのため、悪性腫瘍や黄斑変性など血管新生が関与する疾患を悪化させてしまう可能性があります。
授乳婦・小児に関する注意
9. 特定の背景を有する患者に関する注意
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。母動物(ラット)への投与で本剤は乳汁中へ移行することが報告されている。
9.7 小児等
本剤では小児等を対象とした有効性及び安全性を指標とした臨床試験は実施していない。
マスーレッド錠 添付文書 バイエル薬品株式会社
授乳についてはラットで乳汁中への移行が認められているようです。
ですが、エナロイ錠のように4日間開けて再開する旨の記載はないですし、出生児の眼瞼開裂時期遅延の報告はないようです。
小児については臨床試験が行われていないため適応外となっています。
相互作用(併用注意のみ)
マスーレッド錠はUDP-グルクロン酸転移酵素(UGT)1A1の基質のため、UGT1A1阻害作用を持つ薬剤と併用することで効果が増強してしまう可能性があります。
また、エナロイ、バフセオ、エベレンゾと同様に多価陽イオンと併用することで効果が減弱する可能性があります。
UGT1A1阻害作用を持つ薬剤(併用注意)
10. 相互作用
10.2 併用注意(併用に注意すること)
薬剤名等:HIVプロテアーゼ阻害剤(アタザナビル、リトナビル、ロピナビル・リトナビル等)、チロシンキナーゼ阻害剤(ソラフェニブ、エルロチニブ、ニロチニブ等)、トラニラスト
臨床症状・措置方法:本剤の作用が増強するおそれがあるため、併用する場合は、本剤の減量を考慮するとともに、患者の状態を慎重に観察すること。
機序・危険因子:本剤をアタザナビルと同時投与したところ、本剤のAUC(0-∞)及びCmaxは上昇した。
UGT1A1阻害により本剤のクリアランスが低下する。
マスーレッド錠 添付文書 バイエル薬品株式会社
参考までに、UGT1A1を阻害する薬剤を列挙しておきます。
(相互作用として未記載のものも含めて)
- HIVプロテアーゼ阻害剤
- アタザナビル(レイアタッツ)
- リトナビル(ノービア)
- ロピナビル・リトナビル(カレトラ)
- チロシンキナーゼ阻害剤
- ソラフェニブ(ネクサバール)
- エルロチニブ(タルセバ)
- ニロチニブ(タシグナ)
- トラニラスト(リザベン)
- バルプロ酸(デパケン、セレニカ、バレリン)※添付文書未記載
16.7 薬物相互作用
16.7.1 アタザナビル
健康男性被験者にアタザナビル400mgを食後に反復投与した後、本剤25mgを食後に単回併用投与したときのモリデュスタットの薬物動態に及ぼす影響は下表のとおりである(外国人データ)。
併用薬 併用薬
投与量本剤
投与量例数 幾何平均値の比[90%信頼区間]
(アタザナビル併用投与時/本剤単独投与時)Cmax AUC(0-∞) アタザナビル 400mg 25mg 13 2.07
[1.53、2.79]2.07
[1.87、2.29]マスーレッド錠 添付文書 バイエル薬品株式会社
レイアタッツ400mg/日(アタザナビル)を併用した場合、AUC(0-∞)及びCmaxは約2倍になっていますね。
多価陽イオン(併用注意)
10. 相互作用
10.2 併用注意(併用に注意すること)
薬剤名等:多価陽イオン(カルシウム、鉄、マグネシウム、アルミニウム等)を含有する経口製剤
臨床症状・措置方法:本剤の吸収が低下し、効果が減弱するおそれがあるため、併用する場合は、前後1時間以上間隔をあけて本剤を投与すること。
機序・危険因子:本剤を硫酸鉄と同時投与したところ、本剤のAUC(0-∞)及びCmaxは低下した。
本剤の消化管からの吸収が減少し、血中濃度が低下する。
マスーレッド錠 添付文書 バイエル薬品株式会社
16.7 薬物相互作用 > 16.7.2 経口鉄剤 に鉄剤併用タイミングによるAUC(0-∞)及びCmaxの影響が記載されていますが、影響を軽減させるためには前後2時間程度の間隔を空けたいところですね。
副作用は非常に少ないが・・・
副作用は非常に少なくシンプルに記載されています。
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
11.1.1 血栓塞栓症(0.3%)
脳梗塞(0.3%)、心筋梗塞(頻度不明)、シャント閉塞(頻度不明)等の血栓塞栓症があらわれることがある。
11.1.2 間質性肺疾患(0.5%)
初期症状(呼吸困難、咳嗽、発熱等)が認められた場合には、胸部CT、血清マーカー等の検査を実施すること。間質性肺疾患が疑われた場合には投与を中止し、適切な処置を行うこと。
11.2 その他の副作用
代謝および栄養障害:鉄欠乏(1%以上)
神経系障害:めまい(浮動性、回転性)(1%未満)
眼障害:眼出血、糖尿病網膜症(1%未満)
心臓障害:心のう液貯留(1%未満)
血管障害:高血圧(1%未満)
胃腸障害:便秘、下痢、悪心、嘔吐、腹痛(1%未満)
皮膚及び皮下組織障害:発疹、そう痒症(1%未満)
一般・全身障害および投与部位の状態:浮腫(1%未満)
マスーレッド錠 添付文書 バイエル薬品株式会社
血栓塞栓症はHIF-PH阻害薬に共通のリスクなので、起こさないためにはHb値を定期的に検査し、高値にならないように、急激に上昇させないように用量の調節を行うことが大切になります。
気になるのは間質性肺疾患です。
他のHIF-PH阻害薬には見られないため、マスーレッド特有のものになりますが、頻度も0.5%と低くないので注意が必要ですね。
RMPに記載されている注意点
- 重要な特定されたリスク
- 血栓塞栓症
- 高血圧
- 重要な潜在的リスク
- 心血管系事象(血栓塞栓症を除く)
- 間質性肺疾患
- 悪性腫瘍
- 網膜出血
- 常染色体優性多発性嚢胞腎(ADPKD)患者における病態の進行
間質性肺疾患については他のHIF-PH阻害薬には記載されていないマスーレッド特有のリスクになります。
血栓塞栓症(重要な特定されたリスク)
海外でのESAの臨床試験で、Hb濃度の目標値を高く設定した場合、心血管系障害や脳卒中等の血栓塞栓症の発現頻度が上昇したという報告があります。
マスーレッド錠については、国内第III相臨床試験の実薬対照3試験(試験 19349、19350、19352)の併合解析データにおいて、ダルベポエチンアルファ群と比較して血栓塞栓症関連の有害事象の発現割合が高い傾向が認められています。
HIF-PH阻害薬の投与で発生する有害事象というよりはHb濃度の過剰に高くしてしまった際に生じる有害事象と思っていましたが、マスーレッドについてはダルベポエチンアルファ投与よりもリスクが高くなる可能性があります。
いずれにしても、目標Hb値を超してしまわないような管理が血栓塞栓症の回避につながります。
- 保存期CKD、PD:11g/dL以上13g/dL未満(重篤なCVD合併:12g/dL未満)
- HD:10g/dL以上12g/dL未満
高血圧(重要な特定されたリスク)
腎性貧血の改善に伴い高血圧が発症することが知られています。
「慢性腎臓病患者における腎性貧血治療のガイドライン2015年版(日本透析医学会編)」でその原因は以下の通り記載されています。
- 貧血改善に伴う組織低酸素濃度 の是正から拡張していた末梢血管が収縮すること
- 血液粘度の亢進などによる末梢血管 抵抗の増加に対する心拍出量の反応性低下の欠如ないしは不十分であること
そのためマスーレッド錠でも高血圧が生じる可能性は高いと考えられます。
国内第III相臨床試験の実薬対照 3 試験の併合解析データにおいて、高血圧関連の有害事象はマスーレッド群、ダルベポエチンアルファ群で同程度でした。
心血管系事象(血栓塞栓症を除く)(重要な潜在的リスク)
血栓塞栓症と同じく、海外でのESAの臨床試験で、Hb濃度の目標値を高く設定した場合、心血管系障害や脳卒中等の血栓塞栓症の発現頻度が上昇したという報告に基づいています。
また、国内第III相臨床試験の実薬対照3試験の併合解析データにおいて、MACE※の発現割合はマスーレッド群においてダルベポエチンアルファ群よりも高い傾向が認められたものの、MACEリスクファクター(収縮期血圧、eGFR、CRP、糖尿病性腎症)の患者背景の偏りが影響した可能性は否 定できないと考えられた。
※Major Adverse Cardiovascular Events:心血管死又は原因不明の死亡、心筋梗塞、不安定狭心症、虚血性脳卒中(虚血性脳卒中、又は梗塞後の出血性変化を伴う虚血性脳卒中)、肺血栓塞栓症、急性下肢虚血と定義
間質性肺疾患(重要な潜在的リスク)
国内第III相臨床試験の保存期慢性腎臓病患者を対象とした試験におい て、重篤な間質性肺疾患が2例に認められ、いずれもマスーレッドとの因果関係が否定されなかったものの、合併症、併発事象や併用薬の関与も考えられた。
間質性肺疾患は重大な転帰につながる恐れがあること、また、マスーレッド投与による間質性肺疾患の発現はまだ十分に集積されていないことから、重要な潜在的リスクに設定されました。
網膜出血(重要な潜在的リスク)
HIF安定化によりVGEFの産生が誘導されることが知られています。
VGEFは血管新生や血管透過性を亢進させるため、加齢黄斑変性等の網膜及び脈絡膜で生じる眼疾患の主要な原因因子となります。
国内第I相臨床試験の高用量単回投与時にVEGFの上昇が報告されています。
ですが、第III相臨床試験の既存薬との比較試験において、マスーレッド群とダルベポエチンアルファ群の間で投与後に眼底検査の判定が「正常」から「異常」に変動した被験者の割合に大きな違いは認められなかったようです。
悪性腫瘍(重要な潜在的リスク)
網膜出血と同じく、HIF安定化によるVGEFの産生が悪性腫瘍のリスクとなります。
VEGFは悪性腫瘍の増殖に必要な血管新生の促進因子として知られており、複数の癌でVEGFの産生誘導が予後に悪影響を及ぼすことが知られています。
国内の臨床試験では悪性腫瘍の報告はありましたが、悪性腫瘍を発現した各被験者の悪性腫瘍の発現日までのマスーレッドの曝露期間が比較的短期間(10~270日)であったこと、非臨床試験では、マウス及びラットへ2年間経口投与した結果、がん原性は認められなかったため、重要な潜在的リスクとして設定されました。
常染色体優性多発性嚢胞腎(ADPKD)患者における病態の進行(重要な潜在的リスク)
ADPKDにおいて、嚢胞が大きくなることでネフロンや腎臓内の血管が圧迫され、局所の低酸素が引き起こされ、その結果、嚢胞形成細胞においてHIF-1αが増加すると言われています。
多発性嚢胞腎のモデルマウスにPH阻害薬を投与すると嚢胞が増悪することが報告されています。
ADPKD合併症例に対するマスーレッドの影響は十分に検討されていないため重要な潜在的リスクに設定されています。
まとめ
マスーレッド錠の特徴をまとめます。
まずはHIF-PH阻害薬としての特徴と注意点です。
- 経口投与で腎性貧血に効果を発揮
- 内因性EPO増加
- 鉄吸収促進
- 高ヘプシジン血症の改善効果
- ESA抵抗性(EPO抵抗性)貧血に対しても効果?
- 急激なHb上昇や高Hb値での血栓塞栓症に注意
- 貧血改善による高血圧に注意
- 増量間隔は4週間以上
- 定期的な検査が必要
- 用量調節期:2週間ごと
- 目標Hb濃度達成後:4週間ごと
- Hb濃度高値や急上昇は血栓塞栓症や高血圧のリスク
- 急激なHb濃度上昇:4週間以内に2.0g/dL超の上昇)
- Hb濃度は13g/dL未満(HD:12g/dL未満)
つづいてマスーレッド錠の特徴です。
- 妊娠中は禁忌
- 妊娠可能な年齢の女性は避妊が必要
- 患者のHb値に応じた細かな用量調節が可能
- 食後服用が必要
- 保存期の場合はESA製剤の治療歴で開始用量が異なる
- 保存期CKD(ESA未治療):25mg開始
- 保存期CKD(ESA既治療):25mgまたは50mg開始(ESA製剤の投与量による)
- 透析期:75mg開始
- 用量は8段階で5mg〜200mg
- 多価陽イオンを併用する場合は投与間隔をあける必要
- 間質性肺炎に注意
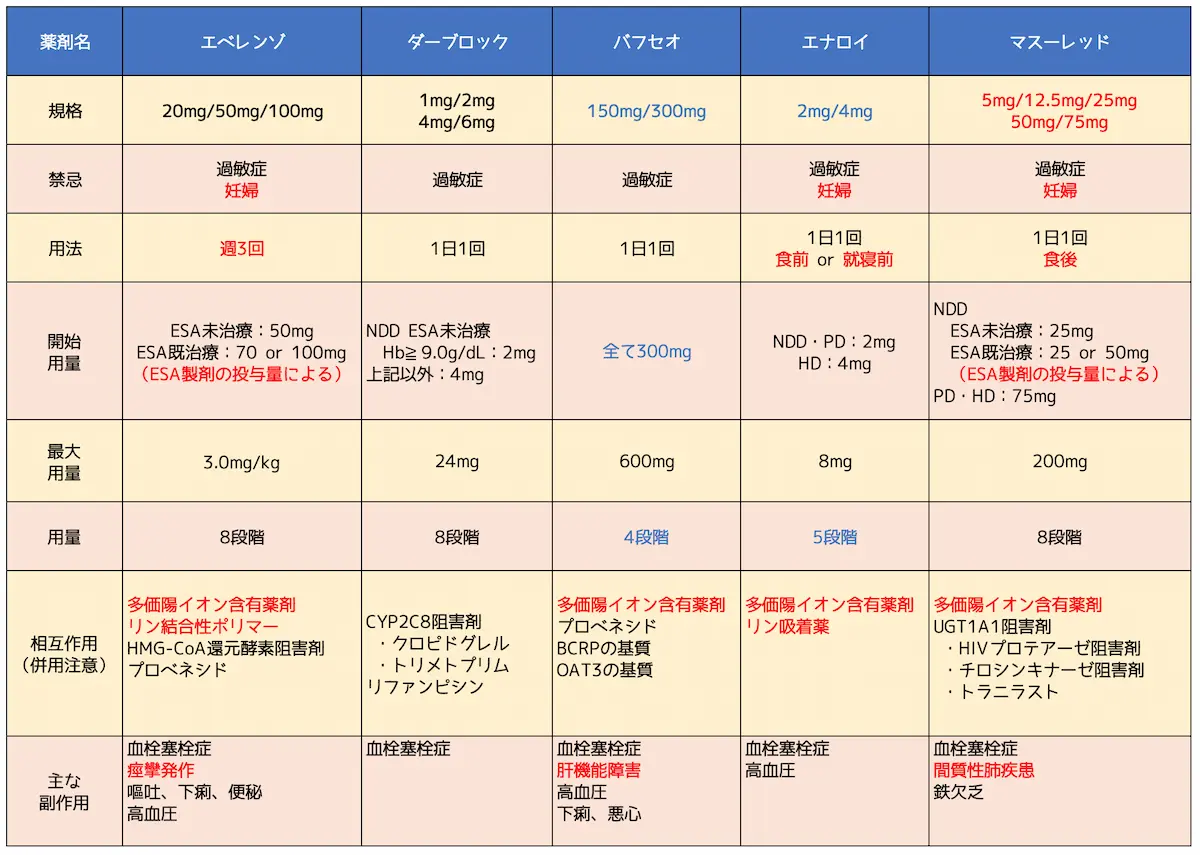
HIF-PH阻害薬の比較
2021.3.10時点の情報でHIF-PH阻害薬を比較したものを表にまとめました。
HIF-PH阻害薬適正使用に関するrecommendation
2020年9月29日付で日本腎臓学会から「HIF-PH阻害薬適正使用に関するrecommendation」が公開されました。
日本腎臓学会 HIF-PH阻害薬適正使用に関するrecommendation 2020年9月29日版
- HIF-PH 阻害薬総論
- 治療に関する推奨
- 注意点
の3つにわけて記載されています。
このうち、推奨の部分について簡単にまとめてみます。
どのような患者に使用することが望ましいか(ESAからの切り替えも含め)
- ESAとHIF-PH阻害薬の選択は、個々の患者の状態や嗜好、通院頻度、ポリファーマシーや服薬アドヒアランス等に応じて、医師が判断
- HIF-PH阻害薬を使用する際は、事前に悪性腫瘍、網膜病変の検査を行い、合併がないか、適切な治療がなされているかを確認した上で開始
- 虚血性心疾患、 脳血管障害や末梢血管病のある患者については、そのリスクを評価した上で適応の可否を慎重に判断
- ESA抵抗性の原因が不明もしくは対応が困難な場合(鉄利用障害など)には、HIF-PH阻害薬への変更を考慮
- 高用量のESAからの切り替え直後にHb値の低下が認められることがあり、Hb値の推移を十分に観察してHIF-PH阻害薬の用量を調節するべき
- ESAとHIF-PH阻害薬の併用は想定されておらず、行うべきではない
鉄補充をどうすることが望ましいか
- フェリチン<100ng/mLまたはTSAT<20%をHIF-PH阻害薬使用中の鉄補充のカットオフに設定することが妥当
- 目標ヘモグロビンに到達しない場合、HIF-PH阻害薬の増量よりも鉄欠乏状体を評価した上で鉄補充を優先
- HIF-PH 阻害薬開始時に急激に造血が亢進することで、TSATやフェリチンが著しく低下する症例があるため、薬剤開始1か月後には、再度これらのマーカーを評価し、鉄欠乏があれば鉄を補充
- HIF-PH阻害薬投与中は、消化管からの鉄の吸収が改善するために経口鉄の効果が従来よりも期待できる
- クエン酸第二鉄やスクロオキシ水酸化鉄などの鉄含有リン吸着薬によっても鉄が補充されることを考慮
所感
個人的に考えたところをまとめます。
保存期CKDに使用できるHIF-PH阻害薬が登場したことの意義
これまで腎性貧血の治療にはESA製剤の投与のため注射が必要でした。
透析期の場合は透析時にESA投与を行うことができますが、保存期CKDや腹膜透析では注射を行う必要があります。
それが嫌でなかなか治療を開始できない患者さんもいますし、定期的な注射が苦痛でQOL低下に繋がっている患者さんも少なくないため、経口投与可能なHIF-PH阻害薬は患者さんにとって大きな選択肢になります。
また、ESA投与でなかなか症状が改善しないESA抵抗性の腎性貧血に対してHIF-PH阻害薬が効果を発揮する可能性があります。
経口投与が可能な薬剤ということで投与しやすくなる一方、腎性貧血はHb濃度の管理に注意が必要な疾患です。
急激なHb濃度上昇や高値になることを防ぎつつ治療を行なっていく必要があるため、ESA投与と同じく定期的にHb濃度を測定して管理を行なっていく必要があります。
ESA製剤は薬局で調剤する機会はありませんでしたが、HIF-PH阻害薬の登場により薬局も腎性貧血に深く関わっていくことになります。
しっかりと対応できるように勉強しておきたいですね。
参考資料
- マスーレッド錠 添付文書 バイエル薬品株式会社
- マスーレッド錠 インタビューフォーム バイエル薬品株式会社
- マスーレッド錠に係る医薬品リスク管理計画書 バイエル薬品株式会社
- マスーレッド錠 審議結果報告書 医薬・生活衛生局医薬品審査管理課
- 日本腎臓学会編.CKD 診療ガイド 2012,東京医学社, 2012.
- 日本腎臓学会編.エビデンスに基づくCKD 診療ガイドライン 2018,東京医学社, 2018.
- 日本透析医学会:2015年版慢性血液透析患者における腎性貧血治療のガイドライン.透析会誌49:89-158,2016.(2015 JSDT Guideline for Renal Anemia in Chronic Kidney Disease)
- KDIGO 2012 clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int 2013;Suppl 3:1‒150.
- 日本透析医学会雑誌 49 巻 2 号 2016
- Kraus A, et al. HIF-1α promotes cyst progression in a mouse model of autosomal dominant polycystic kidney disease. Kidney International. 2018;94:887-899.
- Hofherr A, et al. HIF-1α drives cyst growth in advanced stages of autosomal dominant polycystic kidney disease. Kidney International. 2018;94:849-851.
- Mohanram A, Zhang Z, Shahinfar S, Keane WF, Brenner BM, Toto RD. Anemia and end-stage renal disease in patients with type 2 diabetes and nephropathy. Kidney Int 2004;66:1131.(RENAAL試験)
- Drüeke TB,Locatelli F,Clyne N,Eckardt KU,Macdougall IC,Tsakiris D,Burger HU,Scherhag ;CREATE Investigators. Normalization of hemoglobin level in patients with chronic kidney disease and anemia. N Engl J Med2006;355:2071-2084.(CREATE 研究)
- Singh AK,Szczech L,Tang KL,Barnhart H,Sapp S,Wolfson M,Reddan D;CHOIR Investigators. Correction of anemia with epoetin alfa in chronic kidney disease. N Engl J Med 2006;355:2085- 2098.(CHOIR研究)
- 日本腎臓学会 HIF-PH阻害薬適正使用に関するrecommendation 2020年9月29日版
- エベレンゾ錠 添付文書 アステラス製薬株式会社
- ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
- バフセオ錠 添付文書 グラクソ・スミスクライン株式会社
- エナロイ錠 添付文書 日本たばこ産業株式会社
*1:HIF-Prolyl Hydroxylase Inhibitor
*2:ErythroPOietin
*3:Erythropoiesis Stimulating Agent
*4:HIF-Prolyl Hydroxylase
*5:Chronic Kidney Disease
*6:End-Stage Kidney Disease
*7:CardioVascular Disease
*8:HemoDialysis
*9:Peritoneal Dialysis
*10:Non-Dialysis
*11:aryl hydrocarbon receptor nuclear translocator
*12:Prolyl HyDroxylas
*13:Divalent Metal Transporter 1
*14:Duodenal cytochrome b
*15:Pure Red Cell Aplasia
*16:Major Adverse Cardiovascular Events