2020年6月29日に承認された腎性貧血を適応とするダーブロック錠(成分名:ダプロデュスタット)についてまとめた記事です。
ダーブロック錠はHIF-PH阻害薬と呼ばれる薬剤で、内因性エリスロポエチンの増加作用等により腎性貧血を改善する薬剤です。
これまで腎性貧血にはネスプ(成分名:ダルベポエチン アルファ)やミルセラ(成分名:エポエチン ベータ ペゴル)などのESA製剤が使用されてきましたが、HIF-PH阻害薬はそれに代わる薬剤(ポストネスプとも呼ばれます)として期待されています。
ダーブロックについて
まずはダーブロック錠の承認の背景について簡単にまとめます。
ダーブロック錠(ダプロデュスタット)は腎性貧血に対する適応を有するHIF-PH阻害薬(HIF-PHI*1)と呼ばれる薬剤です。
腎性貧血は腎機能の低下に伴いエリスロポエチン(EPO*2)の産生が低下することによって生じる貧血です。
これまでは腎性貧血の治療にはEPOの補給を行うためにネスプ(成分名:ダルベポエチン アルファ)やミルセラ(成分名:エポエチン ベータ ペゴル)などの赤血球造血刺激因子製剤(ESA*3製剤)が投与されてきました。
それに対してHIF-PH阻害薬は、HIFプロリン水酸化酵素(HIF-PH*4)を阻害することで、HIF経路を活性化させ、内因性EPOの産生を増やし、腎性貧血を改善する薬剤です。(このメカニズムの解明は2019年のノーベル医学・生理学賞を受賞しています)
その作用機序からHIF-PH阻害薬、HIF安定化薬、HIF活性化薬と呼ばれています。
これまで腎性貧血に対して使用されてきたESA製剤とは異なり、経口投与の薬剤のため透析を行っていない(透析と同時にESA製剤を投与できない)保存期CKDの患者さんのQOL改善が期待されていますが、唯一のHIF-PH阻害薬だったエベレンゾの適応は透析期の腎性貧血のみでした。(2020年11月27日に「透析施行中の腎性貧血」→「腎性貧血」に適応拡大)
ダーブロック(と同時に承認されたバフセオ)は保存期CKDの腎性貧血にも使用可能な初のHIF-PH阻害薬でHIF-PH阻害薬の大本命です。この記事ではダーブロックの特性や注意点などについて詳しく解説します。
ダーブロックの基本情報
基本情報をまとめます。
| 医薬品名 | ダーブロック錠1mg ダーブロック錠2mg ダーブロック錠4mg ダーブロック錠6mg |
|---|---|
| 開発コード | GSK1278863A |
| 成分名 | ダプロデュスタット |
| 英語名 | Duvroq(Daprodustat) |
| 製造販売元 | グラクソ・スミスクライン株式会社 |
| 販売元 | 協和キリン株式会社 |
| 命名の由来 | 特になし |
| 効能・効果 | 腎性貧血 |
| 用法・用量 | 保存期慢性腎臓病患者 赤血球造血刺激因子製剤で未治療の場合 通常、成人にはダプロデュスタットとして1回2mg又は4mgを開始用量とし、1日1回経口投与する。 以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1日1回24mg までとする。 赤血球造血刺激因子製剤から切り替える場合 通常、成人にはダプロデュスタットとして1回4mgを開始用量とし、1 日 1 回経口投与する。 以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1日1回24mg までとする。 透析患者 通常、成人にはダプロデュスタットとして1回4mgを開始用量とし、1日1回経口投与する。 以後は、 患者の状態に応じて投与量を適宜増減するが、最高用量は1日1回24mg までとする。 |
| 指定等 | なし |
| 審議 | 2020年5月29日付 薬食審第一部会 (web審議) |
| 承認日 | 2020年6月29日 |
| 薬価収載日 収載時薬価 | 2020年8月26日 ダーブロック錠1mg:105.40円/錠 ダーブロック錠2mg:185.80円/錠 ダーブロック錠4mg:327.40円/錠 ダーブロック錠6mg:456.10円/錠 |
| 薬価算定方式 | 類似薬効比較方式(Ⅰ) エベレンゾ錠100mg(薬価:1,399.00円/錠)の1日薬価457.00円を元にダーブロック錠6mgの薬価456.10円/錠(1日薬価457.00円)を算出 エベレンゾ錠100mgとエベレンゾ錠50mgの規格間比:0.8174を元に1mgと2mgと4mgの薬価を算出 |
| 販売開始 | 2020年8月26日(薬価収載即日発売) |
| 新医薬品の 投与日数制限 | 対象(2021年8月末日まで) |
腎性貧血とダーブロックの作用機序
まず、腎性貧血について簡単に説明してからダーブロックの作用機序について説明していきます。
腎性貧血とは?
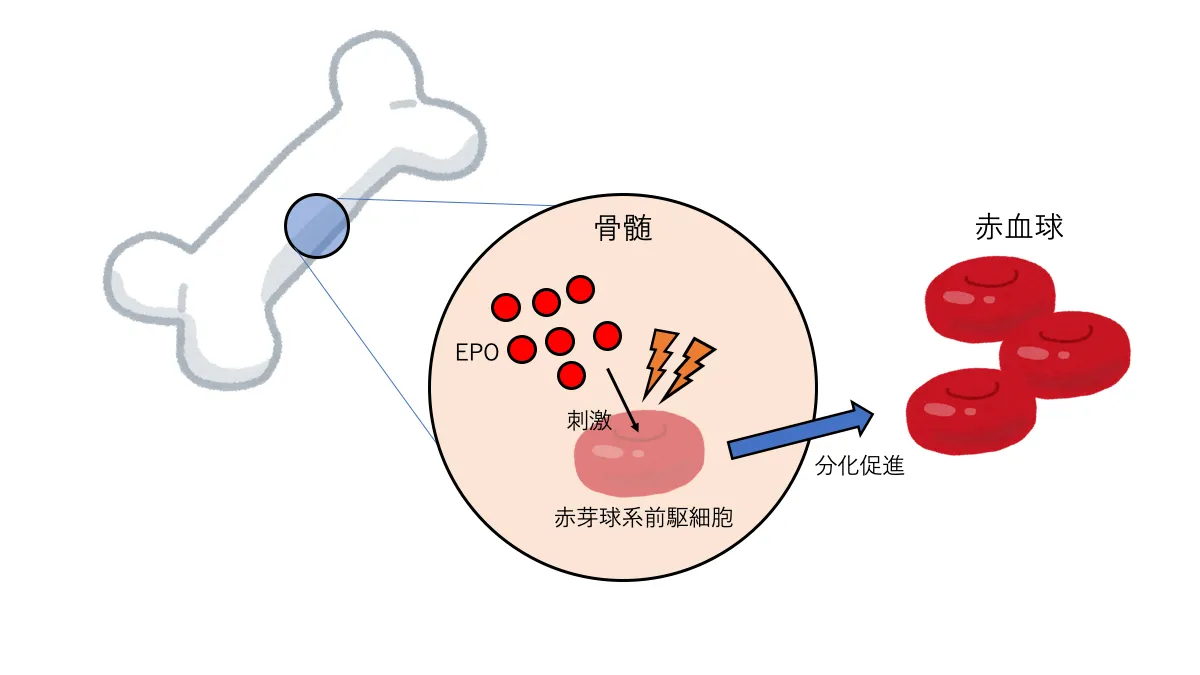
腎性貧血とは慢性腎臓病(CKD*5)の進行に伴い生じる貧血で、その主な原因は腎臓でエリスロポエチン(EPO)が十分に産生されなくなることです。EPOは赤血球の産生を促進する造血因子の一つで、骨髄中の赤芽球系前駆細胞を刺激し、赤血球への分化と増殖を促進します。
CKDの基礎とeGFR
日本でのCKD患者数は1,330万人(成人の8人に1人)と考えられており、新たな国民病の一つと言われています。CKDの原因は多岐に渡りますが、腎炎などの腎疾患だけでなく、自己免疫疾患、加齢、生活習慣病(糖尿病、高血圧など)、薬の副作用など様々なものがあります。
その定義は「腎臓の構造または機能の異常が3カ月を超える場合」とされています。
・eGFR※2 < 60ml/分/1.73㎡
※1:タンパク尿 ≧ 0.15g/gCr(アルブミン尿 ≧ 30mg/gCr)
※2:eGFR(ml/分/1.73㎡) = 194×Cr-1.094×年齢(歳)-0.287(女性は×0.739)
CKDが進行することで末期腎不全(ESKD*6)となり透析や腎移植が必要となってしまいます。
ですが、CKD患者ではESDKに移行するリスクよりも死亡リスクの方が高くなっており、その多くが心血管疾患(CVD*7)による死亡です。
そのため、CKDではCVDによる死亡を回避するために、腎機能だけでなく新血管リスクまでを考慮していくことが重要となります。(もう少し後で心腎貧血症候群という概念を説明します)
CKDの重症度は、原疾患(Cause)、腎機能(GFR)、蛋白尿・アルブミン尿(Albuminuria)の頭文字をとったCGA分類で評価しますが、腎性貧血においては以下の表に示すeGFRによるステージ分類が目安となります。
| CKDステージ | 1 | 2 | 3 | 4 | 5 |
| eGFR値 | 90以上 | 60〜89 | 30〜59 | 15〜29 | 15未満 |
| 腎臓病の程度 | 正常 | CKD | ESKD | ||
| 軽度低下 | 中程度低下 | 高度低下 | |||
| 治療法 | 予防 | 食生活の改善・薬物療法 | 透析・腎移植 | ||
腎性貧血の発症機序
腎性貧血は「腎臓においてヘモグロビン(Hb)の低下に見合った十分量のエリスロポエチン(EPO)が産生されないことによって引き起こされる貧血であり、貧血の主因が腎障害(CKD)以外に求められないもの」と定義されています。CKDステージ3以降に腎性貧血の頻度が増加しますが、合併症などによっては早期から貧血を起こす場合もあります。
日本人における腎性貧血の診断基準値は以下のようになっています。
| 性別 | 60歳未満 | 60歳以上 70歳未満 | 70歳以上 |
| 男性 | Hb<13.5g/dL | Hb<12.0g/dL | Hb<11.0g/dL |
| 女性 | Hb<11.5g/dL | Hb<10.5g/dL | Hb<10.5g/dL |
腎性貧血の原因は主にEPOの産生不足とされていますが、他にも様々な原因が考えられます。
- 赤血球の造血抑制
- EPO産生不足
- 尿毒症性毒素による造血抑制
- 高サイトカイン血症によるEPO感受性低下
- 赤血球寿命の短縮(尿毒素)
- 鉄代謝の障害(高ヘプシジン血症)
- 透析回路における残血、出血
- 栄養障害(ビタミン、葉酸など)
JSDT腎性貧血ガイドライン2015
貧血は心不全を悪化させる原因となり、腎性貧血が進行するほど末期腎不全への移行や死亡率が上昇します。(RENAAL試験のサブ解析)貧血による虚血や酸化ストレスが体液貯留や炎症を引き起こすことで、心臓病や腎臓病の病態悪化に関与すると考えられており、心腎貧血症候群という概念として提唱されています。
腎性貧血の治療
腎性貧血と診断されたからと言って、必ずしもすぐに治療が必要となるわけではなく、治療開始は個々の状態によって判断されます。特に腎性貧血においては健常者と同等のHb=13g/dl以上を目指した場合、有害事象が増え、予後が改善されないことが明らかになっています。(CREATE 研究、CHOIR研究)
そのためガイドラインでは、HD*8(血液透析)・PD*9(腹膜透析)・ND*10(保存期CKD)それぞれの場合において、死亡リスクの上昇、QOL低下のエビデンスを元に開始基準となるHb値と共に目標Hb値が定められています。
第 2 章 腎性貧血治療の目標Hb値と開始基準
CQ1.腎性貧血治療において維持すべき目標 Hb 値と開始基準は何か?
ステートメント 1
- 成人の血液透析(HD)患者の場合,維持すべき目標Hb値は週初めの採血で10g/dL以上12g/dL未満とし,複数回の検査でHb値10g/dL未満となった時点で腎性貧血治療を開始することを推奨する.(1C)
- 成人の保存期慢性腎臓病(CKD)患者の場合,維持すべき目標Hb値は11g/dL以上13g/dL未満とし,複数回の検査でHb値11g/dL未満となった時点で腎性貧血治療を開始することを提案する.(2C)
ただし,重篤な心・血管系疾患(CVD)の既往や合併のある患者,あるいは医学的に必要のある患者にはHb値12g/dLを超える場合に減量・休薬を考慮する.(not graded)- 成人の腹膜透析(PD)患者の場合,維持すべき目標Hb値は11g/dL以上13g/dL未満とし,複数回の検査でHb値11g/dL未満となった時点で腎性貧血治療を開始することを提案する.(2D)
PD患者のESA投与方法は,基本的に保存期CKD患者に準じて考えることが望ましい.(not graded)- HD,PD,保存期CKD患者のいずれにおいても,実際の診療においては個々の症例の病態に応じ,上記数値を参考として目標Hb値を定め治療することを推奨する.(1C)
慢性腎臓病患者における腎性貧血治療のガイドライン2015
HDを受けている場合、日本では週初め(月曜日or火曜日:中2日)の透析前に採血する施設がほとんどです。
その場合、循環血が除水を受ける直前なので、Hb値が最も低い(Hb濃度が薄い)状態での数値になるため、HDの場合のHb値はPD、NDの場合よりも低くなっています。
鉄補充療法を選択する場合
JSDT腎性貧血ガイドライン2015では、それまでESA投与が基本とされていた腎性貧血の治療が「ESA投与」と「鉄補充療法」のいずれか適切な方法で行うように変更されました。
当然ですが、鉄欠乏の状態だといくらEPOによる刺激があっても正常な赤血球が増加できないので貧血は改善しません。その場合は鉄欠乏の治療を行う、もしくは鉄補給と同時にESA投与(HIF-PH阻害薬の投与)が必要となります。
参考までに鉄補充療法を選択する場合についてJSDT腎性貧血ガイドライン2015では以下のように記載されています。
第 4 章 鉄の評価と補充療法
CQ2:鉄の評価はどのような方法が推奨されるか?
ステートメント 2
- 貧血を合併するCKD患者は鉄欠乏・鉄過剰となることがあるため定期的な鉄評価を行う(鉄投与中は月1回,非投与時には3か月に1回程度).(not graded)
- 鉄評価には血清フェリチン値,TSATを用いることを推奨する.(1C)
CQ3:鉄剤の投与・中止基準は何か?
ステートメント 3-1
- ESA製剤も鉄剤も投与されておらず目標Hb値が維持できない患者において,血清フェリチン値が50ng/mL未満の場合,ESA投与に先行した鉄補充療法を提案する.(2D)
- ESA投与下で目標Hb値が維持できない患者において,血清フェリチン値が100ng/mL未満かつTSATが20%未満の場合,鉄補充療法を推奨する.(1B)
ステートメント 3-2※
- ESA投与下で目標Hb値が維持できない患者において,以下の両者を満たす場合には鉄補充療法を提案する.(2C)
- 鉄利用率を低下させる病態が認められない場合
- 血清フェリチン値が100ng/mL未満またはTSATが20%未満の場合
- 血清フェリチン値が300ng/mL以上となる鉄補充療法は推奨しない.(2D)
※このステートメントは,作成ワーキンググループ会議にて全会一致ではなく2/3以上の合意をもって採択された 唯一の記載である.したがって,この内容に関してはまだ議論が多く残されていると考えている.
慢性腎臓病患者における腎性貧血治療のガイドライン2015
HIF-PH阻害薬の作用機序
いよいよここからはダーブロックの作用機序についてまとめていきたいと思います。
ダーブロックの有効成分ダプロデュスタットはPHDを阻害することでHIF経路を活性化(HIF-PH阻害薬)し、腎性貧血に対して効果を発揮します。
中心となるのはエリスロポエチン(EPO)産生促進ですが、HIFの活性化による様々な作用により腎性貧血を改善します。
- EPO産生促進
- 腸管の鉄吸収促進に関わる遺伝子の転写促進
- トランスフェリン・トランスフェリン受容体遺伝子の転写促進
- ヘプシジンの産生・放出の抑制
腎性貧血の治療で従来使用されてきたESA製剤に置き換わる薬剤となります。
HIF経路によるエリスロポエチン産生
HIF-PH阻害薬によるEPO産生促進のメカニズムを知るために、まずは腎臓でHIFがどのように働いてEPOが産生されるかについて解説します。
エリスロポエチンは主に腎臓の近位尿細管周辺の間質に存在する繊維芽細胞様細胞(EPO産生細胞)で生成されます。貧血により腎血流量が低下し、酸素供給が低下した結果、EPO産生細胞の酸素分圧が低下します。この酸素分圧の低下に呼応してEPOの産生が高まるのですが、そこで中心的な役割を果たすのが低酸素誘導因子(HIF)です。
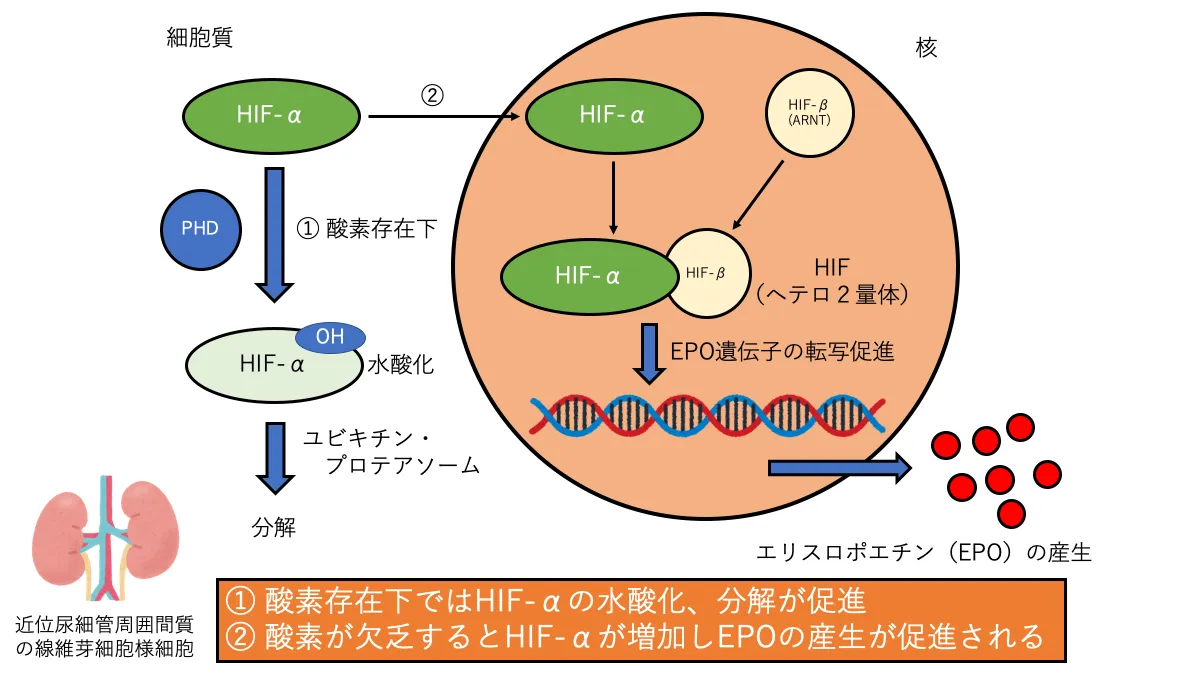
HIFはαサブユニット(HIFα)とβサブユニット(HIFβ、ARNT*11)からなる2量体の転写因子です。
HIFはEPO遺伝子の転写を促進する働きを持っています。
※HIFにはHIF1、HIF2、HIF3が存在し、それぞれのαサブユニットとしてHIF1α、HIF2α、HIF3αが存在しますが、この記事の中では特に区別していません。
HIFαは細胞質に存在し、核内でHIFβと結合して2量体(HIF)となり、EPO遺伝子の転写を促進します。
細胞質にはHIFαのプロリンを水酸化するプロリン水酸化酵素(PHD*12)が存在しています。
PHDはHIFαのプロリンを水酸化し、プロリンが水酸化されたHIFαは細胞質内のユビキチン・プロテアソームにより分解されてしまいます。
PHDは酸素存在化で活性化される酵素です。そのため、貧血によりEPO産生細胞の酸素分圧が低下(酸素が不足)するとEPOの産生量が増加して貧血が改善されます。
このように、HIF経路によるEPO産生ではPHDが酸素センサーの役割を果たし、EPOの産生量を調整しています。
腎障害時のHIF経路
ですが、腎障害時にはHIF経路がうまく機能してくれません。正常な腎臓では尿細管でのNa再吸収が活発に行われることで酸素が消費されています。そのため、酸素供給が低下すると、酸素消費と酸素供給のバランスが崩れて酸素分圧が低下(酸素が不足)します。酸素がない環境ではPHDが抑制されるため、HIFが活性化しEPOの産生が増加します。
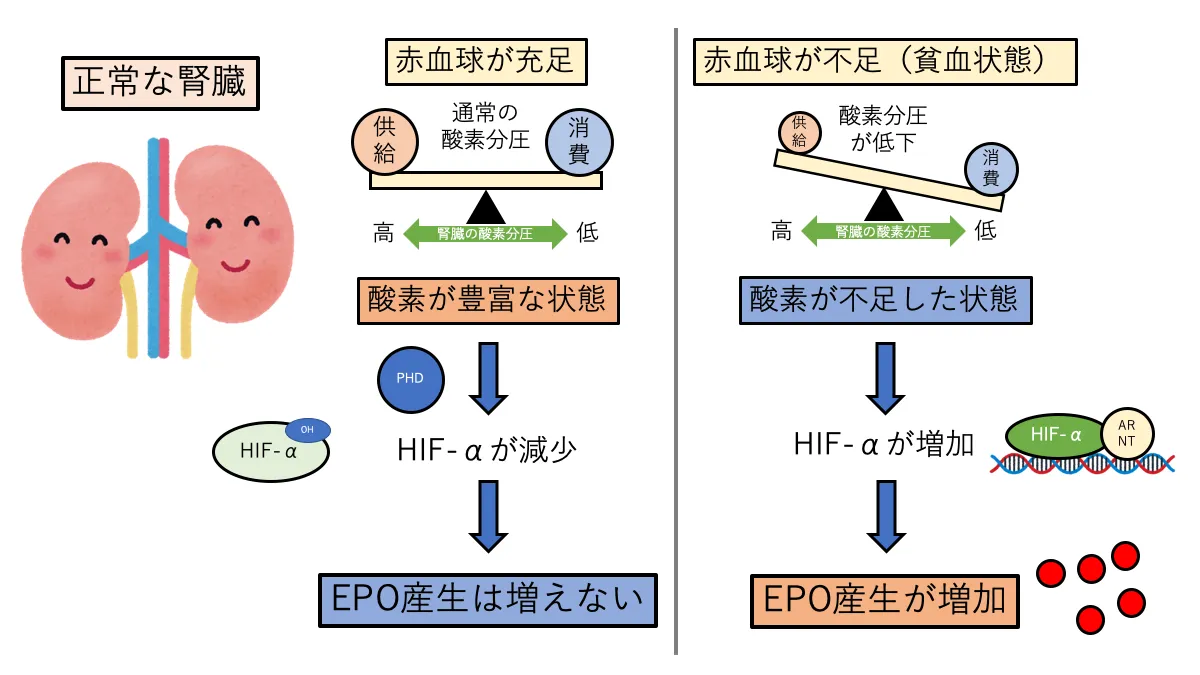
腎機能が低下した場合は、尿細管の機能が低下しているため、酸素の消費量が減少しています。酸素消費量が少ない場合、酸素供給量が低下しても酸素分圧がそれほど低下しない(酸素が不足しない)ため、PHDの働きは低下せず、EPOの産生は増加しません。
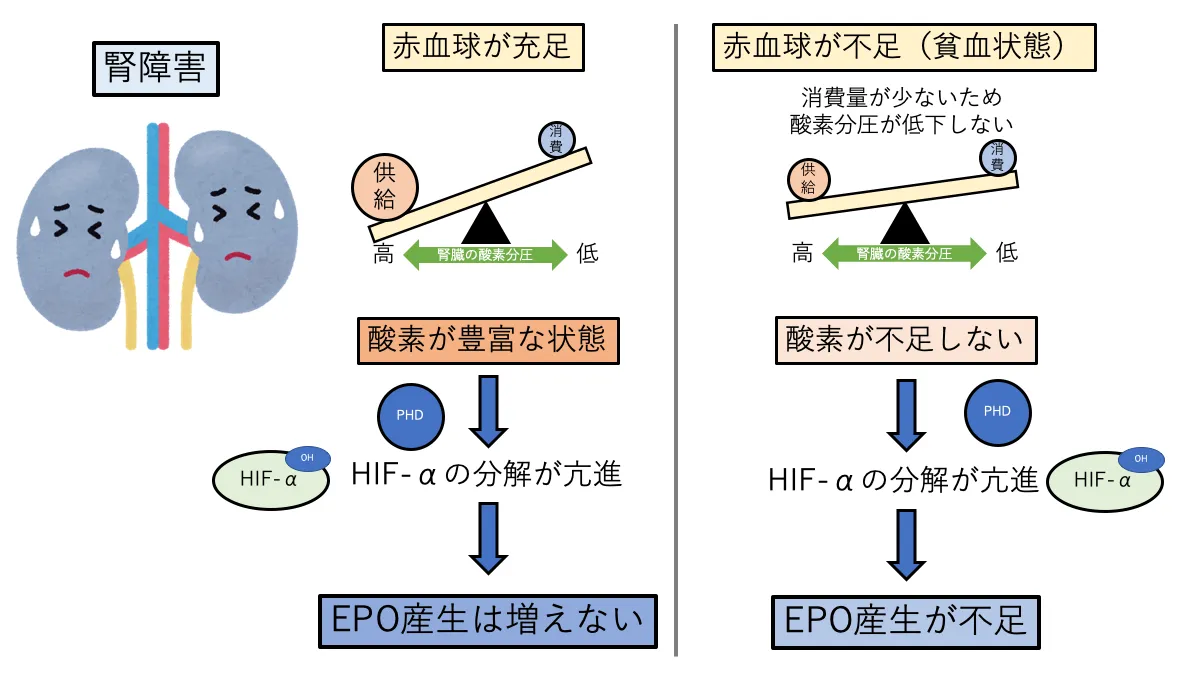
腎機能が低下した状態では、何らかの理由で赤血球数が減少してもEPO産生増加によるフィードバックが機能しないため、EPOの相対的欠乏により貧血を起こしてしまいます。
これが腎性貧血の主な原因と考えられています。
HIF活性化によるEPO産生促進
酸素濃度によって調節されているHIF経路ですが、HIF-PH阻害薬はPHDを直接阻害することで、酸素分圧に関係なくHIFを活性化します。
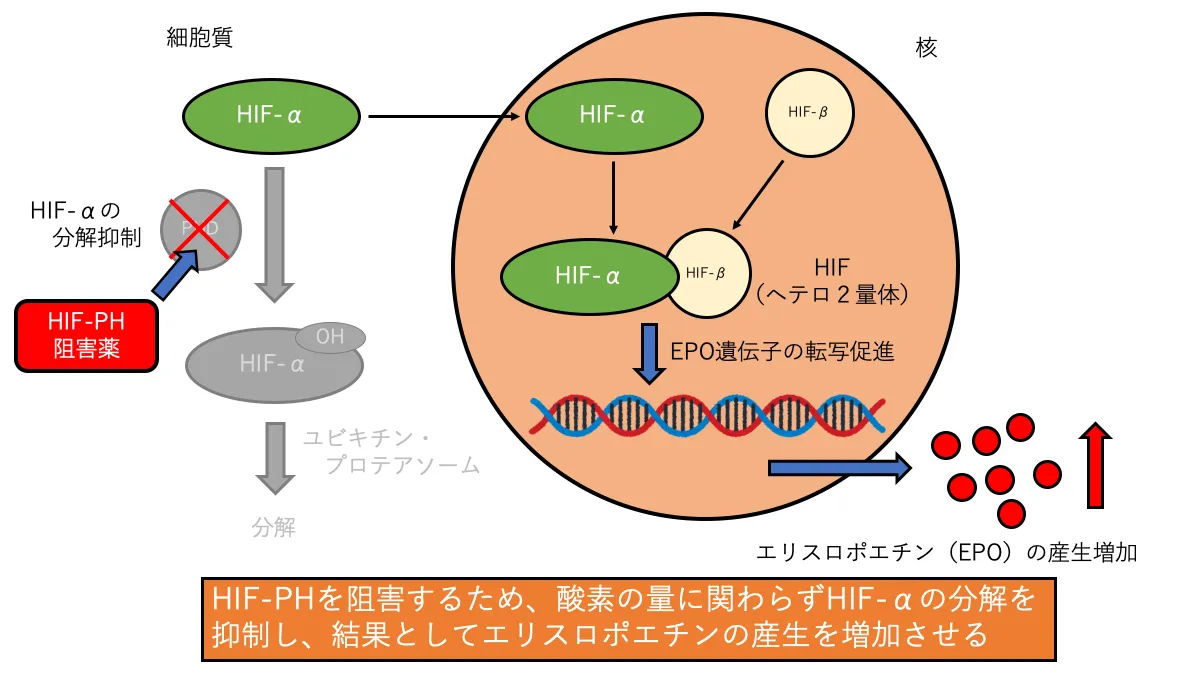
活性化されたHIFによりEPO遺伝子の転写行われ、EPO産生を促進します。この内因性EPOの増加作用こそがHIF-PH阻害薬が腎性貧血を改善する主たる作用になりますが、そのほかにも腎性貧血の改善に繋がる作用が期待されています。
HIF活性化による鉄吸収の促進
HIFは腸管での鉄吸収に関与するDMT1*13遺伝子やDcytb*14遺伝子の転写も促進します。さらに、体内での鉄輸送を担うトランスフェリンの産生やトランスフェリン受容体の産生に関わる遺伝子の転写も促進します。そのため、HIF-PH阻害薬によりHIFが活性化されることで体内の鉄吸収や鉄輸送が促進されます。
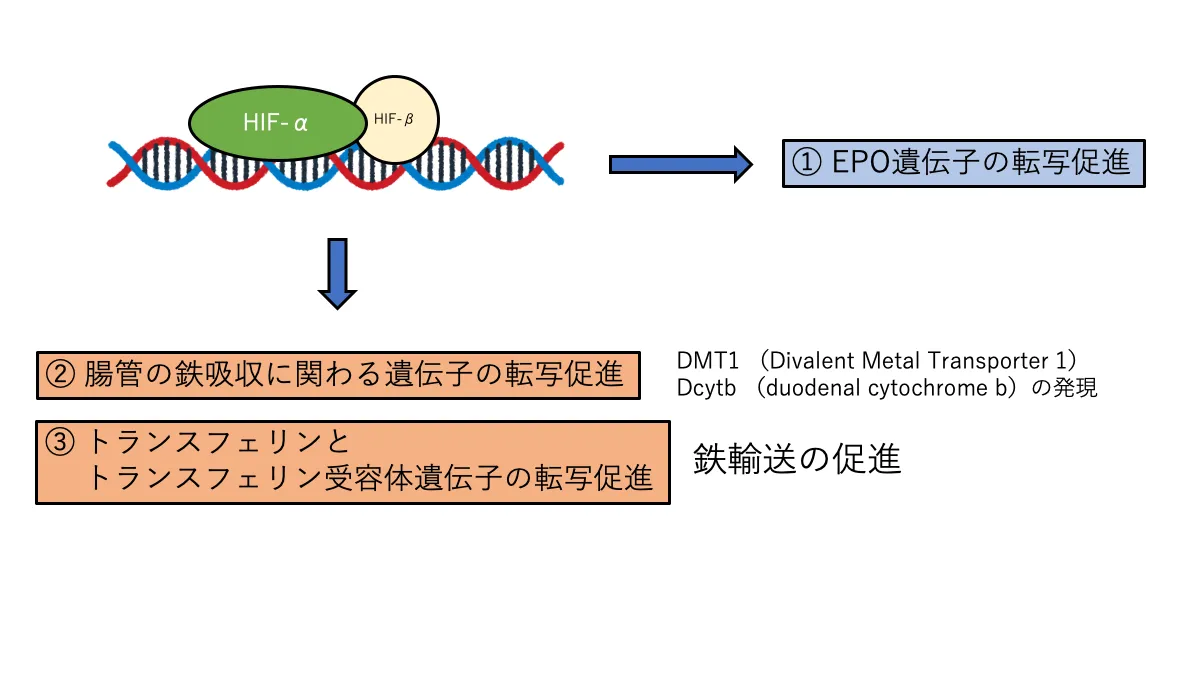
HIF活性化による高ヘプシジン血症の改善
腎性貧血の原因の一つに高ヘプシジン血症があります。
ヘプシジンは血清鉄濃度の恒常性を担うホルモンです。ヘプシジンは血清鉄濃度が上昇することで肝臓から放出され様々な作用で血清鉄濃度を低下させます。
- 肝臓からの貯蔵鉄の放出抑制
- 小腸上部での鉄吸収抑制
- マクロファージによる老化赤血球からの鉄回収抑制
腎性貧血ではEPOによる赤血球への分化が不足しているため、鉄の利用が低下し、血清鉄濃度が上昇しています。
また、慢性的な炎症(CKD)により高IL-6血症を起こしているため、IL-6によるヘプシジンの産生が促進されています。
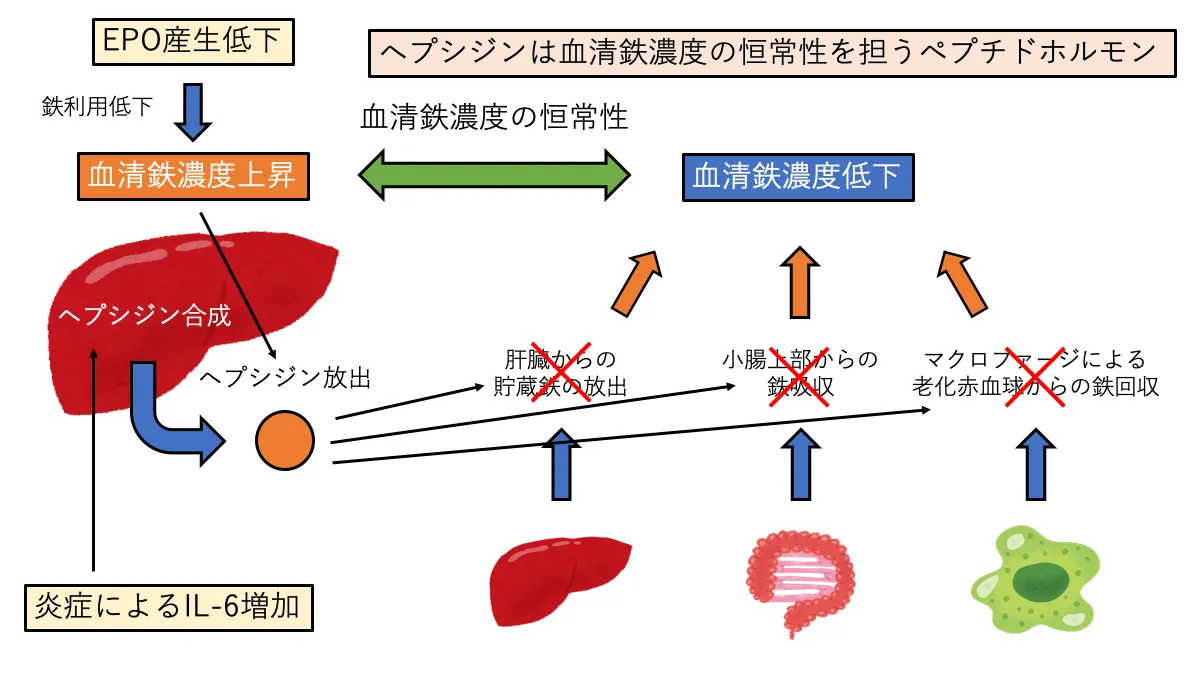
このように、高ヘプシジン血症により血清鉄濃度が低下してしまうのも腎性貧血の原因となっています。
HIF活性化によりEPOが産生、鉄利用が促進することでヘプシジンの放出が抑制されると同時に、HIF自体がヘプシジンの産生を抑制する効果もあると考えられています。
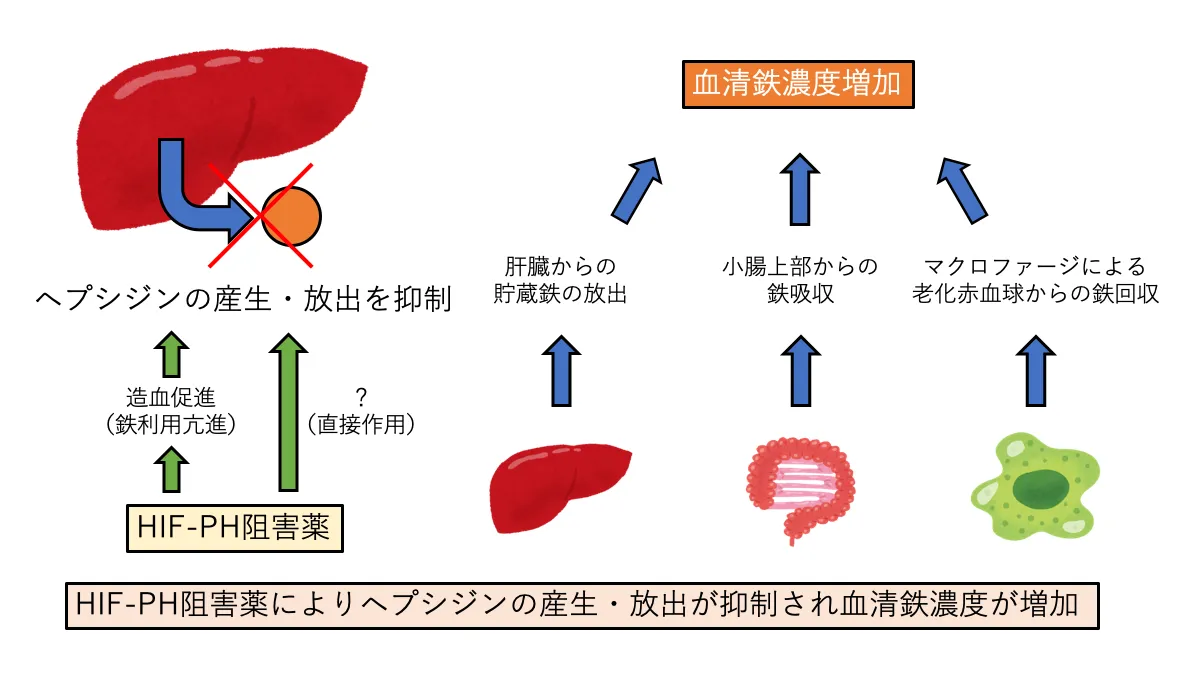
このようにHIF-PH阻害薬は高ヘプシジン血症を改善することでも腎性貧血に対する効果を発揮できると期待されています。
ダーブロックのヘプシジンに対する作用については審議結果報告書の中でも触れられています。
3. 非臨床薬理試験に関する資料及び機構における審査の概略
3.1 効力を裏付ける試験(CTD 4.2.1.1)
3.1.1 in vitro 試験
3.1.1.5 ヘプシジン発現に対する作用(試験番号 UH2009/00011/00)
ヘプシジンは、消化管、肝臓及びマクロファージにおける鉄代謝を制御するペプチドホルモンである。
ヘプシジン発現が低下するとHb産生における鉄利用が亢進することから、ヘプシジンに対する本薬の作用が検討された。BMP-6(25ng/mL)処理によりヘプシジンを誘導したHep3B細胞を、本薬(1.56〜25μmol/L)又はrHuEPO(10〜100mIU/mL)で48時間処理し、ヘプシジンmRNA量を測定した。本薬処理により濃度依存的にヘプシジンmRNA量が抑制された。一方、rHuEPO処理によるヘプシジンmRNA量への影響は認められなかった。
以上の結果から、申請者は、本薬はEPOを介さない経路によりHb産生における鉄利用を亢進する可能性があると考察している。
ダーブロック錠 審議結果報告書 医薬・生活衛生局医薬品審査管理課
そのほか期待される効果
HIF経路は他にも様々な働きに関与していることが知られています。
・嫌気的解糖に関連する酵素の誘導(酸素不足化のエネルギー供給改善)
・cytochrome oxidaseサブユニットの発現調節(好気的解糖の調節)
このあたりの作用もHIF-PH阻害薬の効果に影響していると言われています。
審議結果報告書ではダーブロックによりVEGF-A産生が増加したことが記載されています。
EPO抵抗性貧血に対する効果
腎性貧血の中にはESA製剤に対して低反応性の、EPO抵抗性を有する腎性貧血も存在します。
ESA抵抗性については様々な理由が考えられますが、内因性EPOの増加だけでなく様々な貧血改善作用を持つHIF-PH阻害薬が効果を発揮する可能性があるため期待されています。
また、極めて稀とは言われていますが、ESA製剤では抗エリスロポエチン抗体による赤芽球癆(PRCA*15)が報告されています。
HIF-PH阻害薬であればPRCAも回避できるはずなので、それも大きなメリットとなりそうです。
ダーブロック錠のDI
ここからはダーブロック錠の添付文書、インタビューフォーム、RMP、審査結果報告書から得ることのできる情報についてまとめていきたいと思います。
警告
血栓塞栓症に関して警告が記載されています。
RMPにも記載されていますが、ダーブロックを含むHIF-PH阻害薬では血栓塞栓症が最も重要なリスクになります。
1. 警告
本剤投与中に、脳梗塞、心筋梗塞、肺塞栓等の重篤な血栓塞栓症があらわれ、死亡に至るおそれがある。本剤の投与開始前に、脳梗塞、心筋梗塞、肺塞栓等の合併症及び既往歴の有無等を含めた血栓塞栓症のリスクを評価した上で、本剤の投与の可否を慎重に判断すること。また、本剤投与中は、患者の状態を十分に観察し、血栓塞栓症が疑われる徴候や症状の発現に注意すること。血栓塞栓症が疑われる症状があらわれた場合には、速やかに医療機関を受診するよう患者を指導すること。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
インタビューフォームには下記の通り警告の理由が記載されています。
VIII.安全性(使用上の注意等)に関する項目
1.警告内容とその理由
(解説)
赤血球造血刺激因子製剤(以下、ESA)の副作用として、貧血改善に伴い血液粘稠度が上昇し血栓塞栓症の発現リスクが増加することが報告されており、ESAの添付文書で血栓塞栓症について注意喚起されている。本剤の作用機序を踏まえると、過度の赤血球生成を来した場合、それに続発して血栓塞栓症を発現する可能性がある。本剤の臨床試験では、対照群(ESA群)と同様の発現頻度で血栓塞栓症に関連する有害事象が認められた。
そのため、本剤を使用するにあたり、以下の点に注意すること。
- 本剤の投与開始前に、脳梗塞、心筋梗塞、肺塞栓等の合併症及び既往歴の有無等を含めた血栓塞栓症のリスクを評価した上で、本剤の投与の可否を慎重に判断すること。
- 本剤投与中は、患者の状態を十分に観察し、血栓塞栓症が疑われる徴候や症状の発現に注意すること。
- 血栓塞栓症が疑われる症状があらわれた場合には、速やかに医療機関を受診するよう患者を指導すること。
ダーブロック錠 インタビューフォーム グラクソ・スミスクライン株式会社
あとで紹介する重要な基本的注意やRMP(重要な特定されたリスク)に記載されていますが、HIF-PH阻害薬ではHb値の上昇に伴い血液粘稠度が増すことで血栓塞栓症が発現する恐れがあるため、定期にHbを測定して投与量を調節する必要があります。
同様の機序で血栓塞栓症のリスクが知られているESA製剤では警告記載はありませんが、これはHIF-PH阻害薬は経口投与であるため、(1年後には)長期投与となり、Hb測定が疎かになった結果、血栓塞栓症が発生することがないように注意が必要なためではないかと考えます。
また、注射剤に抵抗があり治療を躊躇っていた境界域の患者さんでも使用可能になるケースが多く、使用する患者さんが多くなる可能性が高いことも警告記載の理由かもしれません。
禁忌は過敏症の既往歴のみ
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
ダーブロック錠 インタビューフォーム グラクソ・スミスクライン株式会社
過敏症の既往歴は当然のとことながら、エナロイは妊娠中の投与が禁忌となっています。
現在(R3.3.10時点)で承認されているHIF-PH阻害剤5剤のうち、マスーレッド、エナロイ、エベレンゾは妊娠中の投与が禁忌です。
| 禁忌 | エベレンゾ | ダーブロック | バフセオ | エナロイ | マスーレッド |
| 過敏症 | × | × | × | × | × |
| 妊娠 | × | – | – | × | × |
効能・効果:腎性貧血(保存期・透析期に関わらず使用可能)
ダーブロック錠の効能・効果は「腎性貧血」です。
ダーブロック錠は他のHIF-PH阻害薬と同様に腎性貧血であれば透析期・保存期の区別なく使用可能です。
(用法・用量については透析の有無などで分かれているので後で解説します)
腎性貧血治療開始の目安
効能・効果には以下の注意書きが加えられています。
5. 効能又は効果に関連する注意
赤血球造血刺激因子製剤で未治療の場合の本剤投与開始の目安は、保存期慢性腎臓病患者及び腹膜透析患者ではヘモグロビン濃度で11g/dL未満、血液透析患者ではヘモグロビン濃度で10g/dL未満とする。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
腎性貧血の説明で紹介したJSDT腎性貧血ガイドライン2015の治療開始基準に従って投与を開始します。
| 状態 | 治療開始のHb値 | 目標Hb値 |
| ND(保存期CKD) | 11g/dL未満 | 11g/dL以上13g/dL未満 |
| PD(腹膜透析) | ||
| HD(血液透析) | 10g/dL未満 | 10g/dL以上12g/dL未満 |
用法・用量(保存期・透析期、ESA治療の有無で開始用量が変化)
6. 用法及び用量
6.1 保存期慢性腎臓病患者
赤血球造血刺激因子製剤で未治療の場合
通常、成人にはダプロデュスタットとして1回2mg又は4mgを開始用量とし、1日1回経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1日1回24mgまでとする。
赤血球造血刺激因子製剤から切り替える場合
通常、成人にはダプロデュスタットとして1回4mgを開始用量とし、1日1回経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1日1回24mgまでとする。
6.2 透析患者
通常、成人にはダプロデュスタットとして1回4mgを開始用量とし、1日1回経口投与する。以後は、患者の状態に応じて投与量を適宜増減するが、最高用量は1日1回24mgまでとする。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
用法・用量は保存期か透析期か、ESA製剤既療中か未治療かで3つにわけて記載されていますが、用法・用量で整理すると2パターンです。
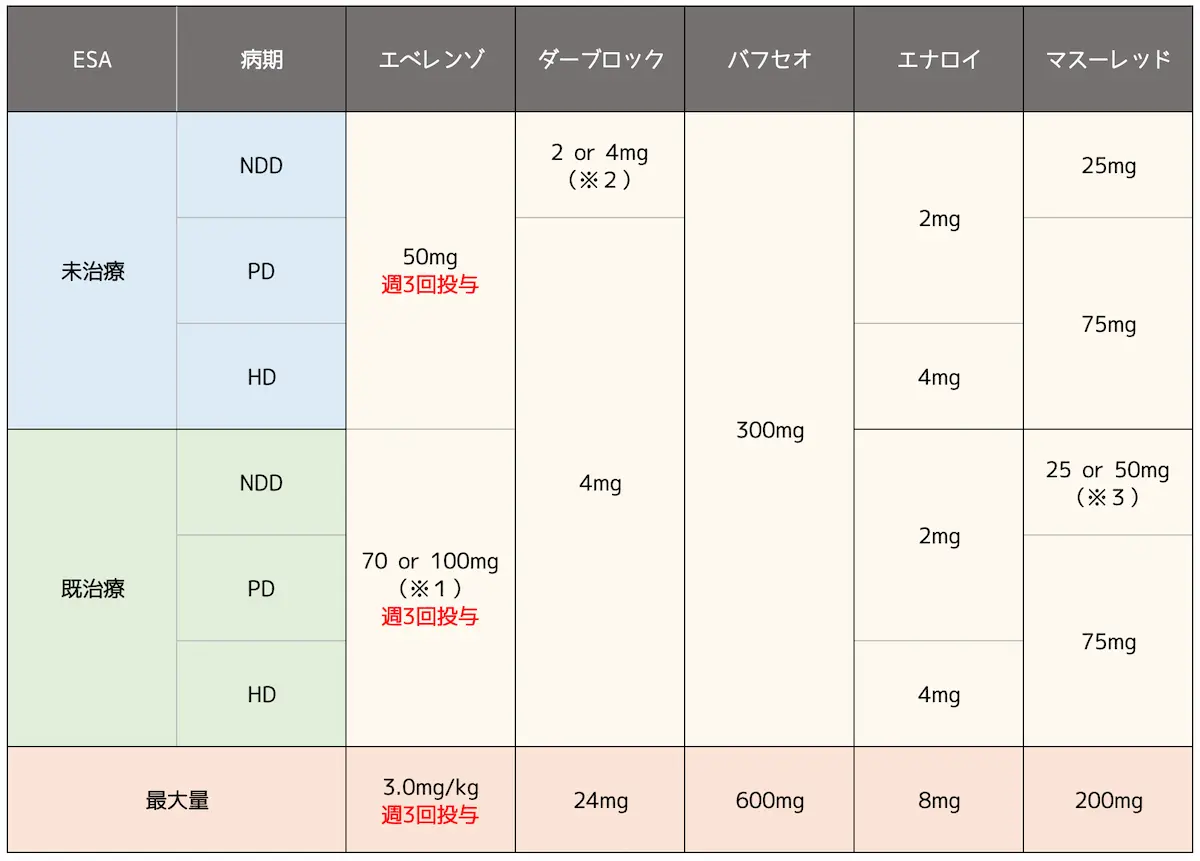
他のHIF-PH阻害薬とあわせて用法・用量を表にまとめてみます。
保存期CKDに対して使用可能な他のHIF-PH阻害薬とあわせて用法・用量をまとめてみます。
※2:Hb≧9.0g/dL 2mg、Hb<9.0g/dL 4mg
保存期CKDでESA製剤未治療の場合の初期用量
保存期CKDでESA製剤による治療を受けていない場合の初期用量は「1回2mg又は4mg」と記載されていますが、2mgか4mgかは投与開始時のHb濃度によって決定します。
7. 用法及び用量に関連する注意
7.1 赤血球造血刺激因子製剤で未治療の保存期慢性腎臓病患者の開始用量
投与開始時のヘモグロビン濃度に応じて、以下の用量で投与を開始すること。
ヘモグロビン濃度 開始用量(1日1回) 9.0g/dL未満 4mg 9.0g/dL以上 2mg ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
結局、2mg開始となるのは「ESA未治療の保存期CKDでHb濃度が9.0以上の場合のみ」ということになりますね。
増量・減量に関する注意点
増量・減量の段階について以下のように記載されています。
7. 用法及び用量に関連する注意
7.2 投与量調節
投与量調節が必要な場合には、下表を参考に1段階ずつ増量又は減量を行うこと。
また、休薬した場合には、休薬前より少なくとも1段階低い用量で投与を再開すること。なお、用量調節を行った場合には、少なくとも4週間は同一用量を維持することとするが、ヘモグロビン濃度が急激に(4週以内に2.0g/dLを超える)上昇した場合には、速やかに減量又は休薬すること。
段階 1 2 3 4 5 6 7 8 投与量 1mg 2mg 4mg 6mg 8mg 12mg 18mg 24mg ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
段階的な増量を守る必要があるのはHb濃度の急激な上昇(4週以内に2.0g/dL超)を防ぐためですね。
また、重要な基本的注意には以下の通り、用量に関する注意が記載されています。
8. 重要な基本的注意
8.1 本剤投与開始後は、ヘモグロビン濃度が目標範囲で安定するまでは、2週に1回程度ヘモグロビン濃度を確認すること。
8.2 本剤投与中は、ヘモグロビン濃度等を4週に1回程度確認し、必要以上の造血作用があらわれないように十分注意すること。赤血球造血刺激因子製剤の臨床試験においてヘモグロビンの目標値を高く設定した場合に、死亡、心血管系障害及び脳卒中の発現頻度が高くなったとの報告がある。
8.3 ヘモグロビン濃度が4週以内に2.0g/dLを超える等、急激に上昇した場合は速やかに減量または休薬する等、適切な処置を行うこと。
8.4 血液透析患者及び腹膜透析患者において、赤血球造血刺激因子製剤の投与量が高い患者では、本剤への切替え後にヘモグロビン濃度が低下する傾向が認められていることから、本剤への切替えの必要性を十分検討すること。本剤へ切り替えた場合は、切替え後のヘモグロビン濃度の低下に注意すること。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
Hb値の目標は以下の通りです。
保存期CKD、PD:11g/dL以上13g/dL未満(重篤なCVD合併:12g/dL未満)
HD:10g/dL以上12g/dL未満
この数値を目標に安定するまでは2週間ごとに検査、安定後は4週間ごとに検査する必要があります。
ESA製剤からの切替時にHb濃度が低下する可能性があっても初期用量は4mg、4週間ごとの段階的な増量を守る必要があるのは過度の造血による血栓症のリスクを避けるためですね。
目標Hb値を維持する際の用量は?
ダーブロック錠の用量は1〜24mgと幅広く、規格も1mg・2mg・4mg・6mgの4種類存在します。
開始用量は2mgか4mgと決められていますが、最終的にどの程度の用量になるかイメージしたいところです。
これについてはインタビューフォームの「V.治療に関する項目 > 3.用法及び用量 > (2)用法及び用量の設定経緯・根拠」の項目に記載されています。
患者さんの状態ごとに「ii)Hgb 値を目標範囲内に到達・維持するための用量」内に最終投与量の中央値と25%点〜75%点が記載されています。
| 投与条件 | 最終投与量 | ||
| 中央値 | 25%点〜75%点 | ||
| ND患者 | ESA未治療 | 4mg | 2〜6mg |
| ESAからの切替 | 4mg | 4〜8mg | |
| HD患者 | ESA未治療 | 4mg | 2〜6mg |
| ESAからの切替 | 6mg | 4〜8mg | |
| PD患者 | ESA未治療 | 4〜12mg | |
| ESAからの切替 | 6mg | 3〜8mg | |
ND患者、HD患者では2〜8mgでほとんどをカバーできるので、2mgと4mgを採用しておけば問題ないかと思います。
患者背景に関わる注意点
合併症など患者の状態による注意点をまとめます。
鉄剤投与の必要性
8. 重要な基本的注意
8.6 造血には鉄が必要であることから、鉄欠乏時には鉄剤の投与を行うこと。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
腎性貧血の治療方法についての部分でも解説しましたが、鉄欠乏により貧血が起きている場合には鉄剤の投与が必要となります。
JSDT腎性貧血ガイドライン2015に記載されている鉄欠乏についての基準を表にまとめておきます。
| 血清フェリチン値 | TSAT | その他 | |
| ESA投与前 | 50ng/mL未満 | – | – |
| ESA投与中 | 100ng/mL未満 | 20%未満 | – |
| 100ng/mL未満 | – | 鉄利用率を低下させる 病態が認められない | |
| – | 20%未満 |
※血清フェリチン値が300ng/mL 以上となる鉄補充療法は推奨しない。
HIF-PH阻害薬投与中の鉄欠乏については、ESA投与中と同様に「フェリチン<100ng/mLまたはTSAT<20%」で判断するべきと考えます。
血栓塞栓症の既往がある患者
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 脳梗塞、心筋梗塞、肺塞栓等の患者、又はそれらの既往歴のある患者
本剤投与により血栓塞栓症を増悪あるいは誘発するおそれがある。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
警告にも記載されていたように、造血作用を持つHIF-PH阻害薬(ESA製剤も)では血栓症のリスク増加が知られています。
そのため、脳梗塞、心筋梗塞、肺塞栓等については既往を含めて注意が必要となります。
高血圧を合併する患者
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.2 高血圧症を合併する患者
血圧上昇があらわれるおそれがある。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
これも、造血作用を持つHIF-PH阻害薬(ESA製剤も)のリスクです。
腎性貧血の改善により抹消血管が収縮し、高血圧が発症、憎悪することが知られています。
そのため、高血圧を合併している場合は注意が必要です。
血管新生によるリスク
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.3 悪性腫瘍を合併する患者
本剤投与により血管新生が亢進する可能性があることから、悪性腫瘍が増悪するおそれがある。
9.1.4 増殖糖尿病網膜症、黄斑浮腫、滲出性加齢黄斑変性症、網膜静脈閉塞症等を合併する患者
本剤投与により血管新生が亢進する可能性があることから、網膜出血があらわれるおそれがある。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
作用機序の部分で少し触れましたがHIFの活性化はEGFRを増加させ、血管新生を促進します。
そのため、悪性腫瘍や黄斑変性など血管新生が関与する疾患を悪化させてしまう可能性があります。
肝機能障害を合併する患者
9. 特定の背景を有する患者に関する注意
9.3 肝機能障害患者
本剤の減量を考慮するとともに、患者の状態を慎重に観察すること。本剤6mgを軽度及び中等度の肝機能低下者(Child-Pugh分類:A 及びB)に単回投与した時、本剤のCmax及びAUC0-∞が上昇した。重度の肝機能低下者(Child-Pugh分類:C)を対象とした臨床試験は実施していない。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
16.6 特定の背景を有する患者
16.6.2 肝機能障害患者
本剤6mgを軽度及び中等度の肝機能低下者(Child-Pugh分類:A及びB)に単回経口投与した時、ダプロデュスタットのCmaxはそれぞれ1.01倍及び1.98倍、AUC0-∞はそれぞれ1.46倍及び2.00倍増加した。また、主要代謝物のCmaxはそれぞれ1.34~1.79倍及び1.04~1.28倍、AUC0-∞はそれぞれ1.46~1.94倍及び1.31~1.65倍増加した(外国人データ)。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
確かに、肝機能障害によりCmaxとAUC0-∞が増加していますが、ダーブロック錠は投与量が幅広い薬剤(1mg〜24mg)で低用量から開始していくため、臨床上大きな問題にはならないのではないかと思います。
また、定期的にHb値を計測して効果を評価して投与量を判断していく薬剤のため、投与中に肝機能の悪化があっても対応可能かと思います。
参考:Child-Pugh(チャイルド・ピュー)分類について
Child-Pugh(チャイルド・ピュー)分類とは肝臓の障害度を表す分類です。
点数表を元にグレードの分類が行われます。
| グレード | 点数 | 肝障害の状態 |
|---|---|---|
| Grade A(軽度) | 5〜6点 | 代償性肝硬変 肝臓の機能が保たれた状態 |
| Grade B(中等度) | 7〜9点 | 代償性肝硬変から非代償性肝硬変への過渡期 軽度の合併症が見られる |
| Grade C(重度) | 10〜15点 | 非代償性肝硬変 肝臓の機能が維持できなくなり様々な合併症があらわれる |
以下の表の点数を元に分類を行います。
| 項目 | 1点 | 2点 | 3点 |
| 脳症 | ない | 軽度(Ⅰ、Ⅱ) | 時々昏睡(Ⅲ〜) |
| 腹水 | ない | 少量(1〜3L) | 中等量(3L〜) |
| 血清ビリルビン値(mg/dL) | 2.0未満 | 2.0〜3.0 | 3.0超 |
| 血清アルブミン値(g/dL) | 3.5超 | 2.8〜3.5 | 2.8未満 |
| プロトロンビン活性値(%) | 70超 | 40〜70 | 40未満 |
参考:腎機能障害時の影響は少ない
腎機能に関する情報も掲載しておきます。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
中等度~重度の腎機能低下者(中等度:eGFR 30~59mL/分/1.73㎡、重度:eGFR 15~29mL/分/1.73㎡)に本剤50mg又は150mg)を単回経口投与した時のダプロデュスタットのAUC0-∞は腎機能正常者(eGFR 90mL/分/1.73㎡以上)と概ね同様であった(外国人データ)。また、本剤5mgを反復経口投与した時の主要代謝物のAUCは、腎機能正常者に比べて、腎機能低下者(eGFR ≤59mL/分/1.73㎡、血液透析患者を含む)で約2~6倍増加した(外国人データ)。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
有効成分の蓄積はなさそうなので特に問題もなさそうです。
(腎機能障害がある場合にしか使用されない薬剤なのでそうでないと困りますよね。)
妊婦・授乳婦・小児に関する注意
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。本剤は胎児に移行する可能性がある。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。ラットの授乳期に本剤を経口投与した時、生後10日の出生児血漿中に本剤が認められたことから、本剤は乳汁に移行する可能性がある。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
造血系に対する作用、血管新生を増加させる作用があることから、胎児・新生児・小児への暴露は避けたいところですね。
ただし、妊婦・授乳婦に関しては禁忌には設定されていないので、注意は必要ですが使用する可能性はあるということになります。
小児については適応外になりますね。
相互作用は少ない
ダーブロック錠には併用禁忌の記載はなくCYP2C8に関連する併用注意のみが記載されています。
10. 相互作用
本剤は主にCYP2C8により代謝される。
10.2 併用注意(併用に注意すること)
CYP2C8阻害剤
・クロピドグレル
・トリメトプリム 等
リファンピシン
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
CYP2C8阻害薬による影響
クロピドグレルやトリメトプリムのようなCYP2C8阻害薬はダーブロックの作用を増強するおそれがあります。参考までに添付文書上に記載されていないCYP2C8阻害薬も含めて商品名を書き出してみます。
トリメトプリム(バクタ、ダイフェン、バクトラミン)
デフェラシロクス(ジャドニュ顆粒分包)
ファビピラビル(アビガン)
実際にどの程度影響があるかについて添付文書と審議結果報告書に記載されているデータを元に表にしてみます。
| CYP2C8阻害薬 | AUC0-∞ | Cmax |
| トリメトプリム (200mg 1日2回) | 1.48倍 | 1.28倍 |
| クロピドグレル | 2.65倍(推定) | 1.79倍(推定) |
※強力なCYP2C8阻害薬とされているゲムフィブロジルについては日本では未発売のため省略
クロピドグレルによる相互作用の評価について審議結果報告書には以下のようにまとめられています。
6. 生物薬剤学試験及び関連する分析法、臨床薬理試験に関する資料並びに機構における審査の概略
6.R 機構における審査の概略
6.R.1 他剤が本薬の薬物動態に及ぼす影響について
国内第III相試験(HD貧血改善試験、HD切替え維持試験及びND/PD試験)の安全性併合解析の結果、クロピドグレル非併用例(343例)と比較して、クロピドグレル併用例(26例)において、有害事象及び副作用の発現割合が高くなる傾向は認められず、特段問題となる事象も認められなかった。また、本薬の投与開始前よりクロピドグレルを併用していた患者及び本薬投与中にクロピドグレルの併用を開始した患者において、Hb値の推移は定期的モニタリングにより管理可能であった。
(略)
これらの母集団薬物動態解析結果を踏まえて、最高臨床用量である本薬24mgとクロピドグレルを併用した場合の本薬未変化体の推定曝露量は、クロピドグレル非併用時に本薬63.6mgを投与した際の曝露量相当となる。当該曝露量は、第I相試験(本薬の最高投与量は100mg)等の国内外の臨床試験で安全性が確認された曝露量を超えないと考える。
以上を踏まえると、クロピドグレルを併用禁忌に設定する必要はないと考える。
ダーブロック錠 審議結果報告書 医薬・生活衛生局医薬品審査管理課
最大用量である24mgとクロピドグレルを併用した場合でも63.6mg相当(第I相試験で安全性が確認された範囲)であること、国内第III相試験でクロピドグレル併用群で有害事象及び副作用の発現割合が高くなる傾向は認められ無かったことが禁忌に該当しない理由です。
ダーブロックは低用量から効果(Hb値)を見ながら増量していくため、投与開始前からCYP2C8阻害薬を併用している場合は特に問題なしです。
ダーブロック服用中にクロピドグレルの併用開始する場合は急激なHb値の変化がないか注意し、状況に応じてダーブロックの中止・減量を考慮するという形で問題ないでしょう。
ちなみに承認された用量を超える過量投与についての安全性が気になる場合、添付文書には以下のような記載があります。
13. 過量投与
13.1 症状
本剤500mg注)を単回投与した時に、頭痛や胃腸障害(悪心、腹痛等)が認められた。本剤の過量投与によりヘモグロビン濃度が必要以上に増加するおそれがある。
注)本剤の承認された最高用量は、1日1回24mgである。
13.2 処置
本剤の減量・休薬等の適切な処置を行うこと。本剤は高い蛋白結合率を有するため、血液透析により除去できる可能性は低い。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
500mgというかなりの過量投与を行った場合でも短期的な影響はそこまで大きくなさそうなので、こまめに血液検査を行い、Hb値を把握することで対応できるのではないかと思います。
CYP2C8誘導薬による影響
CYP2C8阻害薬は阻害剤とは逆にダーブロックの作用を減弱させるおそれがあります。
リファジン
ただし、CYP2C8誘導薬による影響については臨床薬物相互作用試験が行われていないため具体的なデータが存在しません。
影響は否定できないので注意が必要ですが、これについてもHb値をしっかりと管理することで対応可能だと思います。
その他(CYP2C8基質とOATP1B1/1B3基質)
その他としてCYP2C8基質(ピオグリタゾン)とOATP1B1/1B3基質(ロスバスタチン)を併用した場合のデータが記載されています。
16. 薬物動態
16.7 薬物相互作用
16.7.1 In vitro
In vitroにおいて、本剤はCYP2C8を阻害した。また、本剤はBCRPの基質であり、OATP1B1及び1B3を阻害した。
16.7.4 その他の薬剤
健康成人に本剤25又は100mg注)をピオグリタゾン(CYP2C8基質)15mg及びロスバスタチン(OATP1B1/1B3基質)10mgと経口併用投与した時、ダプロデュスタットはピオグリタゾン又はロスバスタチンの曝露量に影響を及ぼさなかった(外国人データ)。
経口鉄剤及びリン吸着剤は本剤の薬物動態に対して影響を与えなかった。
注)本剤の承認された用法は1日1回経口投与であり、最高用量は1日1回24mgである。
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
副作用は非常に少ないが・・・
副作用は非常に少なくシンプルに記載されています。
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
血栓塞栓症(0.8%)
脳梗塞(0.3%)、肺塞栓症(0.3%)、網膜静脈閉塞(0.3%)、深部静脈血栓症(0.3%)、バスキュラーアクセス血栓症(シャント閉塞等)(頻度不明)等の血栓塞栓症があらわれることがある。
11.2 その他の副作用(全て1%未満)
眼:網膜出血
過敏症:過敏症(発疹、皮膚炎、蕁麻疹)
循環器:高血圧
ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
やはり問題になるのは血栓塞栓症でしょうね。
HDの場合はシャント閉塞も起こします。
RMPの項でもまとめますが、薬剤の性質上、避けることができない問題です。
Hb値を定期的に検査し、高値にならないように、急激に上昇させないように用量の調節を行うことが大切になります。
高血圧については腎性貧血の改善に伴い、血中酸素濃度低下が改善、末梢血管が収縮することで発生すると考えられています。
RMPに記載されている注意点
- 重要な特定されたリスク
- 血栓塞栓症
- 高血圧
- 重要な潜在的リスク
- 心血管系事象(血栓塞栓症を除く)
- 悪性腫瘍
- 常染色体優性多発性嚢胞腎(ADPKD)患者における病態の進行
- 網膜血腫
血栓塞栓症(重要な特定されたリスク)
ダーブロック錠の効果が過剰に発現された場合、過度の赤血球生成による血液粘稠度の上昇が起こり、血栓症とそれに伴う組織虚血を起こしてしまう可能性があります。
そのため血栓塞栓症は「重要な特定されたリスク」に設定され、添付文書の「警告」にも記載されています。
非臨床試験では、ダーブロック錠に起因する過度の赤血球生成により、「複数の臓器での血管うっ血/炎症、微小血栓及び組織虚血」が認められています。
| 薬剤 | 血栓塞栓症の有害事象 <因果関係が否定できない> | 重篤な事象 <因果関係が否定できない> |
| ダーブロック群 | 5%(17/369例) <1%未満(3/369例)> | 2% (7/369例) <なし> |
| 対照(ESA)群 | 6%(16/285例) | 2%(5/285例) |
※国内第III相試験 3試験:201753試験、201754試験、204716試験
HIF-PH阻害薬(ESA製剤)の副作用として最も特徴的なものになります。
高血圧(重要な特定されたリスク)
腎性貧血に対してESAを投与した場合にコントロール不良の高血圧が発現するリスクが知られており、高血圧性脳症や痙攣発作の報告もあります。
ダーブロック錠の臨床試験で報告された高血圧関連の有害事象の発現頻度がESA群と同程度であったため「重要な特定されたリスク」に設定されています。
| 薬剤 | 高血圧 | 血圧上昇 |
| ダーブロック群 | 4%(14/369例) | 2%(9/369例) |
| 対照(ESA)群 | 6%(16/285例) | 2%(5/285例) |
※国内第III相試験 3試験:201753試験、201754試験、204716試験(3試験ともにほとんどの被験者がベースライン時に合併症として高血圧を有していた)
腎性貧血の改善に伴い高血圧が発生することが知られており、「慢性腎臓病患者における腎性貧血治療のガイドライン 2015 年版(日本透析医 学会編)」において、貧血改善により組織中低酸素濃度も是正され、拡張していた末梢血管が収縮すること、また 血液粘稠度が亢進すること等により、末梢血管抵抗が増加することに起因すると説明されています。
心血管系事象(血栓塞栓症を除く)(重要な潜在的リスク)
腎性貧血患者にESA製剤を投与した際、特に高い目標Hb値、2週間に1g/dLを超えるHb値の上昇及び高用量のESA投与が死亡及び重篤な心血管系事象の発現リスクの増加と関連
することが知られています。
ダーブロック錠の臨床試験で報告された心血管系関連の有害事象の発現頻度がESA群と同程度であったため「重要な特定されたリスク」に設定されています。
| 薬剤 | MACE*16 <重篤なもの> | 心不全関連の有害事象 <重篤なもの> |
| ダーブロック群 | 2%(8/369例) <1%未満(3/369例)> | 2%(6/369例) <1%(4/369例)> |
| 対照(ESA)群 | 2%(7/285例) <1%(3/285例)> | 4%(10/285例) <3%(9/285例)> |
※国内第III相試験 3試験:201753試験、201754試験、204716試験
※MACEの定義は、すべての死亡、心筋梗塞、脳卒中とした
ちなみに国際共同第II相試験ではMACE及び死亡の発現割合がESA群と比較してダーブロック群の方が高い傾向が認められています。
ですが、試験デザイン、発現数の少なさ、日本人よりも欧米人の方がMACE や死亡のリス クが3〜4倍高いことを踏まえて、心血管系事象のリスク評価は国内第III相試験の結果をもとに行うことが適切と判断されています。
ということで、心血管リスクについてはESA投与と大きく変わらないと考えて問題ないかとは思いますが、欧米人に対して心血管リスクが高まる可能性があることは頭においておきたいところですね。
悪性腫瘍(重要な潜在的リスク)
国内第III相試験 3試験(201753 試験、201754 試験、204716 試験)の併合解析データではダーブロック錠と悪性腫瘍に関連する有害事象は否定(がんの種類や発現部位についても特定の傾向は認められなかった)されており、非臨床試験でのラット2年間投与試験、マウス2年間投与試験でも腫瘍性の変化は認められていません。
ですが、がん患者対象のESAの臨床試験の結果から、腫瘍増殖促進と生命予後悪化のリスクが示唆されています。
また、腫瘍組織のHIF-1増加が癌患者の死亡率上昇に関連していること、HIF-1による標的遺伝子の転写誘導が腫瘍増殖と関連することが示されています。
これらを踏まえて「重要な潜在的リスク」に設定されており、海外で実施中の大規模第III相臨床試験でも評価される予定になっています。
- Semenza GL. Defining the role of hypoxia-inducible factor 1 in cancer biology and therapeutics. Oncogene. 2010;29:625-634.
- Semenza GL. Hypoxia-Inducible Factors in Physiology and Medicine. Cell. 2012;148:399-408.
常染色体優性多発性嚢胞腎(ADPKD)患者における病態の進行(重要な潜在的リスク)
常染色体優性多発性嚢胞腎(ADPKD*17)の進行にHIF-1αが関与している可能性を示唆するin vivoのエビデンスが存在しており、「重要な特定されたリスク」に設定されています。
ADPKDのマウスではHIF-1αを欠損することで多発性嚢胞腎(PKD*18)の進行が抑えられますが、逆にHIF-1αを安定化させるPHD阻害薬を投与すると軽度のPKDが極度に悪化して腎機能が低下してしまいます。
毒性試験のデータでは腎嚢胞の発現や重症度の悪化は見られなかったようですが、国内第III相試験(201753試験)でのADPKD患者数(5例)は限られており情報は限られています。
- Kraus A, et al. HIF-1α promotes cyst progression in a mouse model of autosomal dominant polycystic kidney disease. Kidney International. 2018;94:887-899.
- Hofherr A, et al. HIF-1α drives cyst growth in advanced stages of autosomal dominant polycystic kidney disease. Kidney International. 2018;94:849-851
遺伝性の疾患で、PKD1もしくはPKD2の変異を原因とします。両側の腎臓に嚢胞ができ、年齢とともにその数が増えていく疾患です。嚢胞の増加、肥大に伴い、腎機能が低下していき様々な症状を引き起こします。多発性嚢胞腎は難病に指定されており、ADPKDの他にARPKD*19(常染色体劣性多発性嚢胞腎)が存在します。
網膜血腫(重要な潜在的リスク)
ダーブロック錠はHIF経路の活性化を作用機序としています。
HIF経路の活性化によりEGFR産生が促進され、血管新生が亢進します。
その結果、網膜血管が増殖する可能性が考えられるため、網膜血腫は「重要な潜在的リスク」に設定されています。
まとめ
ダーブロック錠の特徴をまとめます。
まずはHIF-PH阻害薬としての特徴と注意点です。
- 経口投与で腎性貧血に効果を発揮
- 内因性EPO増加
- 鉄吸収促進
- 高ヘプシジン血症の改善効果
- ESA抵抗性(EPO抵抗性)貧血に対しても効果?
- 急激なHb上昇や高Hb値での血栓塞栓症に注意
- 貧血改善による高血圧に注意
- 増量間隔は4週間以上
- 定期的な検査が必要
- 用量調節期:2週間ごと
- 目標Hb濃度達成後:4週間ごと
- Hb濃度高値や急上昇は血栓塞栓症や高血圧のリスク
- 急激なHb濃度上昇:4週間以内に2.0g/dL超の上昇)
- Hb濃度は13g/dL未満(HD:12g/dL未満)
つづいてダーブロック錠の特徴です。
- 患者のHb値に応じた細かな用量調節が可能
- NDの場合はESA製剤の治療歴で開始用量が異なる
- ESA未治療 保存期CKD Hb≧9.0g/dL:2mg開始
- 上記以外:4mg開始
- クロピドグレルの併用で血中濃度上昇
HIF-PH阻害薬の比較
2021.3.10時点の情報でHIF-PH阻害薬を比較したものを表にまとめました。
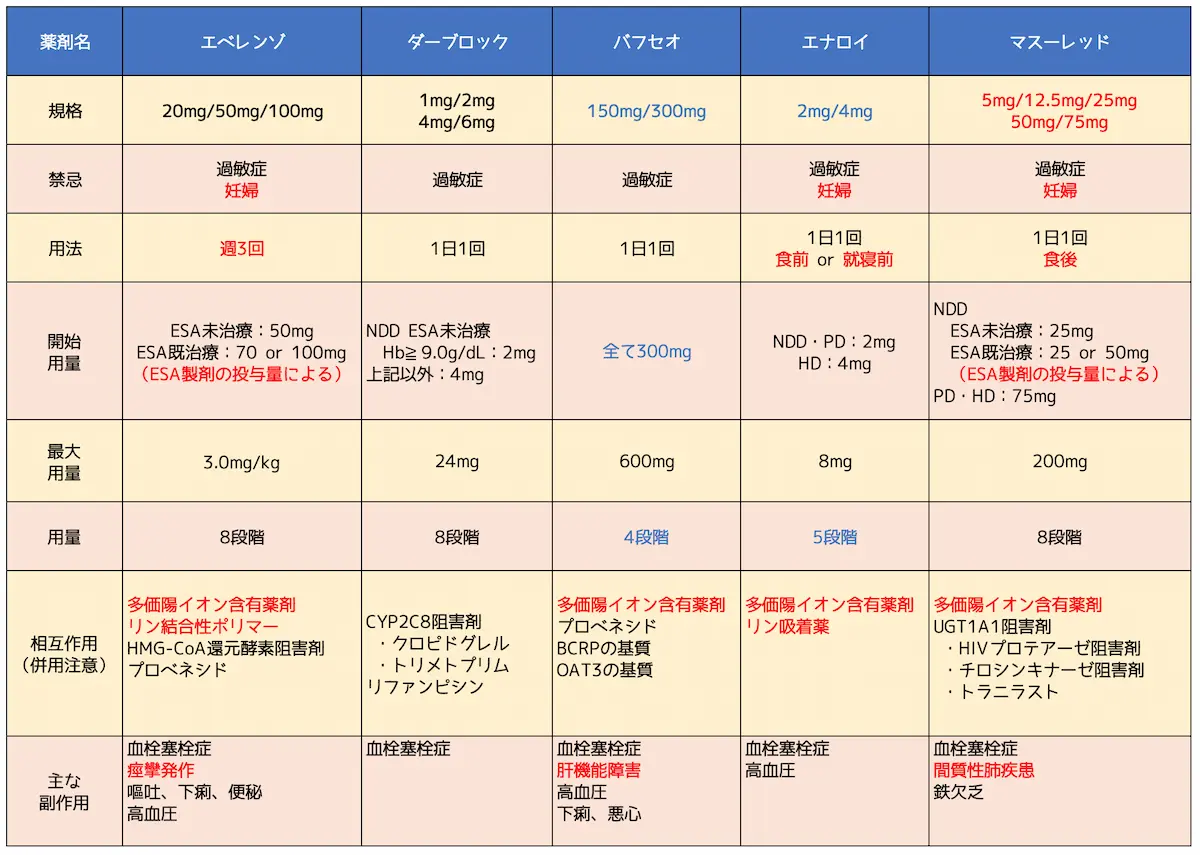 ※2020.11.27にエベレンゾ錠も保存期適応を取得
※2020.11.27にエベレンゾ錠も保存期適応を取得
HIF-PH阻害薬適正使用に関するrecommendation
2020年9月29日付で日本腎臓学会から「HIF-PH阻害薬適正使用に関するrecommendation」が公開されました。
日本腎臓学会 HIF-PH阻害薬適正使用に関するrecommendation 2020年9月29日版
- HIF-PH 阻害薬総論
- 治療に関する推奨
- 注意点
の3つにわけて記載されています。
このうち、推奨の部分について簡単にまとめてみます。
どのような患者に使用することが望ましいか(ESAからの切り替えも含め)
- ESAとHIF-PH阻害薬の選択は、個々の患者の状態や嗜好、通院頻度、ポリファーマシーや服薬アドヒアランス等に応じて、医師が判断
- HIF-PH阻害薬を使用する際は、事前に悪性腫瘍、網膜病変の検査を行い、合併がないか、適切な治療がなされているかを確認した上で開始
- 虚血性心疾患、 脳血管障害や末梢血管病のある患者については、そのリスクを評価した上で適応の可否を慎重に判断
- ESA抵抗性の原因が不明もしくは対応が困難な場合(鉄利用障害など)には、HIF-PH阻害薬への変更を考慮
- 高用量のESAからの切り替え直後にHb値の低下が認められることがあり、Hb値の推移を十分に観察してHIF-PH阻害薬の用量を調節するべき
- ESAとHIF-PH阻害薬の併用は想定されておらず、行うべきではない
鉄補充をどうすることが望ましいか
- フェリチン<100ng/mLまたはTSAT<20%をHIF-PH阻害薬使用中の鉄補充のカットオフに設定することが妥当
- 目標ヘモグロビンに到達しない場合、HIF-PH阻害薬の増量よりも鉄欠乏状体を評価した上で鉄補充を優先
- HIF-PH 阻害薬開始時に急激に造血が亢進することで、TSATやフェリチンが著しく低下する症例があるため、薬剤開始1か月後には、再度これらのマーカーを評価し、鉄欠乏があれば鉄を補充
- HIF-PH阻害薬投与中は、消化管からの鉄の吸収が改善するために経口鉄の効果が従来よりも期待できる
- クエン酸第二鉄やスクロオキシ水酸化鉄などの鉄含有リン吸着薬によっても鉄が補充されることを考慮
所感
これまで腎性貧血の治療にはESA製剤の投与のため注射が必要でした。
透析期の場合は透析時にESA投与を行うことができますが、保存期CKDや腹膜透析では注射を行う必要があります。
それが嫌でなかなか治療を開始できない患者さんもいますし、定期的な注射が苦痛でQOL低下に繋がっている患者さんもいます。
保存期CKDに使用可能なHIF-PH阻害薬(ダーブロック、バフセオ)は患者さんにとって大きな選択肢になります。
また、ESA投与でなかなか症状が改善しないESA抵抗性の腎性貧血に対してHIF-PH阻害薬が効果を発揮する可能性があります。
そのためESA抵抗性の腎性貧血の患者さんにとってHIF-PH阻害薬は期待される薬剤です。
経口投与が可能な薬剤ということで投与しやすくなる一方、腎性貧血はHb濃度の管理に注意が必要な疾患です。
急激なHb濃度上昇や高値になることを防ぎつつ治療を行なっていく必要があるため、ESA投与と同じく定期的にHb濃度を測定して管理を行なっていく必要があります。
ESA製剤は薬局で調剤する機会はありませんでしたが、HIF-PH阻害薬の登場により薬局も腎性貧血に深く関わっていくことになります。
しっかりと対応できるように勉強しておきたいですね。
乳幼児誤飲防止包装
グラクソ・スミスクラインの製品には乳幼児の誤飲を防ぐために、乳幼児には開けにくく、高齢者の使用性が確認された誤飲防止包装が採用されているものがあります。
ダーブロックにはプッシュスルータイプが採用されており、通常より強い力を加えないとPTPシートから錠剤を取り出せなくなっています。
http://glaxosmithkline.co.jp/crsf/healthcare/crsf/crsf_001.html
意図はわかるし、素晴らしい取り組みだと思うのですが、一包化する際に指が痛い。。。
新医薬品の投与制限が解除されると、指の痛みに悩まされそうです。。。
ダーブロック(ダプロデュスタット)の最新情報
m3.comに登録している方は検索機能を利用して「ダプロデュスタット」で検索すると下記のようなダーブロックに関する最新の臨床ニュースを閲覧することができます。
下記の記事ではダルベポエチンアルファに対するダプロデュスタットの貧血改善効果の非劣性についての海外論文について紹介されています。
今後、学会や論文などで新しい報告が出ればそれが記事として公開されるはずですから定期的にチェックしたいですね!
もし、m3.comに未登録の方がいればここをクリックして登録をお願いします。
参考資料
- ダーブロック錠 添付文書 グラクソ・スミスクライン株式会社
- ダーブロック錠 インタビューフォーム グラクソ・スミスクライン株式会社
- ダーブロック錠に係る医薬品リスク管理計画書 グラクソ・スミスクライン株式会社
- ダーブロック錠 審議結果報告書 医薬・生活衛生局医薬品審査管理課
- 日本腎臓学会編.CKD 診療ガイド 2012,東京医学社, 2012.
- 日本腎臓学会編.エビデンスに基づくCKD 診療ガイドライン 2018,東京医学社, 2018.
- 日本透析医学会:2015年版慢性血液透析患者における腎性貧血治療のガイドライン.透析会誌49:89-158,2016.(2015 JSDT Guideline for Renal Anemia in Chronic Kidney Disease)
- KDIGO 2012 clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int 2013;Suppl 3:1‒150.
- 日本透析医学会雑誌 49 巻 2 号 2016
- Semenza GL. Defining the role of hypoxia-inducible factor 1 in cancer biology and therapeutics. Oncogene. 2010;29:625-634.
- Semenza GL. Hypoxia-Inducible Factors in Physiology and Medicine. Cell. 2012;148:399-408.
- Kraus A, et al. HIF-1α promotes cyst progression in a mouse model of autosomal dominant polycystic kidney disease. Kidney International. 2018;94:887-899.
- Hofherr A, et al. HIF-1α drives cyst growth in advanced stages of autosomal dominant polycystic kidney disease. Kidney International. 2018;94:849-851.
- Mohanram A, Zhang Z, Shahinfar S, Keane WF, Brenner BM, Toto RD. Anemia and end-stage renal disease in patients with type 2 diabetes and nephropathy. Kidney Int 2004;66:1131.(RENAAL試験)
- Drüeke TB,Locatelli F,Clyne N,Eckardt KU,Macdougall IC,Tsakiris D,Burger HU,Scherhag ;CREATE Investigators. Normalization of hemoglobin level in patients with chronic kidney disease and anemia. N Engl J Med2006;355:2071-2084.(CREATE 研究)
- Singh AK,Szczech L,Tang KL,Barnhart H,Sapp S,Wolfson M,Reddan D;CHOIR Investigators. Correction of anemia with epoetin alfa in chronic kidney disease. N Engl J Med 2006;355:2085- 2098.(CHOIR研究)
- 日本腎臓学会 HIF-PH阻害薬適正使用に関するrecommendation 2020年9月29日版
- エベレンゾ錠 添付文書 アステラス製薬株式会社
- バフセオ錠 添付文書 田辺三菱製薬株式会社
- エナロイ錠 添付文書 日本たばこ産業株式会社
*1:HIF-Prolyl Hydroxylase Inhibitor
*2:ErythroPOietin
*3:Erythropoiesis Stimulating Agent
*4:HIF-Prolyl Hydroxylase
*5:Chronic Kidney Disease
*6:End-Stage Kidney Disease
*7:CardioVascular Disease
*8:HemoDialysis
*9:Peritoneal Dialysis
*10:Non-Dialysis
*11:aryl hydrocarbon receptor nuclear translocator
*12:Prolyl HyDroxylas
*13:Divalent Metal Transporter 1
*14:Duodenal cytochrome b
*15:Pure Red Cell Aplasia
*16:Major Adverse Cardiovascular Events
*17:Autosomal Dominant Polycystic Kidney Disease
*18:Polycystic Kidney Disease
*19:Autosomal Recessive Polycystic Kidney Disease