2020年6月29日に承認された気管支喘息治療薬 アテキュラ吸入用カプセルについてまとめた記事です。アテキュラ吸入用カプセルはLABA*1/ICS*2 2剤配合吸入薬で気管支喘息の適応を有する薬剤です。
同時に承認されたエナジア吸入用カプセル(LAMA/LABA/ICS)からLAMAであるグリコピロリウムを除いたものです。
2020年6月29日に承認された気管支喘息治療薬 エナジア吸入用カプセルについてまとめた記事です。 エナジア吸入用カプセルはLABA*1/LAMA*2/ICS*3 3剤配合吸入薬としてはテリルジー、ビレーズトリに続いて3番手になりますが、[…]
アテキュラについて
まずはアテキュラについて簡単に紹介します。
アテキュラってどんな薬?
アテキュラ吸入用カプセルは吸入デバイスにブリーズヘラーを用いた吸入薬です。LABAとしてインダカテロール酢酸塩、ICSとしてモメタゾンフランカルボン酸エステル(IND*3/MF*4)を含有するLABA/ICS 2剤配合吸入薬で気管支喘息の適応を持つ薬剤です。
ブリーズヘラーを吸入デバイスにICS(モメタゾンフランカルボン酸エステル)単剤を成分とした薬剤は存在しませんが、同じノバルティスが発売しているアズマネックスツイストヘラーがモメタゾンフランカルボン酸エステルを成分とするICS単剤の吸入薬に該当します。インダカテロール酢酸塩はオンブレス吸入用カプセル(インダカテロールマレイン酸塩)としてLABA単剤を成分としたものが発売されていますが、オンブレスは気管支喘息の適応はなく、慢性閉塞性肺疾患(COPD*5)のみの適応です。
同時に承認されたエナジア吸入用カプセル(IND*6/GLY*7/MF*8)との違いも含めて、アテキュラ吸入用カプセルについて解説していきます。
アテキュラの基本情報
基本情報をまとめます。
| 医薬品名 | アテキュラ吸入用カプセル低用量 アテキュラ吸入用カプセル中用量 アテキュラ吸入用カプセル高用量 |
|---|---|
| 開発コード | QMF149 |
| 成分名 | インダカテロール酢酸塩/モメタゾンフランカルボン酸エステル |
| 英語名 | Atectura low dose inhalation powder with hard capsules Atectura medium dose inhalation powder with hard capsules Atectura high dose inhalation powder with hard capsules (Indacaterol Acetate/Mometasone Furoate) |
| 製造販売元 | ノバルティスファーマ株式会社 |
| 命名の由来 | architectやarchitectureを由来としてAtectura(アテキュラ) |
| 効能・効果 | 気管支喘息 (吸入ステロイド剤及び長時間作用性吸入β2刺激剤の併用が必要な場合) |
| 用法・用量 | 通常、成人にはアテキュラ吸入用カプセル低用量1回1カプセル(インダカテロールとして150μg及びモメタゾンフランカルボン酸エステルとして80μg)を1日1回本剤専用の吸入用器具を用いて吸入する。 なお、症状に応じて以下用量の1回1カプセルを1日1回本剤専用の吸入用器具を用いて吸入する。 ・アテキュラ吸入用カプセル中用量(インダカテロールとして150μg及びモメタゾンフランカルボン酸エステルとして160μg) ・アテキュラ吸入用カプセル高用量(インダカテロールとして150μg及びモメタゾンフランカルボン酸エステルとして320μg) |
| 指定等 | なし |
| 審議 | 2020年5月28日付で議決の薬食審第二部会 (新型コロナウイルスの影響でweb会議で実施) |
| 承認日 | 2020年6月29日 |
| 薬価収載日 収載時薬価 | 2020年8月26日 アテキュラ吸入用カプセル低用量:157.80円/カプセル アテキュラ吸入用カプセル中用量:173.10円/カプセル アテキュラ吸入用カプセル高用量:192.20円/カプセル |
| 薬価算定方式 | 類似薬効比較方式(Ⅱ) アドエア100ディスカス60吸入用(薬価:6,351.10円/キット)の1日薬価211.70円を元にアテキュラ吸入用カプセル低用量の薬価157.80円/カプセル(1日薬価157.80円)を算出 アズマネックスツイストへラー200μg60吸入とアズマネックスツイストへラー100μg60吸入の規格間比0.32520を元にアテキュラ吸入用カプセル中用量とアテキュラ吸入用カプセル高用量の薬価を算出 |
| 販売開始 | 2020年8月26日(薬価収載即日発売) |
| 新医薬品の 投与日数制限 | 対象(2021年8月末日まで) |
単剤と薬価(2020.8.26)を比較
アテキュラ(IND/MF)と成分・成分量が同等になる組み合わせをまとめます。
- アテキュラ高用量(IND/MF)=オンブレス(IND)+アズマネックス(MF)800μg相当
- アテキュラ中用量(IND/MF)=オンブレス(IND)+アズマネックス(MF)400μg相当
- アテキュラ低用量(IND/MF)=オンブレス(IND)+アズマネックス(MF)200μg相当
関連する医薬品の薬価(2020.8.26)はそれぞれ以下の通りです。
- アズマネックスツイストヘラー200μg60吸入:2935.40円/キット
(800μg相当:195.70円、400μg相当:97.85円、200μg相当:48.92円) - オンブレス吸入用カプセル150μg:139.40円/カプセル
これらを元に1日薬価(2020.8.26)を比較すると・・・
- アテキュラ高用量 192.20円
- オンブレス+アズマネックス800μg相当 335.1円
- アテキュラ中用量 173.10円
- オンブレス+アズマネックス400μg相当 237.25円
- アテキュラ低用量 157.80円
- オンブレス+アズマネックス200μg相当 188.32円
合剤であるアテキュラは1度で吸入が済むだけでなく薬価の面でもメリットがあることがわかりますね。
気管支喘息とアテキュラの作用機序
気管支喘息についての基礎知識とアテキュラの作用機序についてまとめていきます。
気管支喘息とは?
2014年(平成26年)の厚生労働省による病院及び診療所における患者調査によると喘息患者数は約118万人と報告されています。1990年代には喘息によって年間6,000人が死亡していましたが、ICSやLABAの普及により死亡率は減少しており、2016年(平成28年)には年間1,500人まで減少しています。気管支喘息による死亡を減らすため、新規薬剤の開発や適切な治療が推進されています。
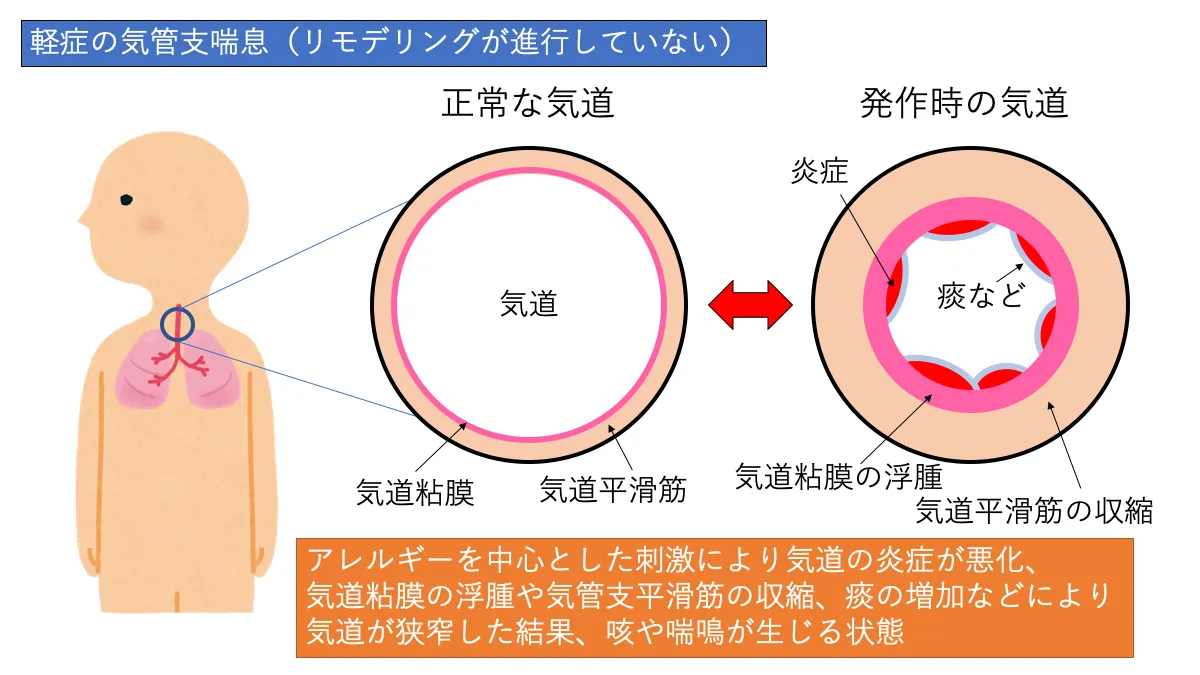
気管支喘息は喘息予防・管理ガイドライン2018で「気道の慢性炎症を本態として、変動性を持った気道狭窄(喘鳴、呼吸困難)や咳などの臨床症状で特徴付けられる疾患」と定義されています。気管支喘息では、アレルギーなどの刺激により「気道平滑筋の収縮」、「粘膜の浮腫」、「痰などの分泌物の増加」が起こり、気道狭窄が起こります。その結果、息苦しさや喘鳴、激しい咳と言った症状が起きます。
気道リモデリングによる症状の悪化
気管支喘息では発作時以外にも慢性的に気道炎症が起きています。無治療の状態では慢性炎症や発作による気道組織の破壊と修復が繰り返され、組織の繊維化が進んでいきます。これを気道リモデリングと言います。
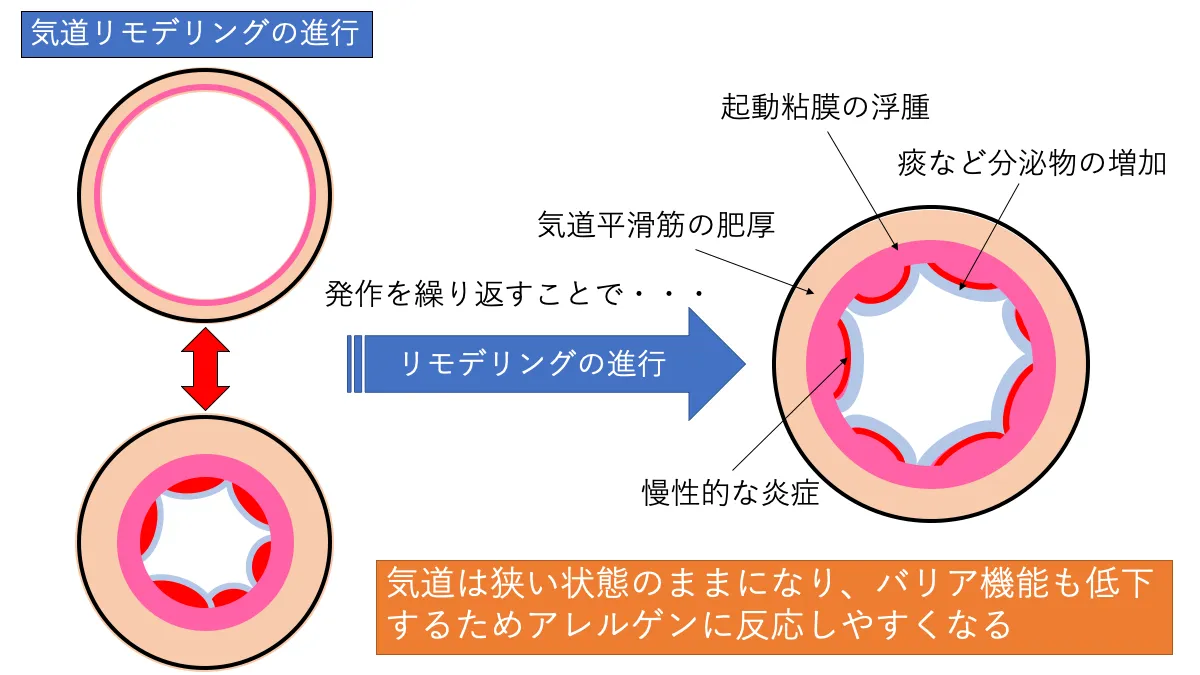
気道平滑筋が肥厚することで気道は狭くなり、組織が柔軟性を失うことで過敏性が亢進します。このように気道リモデリングが進むことで気管支喘息は重症化し、発作を起こしやすく、その症状も重篤なもの(呼吸困難等)になっていきます。
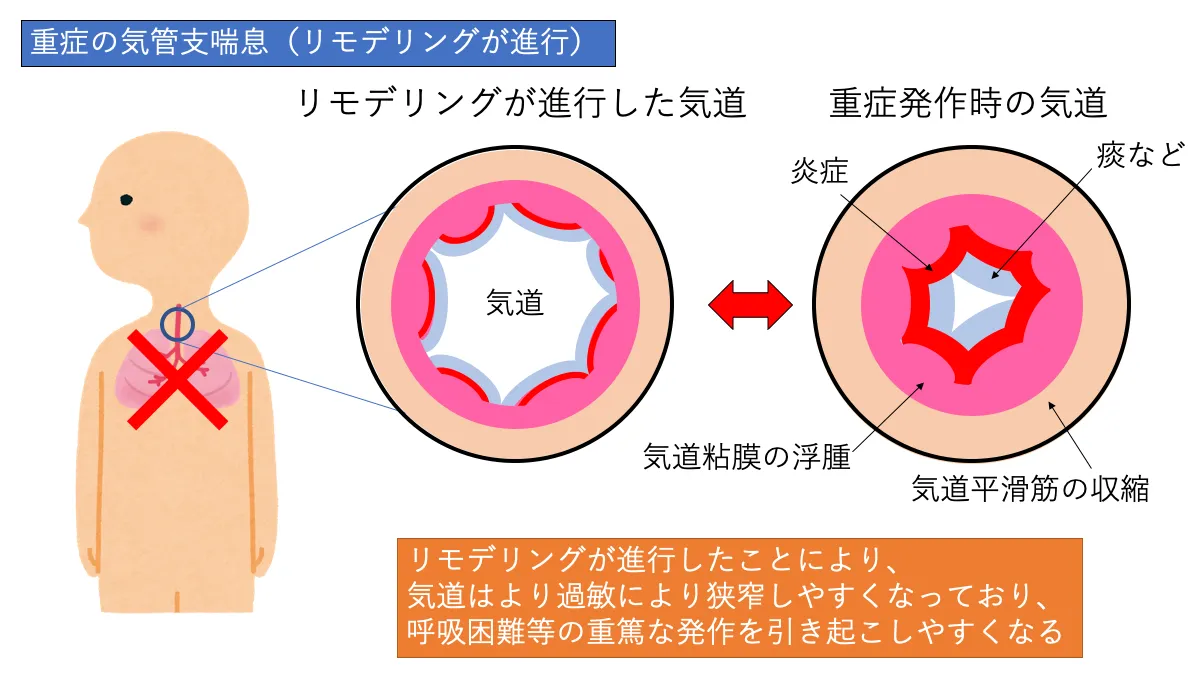
そのため、気管支喘息では発作を予防し、気道リモデリングを進行させないための治療が重要になります。
気管支喘息では「気道の炎症」「気道リモデリング」「気道過敏性の亢進」の3つの特徴が相互に影響しあって「気道の狭窄」を引き起こすという考えが重要になります。
気管支喘息の治療
気管支喘息の治療では喘息発作を起こさないこと(症状のコントロール)を目標に長期管理薬(コントローラー)による治療が行われます。喘息発作時には短期的に発作治療薬(リリーバー)が使用されます。
喘息の症状により治療ステップが分けられており、治療ステップごとにコントローラーとして使用される薬剤が定められています。(ICSによる治療がどのステップでも基本となっています)以下に示すように「喘息予防・管理ガイドライン2018」では新たにLAMAがステップ2に加わっています。
| 分類 | ステップ1 | ステップ2 | ステップ3 | ステップ4 | |
|---|---|---|---|---|---|
| 長期管理薬 | 基本治療 | ICS 低用量 | ICS 低〜中用量 | ICS 中〜高用量 | ICS 高用量 |
| ICSが使用できない場合、 以下のいずれかを用いる LTRA テオフィリン徐放製剤 ※症状が稀なら不要 | ICSで不十分な場合、 以下のいずれか1剤を併用 LABA(配合剤使用可) LAMA LTRA テオフィリン徐放製剤 | 以下のいずれか1剤、 もしくは複数を併用 LABA(配合剤使用可) LAMA LTRA テオフィリン徐放製剤 | 下記の複数を併用 LABA(配合剤使用可) LAMA LTRA テオフィリン徐放製剤 抗IgE抗体 抗IL-5抗体 抗IL-5α抗体 抗ステロイド薬 気管支熱形成術 | ||
| 追加治療 | LTRA以外の抗アレルギー薬 | ||||
| 発作治療 | SABA | ||||
ICSの作用機序
アテキュラ吸入用カプセルの成分の一つであるモメタゾンフランカルボン酸エステル(MF)は副腎皮質ステロイド(吸入薬なのでICS)です。副腎皮質ステロイド(corticosteroids)とは糖質ステロイド(Glucocorticoids、グルココルチコイド)のことを指します。糖質コルチコイドは吸入されることで気道の炎症細胞に到達し抗炎症作用を発揮します。
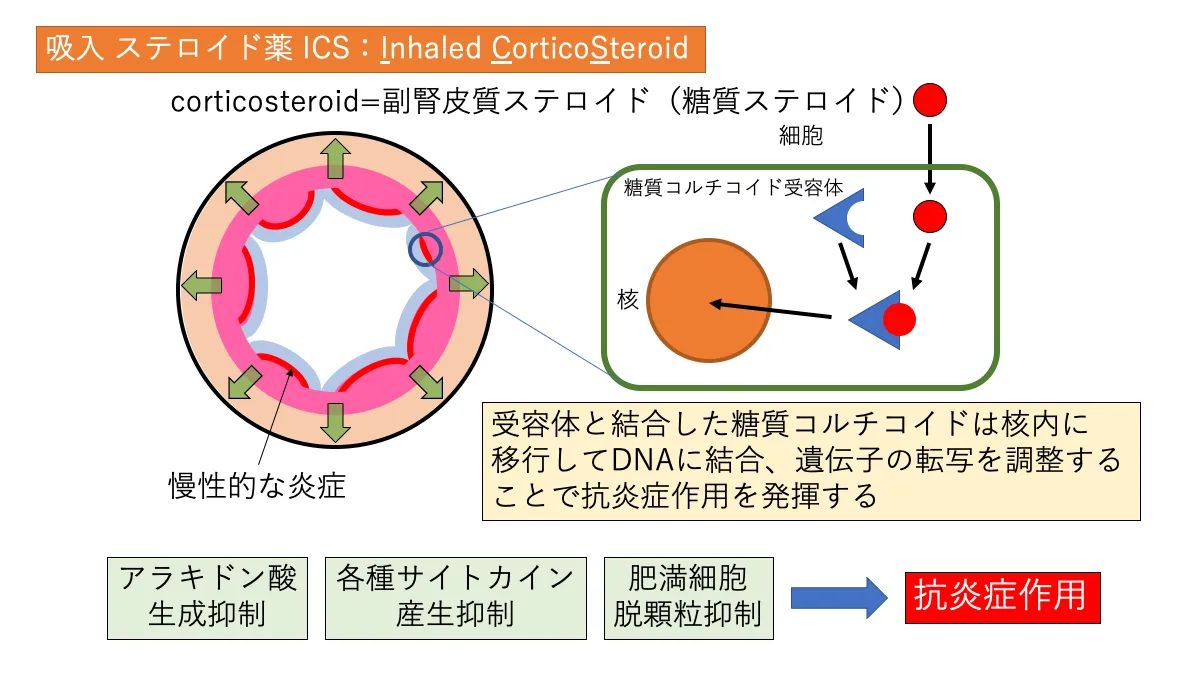
糖質コルチコイドは細胞内で糖質コルチコイド受容体(グルココルチコイドレセプター)と結合します。糖質コルチコイドは受容体と結合することで核内に進入し、DNAと結合しその転写を調節し、以下のような作用により抗炎症作用を発揮します。
- ホスホリパーゼA2(PLA2*11)の阻害→アラキドン酸の生成抑制
- サイトカインの産生抑制
- 肥満細胞(マスト細胞)の脱顆粒抑制
モメタゾンフランカルボン酸エステルの特徴
モメタゾンフランカルボン酸エステル(MF)は古くから使用されている成分で吸入薬以外ではフルメタ軟膏(very strong)やナゾネックス点鼻液の成分として使用されています。吸入薬としては以下の医薬品で使用されています。
- アズマネックスツイストヘラー
MFはグルココルチコイド受容体に対する親和性が高く、強い局所抗炎症作用を示します。全身吸収性が極めて低いため安全性が高いと言われています。
気管支拡張薬(LABA)の作用機序
アテキュラ吸入用カプセルには長時間作用性β2受容体刺激薬(LABA)としてインダカテロール酢酸塩が含まれています。LABAは気道平滑筋を弛緩することで、気管支拡張作用を発揮します。
気道平滑筋細胞にはβ2受容体が存在しており、刺激を受けると以下のような流れで気道平滑筋が弛緩されます。
- 気道平滑筋細胞にのβ2受容体刺激
- アデニル酸シクラーゼの活性化
- 細胞内cAMP濃度の上昇
- プロテインキナーゼAの活性化
- 気道平滑筋の弛緩
LABAが登場する前のβ2刺激薬はサルブタモール硫酸塩(サルタノール/ベネトリン)、プロカテロール塩酸塩水和物(メプチン)に代表されるSABA*10(短時間作用型β2刺激薬)のみでした。SABAという呼び名からも分かるように効果が短いためリリーバー(発作治療薬)として使用されていました。
その後、LABAが開発され、今では気管支喘息や慢性閉塞性肺疾患(COPD((Chronic Obstructive Pulmonary Disease)の治療薬(コントローラー)として広く使用されています。LABAの持つ疎水性の側鎖はβ2受容体の非活性部位に強力に結合します。その状態で親水性部分が受容体の活性部位に結合することで、長時間にわたってβ2受容体を刺激します。
LABAは気道平滑筋のβ2受容体を刺激する直接的な作用に加えて、コリン作動性神経終末のβ2受容体を刺激することによりアセチルコリンの遊離を抑制(ムスカリンM3受容体の刺激を抑制)して間接的な作用で気道を拡張します。

インダカテロール酢酸塩の特徴
インダカテロールは日本で最初に承認されたultra-LABA(24時間以上効果を発揮するLABA)です。β2受容体が多く発現するラフト脂質への親和性が高いため、気道平滑筋細胞に長時間留まることができると考えられています。作用発現が速やか(サルブタモールと同程度)なため、効果を実感しやすいとされています。
β2刺激薬の作用発現時間
- インダカテロール:7.8±0.7分
- ホルモテロール:5.8±0.7分
- サルメテロール:19.4±4.3分
- サルブタモール:11.0±4.0分
単離ヒト気管支に対してβ2刺激薬を投与した際の作用発現時間(Naline E, et al. Eur Respir J. 2007;29:575-581.)
インダカテロール酢酸塩とマレイン酸塩
アテキュラ吸入用カプセル、エナジア吸入用カプセルに採用されたインダカテロールは酢酸塩ですが、それ以前のもの(オンブレス吸入用カプセル、ウルティブロ吸入用カプセル)ではマレイン酸塩でした。インダカテロール酢酸塩とインダカテロールマレイン酸塩の有効性は同等であることが申請資料概要に記載されています。
2.6.1 緒言
インダカテロール酢酸塩及びインダカテロールマレイン酸塩の有効性は臨床薬理試験において同様であることが確認されている(QVM149B2203試験)
2.7.1 生物薬剤学試験及び関連する分析法
インダカテロール酢酸塩とマレイン酸塩は薬物動態的に同様であると考えられる。
引用元:エナジア吸入用カプセル中用量 同吸入用カプセル高用量に関する資料 ノバルティスファーマ株式会社
ということで、エナジアとアテキュラで採用されているインダカテロール酢酸塩はオンブレスやウルティブロに使用されているインダカテロールマレイン酸塩と同じ有効性、動態を持つものと考えてOKです。わざわざインダカテロールマレイン酸塩からインダカテロール酢酸塩に変えた理由ですが、EMS2019でノバルティスによる「Lung function, pharmacokinetics, and tolerability of indacaterol maleate and acetate in asthma patients」という発表が行われており、それによるとインダカテロールマレイン酸塩とインダカテロール酢酸塩の有効性には差はなかったが、インダカテロールマレイン酸塩に見られる咳の副作用はインダカテロール酢酸塩では起こりにくいことを示唆する結果が得られています。
配合吸入薬を用いるメリットは?
配合剤にすることで1回でまとめて使用できるため、使用が容易になり使用忘れも防ぐことができます。内服に比べて手技が煩雑な吸入薬ではこのメリットがより大きくなります。また、LABA、ICS(、LAMA)はそれぞれ単独で使用した場合と比較して併用することで効果が強くなることが知られてます。
ICS/LABA
ICS単剤とLABA単剤を併用した場合と比較して、ICS/LABA配合剤を使用した方が効果が強くなることが知られています。ICSはβ2受容体とGsタンパク質の発現を誘導することが知られています。この効果により細胞表面上のβ2受容体が増加するため、LABAの効果が増強されると同時に、LABAの長期使用に伴うβ2受容体のダウンレギュレーションを抑制することができます。また、LABAはグルココルチコイド受容体の核内移行を促進するため、ICSの抗炎症作用を増強します。
配合吸入薬として使用することでICSとLABAが同一細胞に到達することでこの相互作用が効率よく発揮できるのはないかと考えられています。
吸入器の特徴
吸入薬にとって成分と同じくらい重要なのが吸入器(吸入デバイス)です。それぞれの特徴を紹介した上でアテキュラ吸入用カプセルの吸入デバイスであるブリーズヘラーについて説明します。
DPI製剤とpMDI製剤
吸入デバイスは以下の2つに大きく分類されます。
それぞれの基本的な特徴を簡単にまとめます。(現在は欠点を改良した製剤も存在します)
・残量が分かり易い
・噴霧との同期が不要(スペーサーが不要)
・刺激性添加物を含まない
欠点
・吸入前に操作が必要なものが多い
・嗄声が比較的多い
・吸入流速が低いと薬剤が肺内に到達しない
・すぐに使用可能
・吸入流速が低くても使用可能
・嗄声を起こしにくい
欠点
・残量が分かりにくいものがある
・噴霧と吸気を同調させる必要がある
・口腔内に沈着しやすい
pMDIの同調が困難な場合はスペーサーを用いることがあります。
吸入デバイスと吸入流速
各デバイスが必要とする吸入流速をまとめます。
| 吸入デバイス | 製品名 | 吸入流速(L/min) |
| ディスクヘラー (ロタディスク) | フルタイド セレベント | 30〜60 |
| ディスカス | フルタイド セレベント アドエア | 30 |
| タービュヘイラー | パルミコート シムビコート オーキシス | 30 |
| ハンディヘラー | スピリーバ | 20 |
| ツイストヘラー | アズマネックス | 20〜30 |
| ブリーズヘラー | オンブレス シーブリ ウルティブロ エナジア アテキュラ | 20 |
| エリプタ | レルベア アノーロ エンクラッセ アニュイティ テリルジー | 30〜36 |
| ジェヌエア | エリクラ | 45 |
| スイングヘラー | メプチン | 20 |
※pMDI(エアゾール)製剤やレスピマット製剤は10L/min以上あれば吸入可能
図にすると以下のようになります。

ブリーズヘラーは最大吸気流量が低下している場合でも比較的使用しやすい吸入デバイスになります。
ブリーズヘラーの特徴
アテキュラ吸入用カプセルは吸入デバイスにブリーズヘラーを用いる薬剤です。
シートからカプセルを取り出し、ブリーズヘラーにセットし、側面のボタンを押し込みことでカプセルに穴を開けます。
吸入口を加えて息を吸い込み、必要な吸入流速に達すると、内部でカプセルが回転し薬剤が吸入口から放出され肺に到達します。
カプセルをセットする手間がかかるのと誤飲に対して注意する必要がありますが、カプセルが回転する音と吸入後にカプセルの中身を確認することで吸入できているかどうかを確認することが可能なのは大きなメリットです。
ブリーズヘラーは吸入抵抗が少ない構造となっているため、前述したとおり、最大吸気流量が低下している場合でも使用しやすくなっています。
アテキュラ吸入用カプセルのDI
ここからはアテキュラ吸入用カプセルの添付文書、インタビューフォーム、RMP、審査結果報告書から得ることのできる情報についてまとめていきたいと思います。
禁忌
まずは禁忌についてです。
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 有効な抗菌剤の存在しない感染症、深在性真菌症の患者[ステロイドの作用により症状を悪化させるおそれがある。]
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
「閉塞隅角緑内障」、「前立腺肥大等による排尿障害」はグリコピロニウム、「有効な抗菌剤の存在しない感染症、深在性真菌症」はモメタゾンフランカルボン酸エステル由来の禁忌ですね。
中用量/高用量で異なるのはMFの量
アテキュラ吸入用カプセルは中用量と高用量の2規格が存在しており、異なるのはモメタゾンフランカルボン酸エステル(MF)の量です。
| 成分名 | アテキュラ吸入用カプセル | ||
| 低用量 | 中用量 | 高用量 | |
| インダカテロール | 150μg | 150μg | 150μg |
| モメタゾンフランカルボン酸エステル | 80μg | 160μg | 320μg |
アテキュラ吸入用カプセルをブリーズヘラーで吸入した際のMFの全身暴露量をMF単独を有効成分とするアズマネックスツイストヘラーのものと比較すると以下のようになります。
- アテキュラ吸入用カプセル低用量(MF 80μg)=アズマネックスツイストヘラー200μg
- アテキュラ吸入用カプセル中用量(MF 160μg)=アズマネックスツイストヘラー400μg
- アテキュラ吸入用カプセル高用量(MF 320μg)=アズマネックスツイストヘラー800μg
エナジアとはモメタゾンの量で比較しないように注意
アテキュラが低用量/中用量/高用量の3規格なのに対して、エナジア吸入用カプセル(インダカテロール酢酸塩/グリコピロリウム臭化物/モメタゾンフランカルボン酸エステル)は中用量/高用量の2規格が存在します。とてもややこしい話になるのですが、アテキュラ中用量とエナジア中用量、アテキュラ高用量とエナジア高用量では含有されるMFの量が異りますが、効果が期待できるMFの量は同じです。
このことは添付文書にも記載されています。
3. 組成・性状
3.1 組成
※:モメタゾンフランカルボン酸エステルの配合量は、本剤中用量とエナジア吸入用カプセル中用量で、また本剤高用量とエナジア吸入用カプセル高用量でそれぞれ異なるが、肺に到達し薬効発現が期待されるモメタゾンフランカルボン酸エステルの粒子量は、中用量同士、高用量同士で同程度である。(エナジア吸入用カプセル:インダカテロール酢酸塩、モメタゾンフランカルボン酸エステル及びグリコピロニウム臭化物の配合剤)
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
エナジアのインタビューフォームにはもう少し詳しく記載されています。
V.治療に関する項目
V-3. 用法及び用量
(2)用法及び用量の設定 経緯・根拠
(4) 本剤に配合する各配合成分の用法及び用量
In vitro試験及びアテキュラ®投与時の薬物相互作用試験(QMF149E2102試験)において、インダカテロール及びMFの2有効成分間に相互作用が認められなかったことから、ブリーズヘラー®使用時のアテキュラ®に配合するMFの用量を80μg(低用量)、160μg(中用量)及び320μg(高用量)と決定した。一方、本剤では、MFのFPM(肺へ到達可能な微粒子量)が増加したことから、本剤とアテキュラ®のMFのFPMを同等とするため、本剤に配合するMFの用量を80μg(アテキュラ®中のMF160μgに相当)、160μg(アテキュラ®中のMF320μg に相当)に調整した。外国人健康被験者を対象とした本剤の薬物相互作用試験(外国QVM149B2102試験)では、本剤投与時と各単剤投与時で定常状態における各有効成分の全身曝露量は同程度であり、本剤の3有効成分間に相互作用が認められなかったことなどから、本剤の各有効成分の用量を150/50/80μg(中用量)及び150/50/160μg(高用量)とし、用法は1日1回吸入投与とした。
引用元:エナジア吸入用カプセル インタビューフォーム ノバルティスファーマ株式会社
合剤になるとMFの肺到達率が増加する・・・これは添加物の違いがポイントのようです。
ポイントとなるのはグリコピロニウムに使用される添加剤
ブリーズヘラーをデバイスとする吸入剤に使用されている添加剤は乳糖とステアリン酸マグネシウムです。
添加剤で薬剤を分類すると以下のようになります。
- 添加剤:乳糖水和物
- オンブレス(IND)
- アテキュラ(IND/MF)
- 添加剤:乳糖水和物、ステアリン酸マグネシウム
- シーブリ(GLY)
- ウルティブロ(GLY/IND)
- エナジア(GLY/IND/MF)
ご覧の通り、グリコピロニウムを含む製剤には添加剤としてステアリン酸マグネシウムが使用されています。
このステアリン酸マグネシウムがMFのFPMを増加させているようです。オンブレス(IND 150μg)とウルティブロ(IND 110μg)でインダカテロールの量が異なるのも同じ理由です。
MF含有量の比較
アテキュラ、エナジア、アズマネックスを比較すると以下のようになります。
| アズマネックス MF量 | アテキュラ (MF量) | エナジア (MF量) |
| 200μg | 低用量 (80μg) | – |
| 400μg | 中用量 (160μg) | 中用量 (80μg) |
| 800μg | 高用量 (320μg) | 高用量 (160μg) |
効能・効果と用法・用量
基本的な部分ですが少し詳しく見ておきます。
現時点での適応は気管支喘息のみ
4. 効能又は効果
気管支喘息(吸入ステロイド剤及び長時間作用性吸入β2刺激剤の併用が必要な場合)
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
現時点で適応は気管支喘息のみで慢性閉塞性肺疾患(COPD)に対する適応は取得していません。ですが、COPDでICSを使用するのは喘息病態合併(ACO*13)が基本となっています。
アテキュラは喘息を合併しているACOには当然使用可能なので、ガイドライン通りに使用するのであれば気管支喘息のみの適応でCOPDまでカバーできることになりますね。もちろん、その場合はエナジアを使用することになるとは思いますが・・・。
あくまでもコントローラーとして使用する薬剤
当然ですが、アテキュラはコントローラーとして使用される薬剤でリリーバーとして使用することはできません。
5. 効能又は効果に関連する注意
患者に対し、次の注意を与えること。
本剤は発現した発作を速やかに軽減する薬剤ではないので、急性の発作に対しては使用しないこと。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
このことを含めてコントローラーとしての注意点が「重要な基本的注意」にも記載されています。
8. 重要な基本的注意
8.1 本剤は喘息の急性症状を速やかに軽減する薬剤ではないので、毎日規則正しく使用するよう患者を指導すること。
8.2 本剤の投与期間中に発現する気管支喘息の急性の発作に対しては、短時間作用性吸入β2刺激剤等の他の適切な薬剤を使用するよう患者に注意を与えること。
また、その薬剤の使用量が増加したり、あるいは効果が十分でなくなってきた場合には、疾患の管理が十分でないことが考えられるので、可及的速やかに医療機関を受診し医師の治療を求めるよう患者に注意を与えること。
そのような状態では患者の生命が脅かされる可能性があるので、患者の症状に応じてステロイド療法の強化(本剤のより高い用量への変更等)を考慮すること。
8.3 本剤の投与終了後に症状の悪化があらわれることがあるので、患者自身の判断で本剤の使用を中止することがないよう指導すること。また、投与を中止する場合には観察を十分に行うこと。
8.4 本剤の投与期間中に喘息に関連した事象及び喘息の悪化があらわれることがある。本剤の投与開始後に喘息症状がコントロール不良であったり、悪化した場合には、患者自身の判断で本剤の吸入を中止せずに、医師に相談するよう指導すること。
8.5 本剤は患者の喘息症状に応じて最適な用量を選択する必要があるため、本剤の投与期間中は患者を定期的に診察すること。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
発作時はSABA等を使用し、発作が改善しないようであれば速やかに受診してコントローラーの処方を見直してもらう必要があります。症状が改善したり、安定していても油断せず治療を継続し、定期的に診察を行うことが必要です。
用法・用量と注意点
6. 用法及び用量
通常、成人にはアテキュラ吸入用カプセル低用量1回1カプセル(インダカテロールとして150μg及びモメタゾンフランカルボン酸エステルとして80μg)を1日1回本剤専用の吸入用器具を用いて吸入する。
なお、症状に応じて以下用量の1回1カプセルを1日1回本剤専用の吸入用器具を用いて吸入する。
・アテキュラ吸入用カプセル中用量(インダカテロールとして150μg及びモメタゾンフランカルボン酸エステルとして160μg)
・アテキュラ吸入用カプセル高用量(インダカテロールとして150μg及びモメタゾンフランカルボン酸エステルとして320μg)7. 用法及び用量に関連する注意
7.1 本剤は吸入用カプセルであり、必ず本剤専用の吸入用器具(ブリーズヘラー®)を用いて吸入し、内服しないこと。
7.2 本剤は1日1回、時間を問わず一定の時間帯に吸入すること。吸入できなかった場合は、可能な限り速やかに1回分を吸入すること。ただし1日1回を超えて吸入しないこと。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
カプセルという剤形の薬剤なので誤飲しないように注意することが必須になります。また、吸入し忘れた場合は当日中であれば速やかに吸入するように記載されています。
吸入薬であり内服しないという注意点については「適用上の注意」にも記載されています。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 吸入前
(1) 医療従事者は、患者に専用の吸入用器具(ブリーズヘラー®)及び使用説明文書を渡し、正しい使用方法を十分に指導すること。また、呼吸状態の改善が認められない場合には、本剤を吸入せずに内服していないか確認すること。
(2) 吸入の直前にブリスター(アルミシート)からカプセルを取り出すように指導すること。
(3) 本剤のカプセル内容物は少量であり、カプセル全体に充填されていない。
14.1.2 吸入時
本剤は吸入用カプセルであり、必ず専用の吸入用器具(ブリーズヘラー®)を用いて吸入し、内服しないこと。
14.1.3 吸入後
局所的な副作用(カンジダ症又は発声障害等)を予防するため、本剤吸入後に、うがいを実施するよう患者を指導すること。ただし、うがいが困難な場合には、口腔内をすすぐよう指導すること。また、口に含んだ水を飲み込まないよう指導すること。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
ICSでは吸入後のうがいは必須ですね。
各成分に由来する注意点
添付文書の「重要な基本的注意」と「特定の背景を有する患者に関する注意」に記載されている注意点をまとめてみます。
8. 重要な基本的注意
8.7 本剤の吸入により気管支痙攣が誘発され生命を脅かすおそれがある。気管支痙攣が認められた場合は、直ちに投与を中止し、適切な処置を行うこと。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
気管支痙攣は吸入薬である以上、避けることのできない注意点です。
ここからは各成分に由来するものなのでそれぞれにまとめていきます。
ICS由来の注意点
まずはICS(モメタゾンフランカルボン酸)由来の注意点をまとめます。
吸入薬であるため全身への暴露量は少なくなっていますが、長期に渡って使用する薬剤であるため注意が必要になります。
8. 重要な基本的注意
8.6 全身性ステロイド剤と比較し可能性は低いが、吸入ステロイド剤の投与により全身性の作用(クッシング症候群、クッシング様症状、副腎皮質機能抑制、小児の成長遅延、骨密度の低下、白内障、緑内障を含む)が発現する可能性があるので、吸入ステロイド剤の投与量は患者毎に喘息をコントロールできる最少用量に調節すること。特に長期間、高用量投与の場合には定期的に検査を行い、全身性の作用が認められた場合には患者の喘息症状を観察しながら適切な処置を行うこと。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
ステロイドには免疫抑制作用もあるため感染症、特に呼吸器系の悪化には注意が必要となります。
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 結核性疾患又は感染症(有効な抗菌剤の存在しない感染症、深在性真菌症を除く)の患者
症状を悪化させるおそれがある。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
LABA由来の注意点
次にLABA(インダカテロール)由来の注意点。
β2受容体選択性が高いと言ってもβ1受容体への影響は完全には否定できませんし、長期に渡って使用する薬剤であるため心臓に対しての副作用には注意が必要です。
8. 重要な基本的注意
8.8 過度に使用を続けた場合、不整脈、場合により心停止を起こすおそれがあるので、用法・用量を超えて使用しないよう注意すること。また、患者に対し、本剤の過度の使用による危険性を理解させ、1日1回を超えて使用しないよう注意を与えること。本剤の気管支拡張作用は通常24時間持続するので、その間は次の投与を行わないこと。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
以下の記載もβ2受容体刺激作用に由来するものです。
9. 特定の背景を有する患者に関する注意
9.1.2 甲状腺機能亢進症の患者
症状を悪化させるおそれがある。
9.1.3 心血管障害(冠動脈疾患、急性心筋梗塞、不整脈、高血圧、心不全、QT間隔延長等)の患者又はこれらの既往歴のある患者
症状を悪化させるおそれがある。
9.1.4 糖尿病の患者
血糖値をモニタリングするなど慎重に投与すること。高用量のβ2刺激剤又はステロイド剤を投与すると、血糖値が上昇するおそれがある。
9.1.5 てんかん等の痙攣性疾患のある患者
痙攣の症状を悪化させるおそれがある。
9.1.7 低酸素血症の患者
血清カリウム値に注意すること。低酸素血症により血清カリウム値の低下の心リズムに及ぼす影響が増強されることがある。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
LABAを含むβ受容体刺激薬はNa+/K+ATPaseを活性化させ細胞外カリウムを細胞内へ移動させるため低カリウム血症を増悪させるおそれがあります。
妊婦・授乳婦・小児
妊婦・授乳婦は有益性投与、小児適応は取得していません。
9. 特定の背景を有する患者に関する注意
9.5 妊婦
妊婦又は妊娠している可能性のある女性には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。モメタゾンフランカルボン酸エステルの経皮又は経口投与による動物実験(ラット、ウサギ)で催奇形性作用が報告されている。インダカテロールの動物実験(ウサギ)で骨格変異の発生率増加を伴う生殖発生毒性が報告されている。また、インダカテロールの動物実験(ラット)で胎盤通過性が報告されている。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。インダカテロール、モメタゾンフランカルボン酸エステルの動物実験(ラット)で乳汁中に移行することが報告されている。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
相互作用
吸入薬といえども3成分を含有しているのでどうしも相互作用の数は増えます。
10. 相互作用
インダカテロールは主に代謝酵素チトクロームP450 3A4(CYP3A4)で代謝され、またP糖蛋白(Pgp)の基質である。モメタゾンフランカルボン酸エステルの代謝にはCYP3A4が関与している。
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
これも成分ごとに分類してみます。
- インダカテロール
- CYP3A4阻害剤(エリスロマイシン等):エリスロマイシンの併用でCmax1.2倍、AUC1.4〜1.6倍(CYP3A4阻害による代謝阻害)
- P糖蛋白を阻害する薬剤(ベラパミル等):ベラパミルとの併用でCmax1.5倍、AUC1.4~2.0倍(P糖蛋白活性阻害による排泄阻害)
- リトナビル:AUC1.6〜1.8倍(CYP3A4及びP糖蛋白の活性阻害による代謝及び排泄の阻害)
- QT間隔延長を起こす薬剤(MAO阻害剤、三環系抗うつ剤等):心室性不整脈等のリスク増大(QT間隔を延長)
- 交感神経刺激剤:作用増強の可能性(アドレナリン作動性神経刺激を増大)
- キサンチン誘導体:低カリウム血症による心血管事象(不整脈)を起こすおそれ(アドレナリン作動性神経刺激を増大)
- ステロイド剤、利尿剤(サイアザイド系利尿剤、サイアザイド系類似利尿剤、ループ利尿剤):低カリウム血症による心血管事象(不整脈)を起こすおそれ(尿細管でのカリウム排泄促進作用)
- β遮断剤(点眼剤を含む):作用減弱の可能性(作用が拮抗される可能性)
- モメタゾンフランカルボン酸エステル
- CYP3A4阻害剤(エリスロマイシン等):ステロイド剤を全身投与した場合と同様の症状があらわれる可能性(CYP3A4阻害による代謝阻害)
気になる副作用は?
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
11.1.1 アナフィラキシー(頻度不明)
血管浮腫、呼吸困難、舌・口唇・顔面の腫脹、蕁麻疹、皮疹などがあらわれることがある。
11.1.2 重篤な血清カリウム値の低下(頻度不明)
11.1.3 心房細動(頻度不明)
引用元:アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
これら重大な副作用についてはこの後のRMPの項でまとめています。
「11.2 その他の副作用」で気になるのはやはり以下の内容でしょうか。
- 1%以上
- 発声障害(呼吸器、胸郭および縦隔障害)
- 筋痙縮(筋骨格系および結合組織障害)
- 1%未満
- カンジダ症(感染症および寄生虫症)
- 口腔咽頭痛(呼吸器、胸郭および縦隔障害)
LABA/ICS配合吸入薬ではお馴染みの副作用なので注意が必要ですね。
RMPに記載されている注意点
- 重要な特定されたリスク
- 心血管系事象
- アナフィラキシー
- 重篤な血清カリウム値の低下
- 重要な潜在的リスク
- 肺炎
- 副腎皮質ステロイド剤の全身作用(副腎皮質機能抑制、骨障害、眼障害等)
心血管系事象(重要な特定されたリスク)
心血管系事象の特定されたリスクには、虚血性心疾患、心筋梗塞、心不全、心房細動、頻脈性不整脈、不整脈(伝導異常、異所性興奮、非特異的不整脈等)、脳血管事象が含まれます。心血管系事象は以下の通り、LABAに由来するものと考えられています。
- β2刺激剤の吸入:薬理学的作用によるクラスエフェクト
| 心血管系事象 | アテキュラ中用量 | アテキュラ高用量 |
|---|---|---|
| 虚血性心疾患 | 1.0/100人年 | 0.7/100人年 |
| 心筋梗塞 | 報告なし | 0.5/100人年 |
| 不整脈 | 2.2/100人年 | 2.7/100人年 |
| QTc 延長及び QTc 延長を誘発すること が知られている薬剤との相互作用 | 0.5/100人年 | 0.5/100人年 |
| 脳血管事象 | 報告なし | 0.5/100人年 |
※心不全の報告はなし
| 心血管系事象 | アテキュラ中用量 | アテキュラ高用量 |
|---|---|---|
| 虚血性心疾患 | 0.5/100人年 | 0.7/100人年 |
| 心筋梗塞 | 0.3/100人年 | 0.5/100人年 |
| 心不全 | 0.3/100人年 | 報告なし |
| 不整脈 | 3.4/100人年 | 3.3/100人年 |
| 脳血管事象 | 0.5/100人年 | 0.9/100人年 |
※QTc延長及びQTc延長を誘発することが知られている薬剤との相互作用は報告なし
| 心血管系事象 | アテキュラ低用量 |
|---|---|
| 虚血性心疾患 | 2.2/100人年 |
※虚血性心疾患、心筋梗塞、心不全、QTc延長及びQTc延長を誘発することが知られている薬剤との相互作用、脳血管事象の報告はなし
以上を踏まえて重要な特定されたリスクに設定されています。
アナフィラキシー(重要な特定されたリスク)
| アテキュラ中用量 | アテキュラ高用量 | |
|---|---|---|
| アナフィラキシー反応※ | 1.5/100人年 | 1.5/100人年 |
| アテキュラ中用量 | アテキュラ高用量 | |
|---|---|---|
| アナフィラキシー反応※ | 0.2/100人年 | 1.4/100人年 |
| アテキュラ低用量 | |
|---|---|
| アナフィラキシー反応※ | 3.3/100人年 |
※集計に用いた事象名(MedDRA基本語):後天性C1インヒビター欠損、アレルギー 性浮腫、賦形剤アレルギー反応、アナフィラキシー反応、血管浮腫、口周囲浮腫、口周囲腫脹、使用製品に対する記録された過敏症、薬物過敏症、過敏症、特発性血管浮腫、喉頭浮腫、喉頭気管浮腫、口唇浮腫、口唇腫脹、口腔浮腫、口腔咽頭腫脹、咽頭腫脹、そう痒症、アレルギー性そう痒症、舌浮腫、1型過敏症、蕁麻疹
低用量群および高用量群で因果関係が否定できないアナフィラキシー反応の発現が認められたため、重要な特定されたリスクに設定されています。
重篤な血清カリウム値の低下(重要な特定されたリスク)
LABAを含むβ受容体刺激薬はNa+/K+ATPaseを活性化させ細胞外カリウムを細胞内へ移動させるため低カリウム血症を増悪させるおそれがあります。
国際共同第III相試験(PALLADIUM試験/CQVM149B2301試験、IRIDIUM試験/CQVM149B2302試験、QUARTZ試験/CQVM149B2303試験)では低カリウム血症は報告されていませんが、インダカテロールマレイン酸塩単剤(オンブレス)とその配合剤(ウルティブロ)では国内市販後において、重篤な血清カリウム値の低下が報告されているため、重要な特定されたリスクに設定されています。
肺炎(重要な潜在的リスク)
ICSによる肺炎リスクについて、喘息患者と比較し年齢層の高いCOPD患者におけるICS治療による肺炎のリスクの増大が示唆されています。(Calverley et al 2007,Ernst et al 2007)
| アテキュラ中用量 | アテキュラ高用量 | |
|---|---|---|
| 肺炎 | 1.0/100人年 | 0.2/100人年 |
| アテキュラ中用量 | アテキュラ高用量 | |
|---|---|---|
| 肺炎 | 1.6/100人年 | 0.7/100人年 |
- 国際共同第III相試験(QUARTZ試験/CQVM149B2303試験)のアテキュラ低用量群では肺炎の報告なし
喘息患者を対象とした4試験併合データ(PALLADIUM試験/CQVM149B2301試験、IRIDIUM試験/CQVM149B2302試験、QUARTZ試験/CQVM149B2303試験及びCQVM149B1305試験)でのアテキュラを使用した場合の肺炎の発現割合を年齢による部分集団で比較すると以下の通りです。
- 65歳未満:0.6%(13/2149例)
- 65歳以上:1.3%(5/399例)
臨床試験において特段の懸念はみらませんでしたが、COPD患者でのICS治療による肺炎のリスク増大も考慮して重要な潜在的リスクに設定されています。
副腎皮質ステロイド剤の全身作用(副腎皮質機能抑制、骨障害、眼障害等)(重要な潜在的リスク)
| アテキュラ中用量 | アテキュラ高用量 | |
|---|---|---|
| 骨密度減少 | 報告なし | 0.5/100人年 |
| 骨折 | 0.7/100人年 | 1.5/100人年 |
| 緑内障及び眼圧上昇 | 報告なし | 0.2/100人年 |
| 白内障 | 1.0/100人年 | 報告なし |
※高コルチコイド症、副腎抑制は報告なし
| アテキュラ中用量 | アテキュラ高用量 | |
|---|---|---|
| 骨密度減少 | 0.5/100人年 | 0.3/100人年 |
| 骨折 | 1.4/100人年 | 1.7/100人年 |
| 緑内障及び眼圧上昇 | 0.2/100人年 | 報告なし |
| 白内障 | 0.3/100人年 | 0.5/100人年 |
※高コルチコイド症、副腎抑制は報告なし
- 国際共同第III相試験(QUARTZ試験/CQVM149B2303試験)のアテキュラ低用量群では骨折が1.1/100人年で、高コルチコイド症及び副腎抑制、骨密度減少、緑内障及び眼圧上昇、白内障は報告なし
臨床試験では特段の懸念はみらませんでしたが、その作用による影響を考慮して重要な潜在的リスクに設定されています。
臨床試験とその成績
代表的な臨床試験データについてまとめておきます。
ノバルティスはPLATINUM臨床開発プログラムとしてQVM149(エナジア)、QMF149(アテキュラ)に関する臨床試験を行いました。
- QUARTZ試験(CQVM149B2303試験):アテキュラ低用量とアズマネックス低用量の比較
- PALLADIUM試験(CQVM149B2301試験):アテキュラ中〜高用量とアズマネックス中〜高用量(とアドエア)の比較
- IRIDIUM試験(CQVM149B2302試験):アテキュラとエナジアの比較
- ARGON試験:エナジアとアドエア+スピリーバの比較
この中で、アテキュラに関連するQUARTZ試験とPALLADIUM試験について紹介します。
QUARTZ試験(CQVM149B2303試験):アテキュラ低用量とアズマネックス低用量の比較
低用量ICSでコントロール不十分な喘息患者を対象に、MF/IA*14合剤の有効性及び安全性をツイストヘラーを用いた既承認のMF製剤を対照として比較した国際共同第Ⅲ相臨床試験です。
- 主要評価項目:投与12週後におけるトラフFEV1 のベースラインからの変化量
- 対象:802例(12歳以上18歳未満の青年期患者64例を含む)
- 1ヵ月以上にわたり低用量ICS(LABAの有無を問わない)の投与を継続
- 平均年齢 45.6歳
- 喘息の平均罹病期間 14.0年
- 気管支拡張薬投与前の平均FEV1(正常予測値に対する%)は、ベースライン時に75.1%、SABA吸入後のFEV1可逆性の平均は20.7%
- 試験デザイン:第III相、多施設共同、無作為化、12週投与、二重盲検試験
- 方法:導入期(フルチカゾンプロピオン酸100μg Accuhaler※ 1日2回投与)終了後に2群(1:1)に割り付け
- MF/IA 80/150μg ブリーズヘラー 1日1回投与群(n=398)
- MF 200μg ツイストヘラー 1日1回投与群(n=404)
※Accuhaler(アキュヘラー):日本ではディスカス
| 投与群 | MF/IA低用量群 | MF低用量群 |
|---|---|---|
| ベースライン | ||
| 投与12週後 | ||
| 投与12週後[95%信頼区間] | ||
| MF低用量群との差 [95%信頼区間] p値 | [0.148,0.217] <0.001 |
MF/IA低用量群とMF低用量群で投与12週後におけるトラフFEV1に統計学的に有意な差が認めらています。
つまり、アテキュラ吸入用カプセル低用量はアズマネックスツイストヘラー200μgと比較して有意にトラフFEV1を改善します。
PALLADIUM試験(CQVM149B2301試験):アテキュラ中〜高用量とアズマネックス中〜高用量(とアドエア)の比較
中〜高用量ICSまたは低用量のICS/LABAでコントロール不十分な喘息患者を対象に、MF/IA合剤の有効性及び安全性をツイストヘラーを用いた既承認のMF製剤を対照として比較した国際共同第Ⅲ相臨床試験です。
- 主要評価項目:投与26週後におけるトラフFEV1のベースラインからの変化量
- 対象:2,216例(12歳以上18歳未満の青年期患者107例を含む)
- スクリーニングの3ヵ月前に中用量または高用量のICS、またはLABA/ICS低用量を使用
- 気管支拡張薬投与前のFEV1が患者の予測正常値の50%以上80%未満
- 喘息コントロール質問票(ACQ-7)スコアが1.5超
- 試験デザイン:多施設共同、無作為化、52週間投与、二重盲検、トリプルダミー、並行群間比較試験
- 方法:5群(1:1:1:1:1)で割り付け
※Accuhaler(アキュヘラー):日本ではディスカス
| 投与群 | MF/IA中用量群 | MF中用量群 | MF/IA高用量群 | MF高用量群 | FP/SX群 |
| ベースライン | |||||
| 投与26週後 | |||||
| ベースラインからの変化量 | |||||
| MF中用量群との差 [95%信頼区間] 調整後p値 | [0.167,0.255] <0.001 | ||||
| MF高用量群との差 [95%信頼区間] 調整後p値 | [0.086,0.173] <0.001 |
MF/IA中用量群とMF中用量群、MF/IA高用量群とMF高用量群、それぞれの比較で投与26週後におけるトラフFEV1に統計学的に有意な差が認めらています。副次評価項目のMF/IA高用量群とFP/SX群の比較では投与26週後におけるトラフFEV1に統計的な有意差は認められませんでした。つまり、アテキュラ中用量はアズマネックス400μgと比較して、アテキュラ高用量はアズマネックス800μgと比較して、それぞれ有意にトラフFEV1を改善します。また、アテキュラ高用量はアドエア500と同等の効果を発揮します。
まとめ
まずはアテキュラ吸入用カプセルの特徴についてまとめます。
COPDの適応はないがガイドラインで対象となるACOには使用可能
吸入デバイスにはブリーズヘラーを採用
・最大呼気流量が低下している場合でも比較的使用しやすいDPI
・吸入時のカプセルの回転音、吸入後のカプセルを確認することで吸入できたかどうか確認可能
・カプセルの誤飲がないように指導が必要
1日1回 1カプセルの吸入で効果を発揮
ブリーズヘラーを吸入デバイスとする薬剤
吸入デバイスにブリーズヘラーを採用している薬剤をまとめておきます。
| 比較 | オンブレス 150μg | シーブリ 50μg | ウルティブロ | アテキュラ 低用量 | アテキュラ 中用量 | アテキュラ 高用量 | エナジア 中用量 | エナジア 高用量 |
| 適応 | COPD | COPD | COPD | 気管支喘息 | 気管支喘息 | 気管支喘息 | 気管支喘息 | 気管支喘息 |
| 用法・用量 | 1日1回 1カプセル | 1日1回 1カプセル | 1日1回 1カプセル | 1日1回 1カプセル | 1日1回 1カプセル | 1日1回 1カプセル | 1日1回 1カプセル | 1日1回 1カプセル |
| インダカテロール | 150μg | – | 110μg ※3 | 150μg | 150μg | 150μg | 150μg | 150μg |
| グリコピロニウム | – | 50μg | 50μg | – | – | – | 50μg | 50μg |
| モメタゾンフラン カルボン酸エステル | – | – | – | 80μg | 160μg | 320μg | 80μg※1 | 160μg※2 |
※1:アテキュラの160μg相当
※2:アテキュラの320μg相当
※3:オンブレスの150μg相当
ブリーズヘラセンサーでスマホと連携
ブリーズヘラーに装着するブリーズヘラセンサーというデバイスが存在するようです。
ブリーズヘラーに装着し、Bluetoothでスマホアプリ(プロペラ)と連携することで、
- 服用状況の記録
- ブリーズヘラーがどこにあるか
- 症状再燃の原因を予測
など知ることが可能になるようです。
プロペラアプリのリンクを貼っておきますね。(ブリーズヘラーセンサーがないと利用できませんが)
ライバルは?
アテキュラのライバルとなるのはアドエア、シムビコート、レルベア、フルティフォームです。こちらについても表にまとめておきますね。
| 項目 | アドエア | シムビコート | レルベア | フルティフォーム | アテキュラ | |
| デバイス | ディスカス | エアゾール | タービュヘイラー | エリプタ | エアゾール | ブリーズヘラー |
| 適応 | 気管支喘息 COPD | 気管支喘息 COPD | 気管支喘息 COPD(100のみ) | 気管支喘息 | 気管支喘息 | |
| 用法・用量 | 1日2回 1回1吸入 | 1日2回 1回2吸入 | 1日2回 1回1〜4吸入 発作時1吸入※1 | 1日1回 1回1吸入 | 1日2回 1回2〜4吸入 | 1日1回 1回1吸入 |
| 小児適応 | ◯ | なし | なし | ◯ | なし | |
| LABA※2 | サルメテロール50μg | サルメテロール25μg | ホルモテロールフマル酸塩水和物4.5µg | ビランテロール25μg | ホルモテロールフマル酸塩水和物5µg | インダカテロール150µg |
| ICS※2 | フルチカゾンプロピオン酸エステル100〜500μg | ブデソニド160µg | フルチカゾンフランカルボン酸エステル100〜200μg | フルチカゾンプロピオン酸エステル50〜125μg | モメタゾンフランカルボン酸エステル80〜320μg | |
| 薬価(1日薬価) | 100 28吸入:3039.60円/キット(217.11円) 100 60吸入:6351.10円/キット(211.70円) 250 28吸入:3497.60円/キット(249.83円) 250 60吸入:7301.50円/キット(243.38円) 500 28吸入:3912.80円/キット(279.49円) 500 60吸入:8286.10円/キット(276.20円) | 50 120吸入:6708.80円/キット(223.63円) 125 120吸入:7832.90円/キット(261.10円) 250 120吸入:8864.20円/キット(295.47円) | 30吸入:2201.50円/キット(146.77〜587.07円) 60吸入:4252.00円/キット(141.73〜566.93円) | 100 14吸入:2651.60円/キット(189.40円) 100 30吸入:5558.00円/キット(185.27円) 200 14吸入:2918.20円/キット(208.44円) 200 30吸入:6201.50円/キット(206.72円) | 50 56吸入:2502.00円/キット(178.71〜357.43円) 50 120吸入:5244.40円/キット(174.81〜349.63円) 125 56吸入:2901.20円/キット(207.23〜414.46円) 125 120吸入:6031.40円/キット(201.05〜402.09円) | 低用量:157.80円/カプセル 中用量:173.10円/カプセル 高用量:192.20円/カプセル |
※1:SMART療法
※2:1吸入中に含まれる量
LABA/ICSは広く使用されているため、様々な薬剤が存在しており、今からここに参入するのは厳しいように思えますが、ブリーズヘラーの特性を考えると高齢者等への選択肢として待ち望んでした方も少なくないのではないかと思います。個人的にも、あの患者さんやあの患者さんに提案してみたいなぁと思っていたり・・・。
アテキュラ(インダカテロール酢酸塩/モメタゾンフランカルボン酸エステル)の最新情報
m3.comに登録している方は検索機能を利用して「インダカテロール」で検索すると下記のようなアテキュラに関する最新の臨床ニュースを閲覧することができます。下記の記事ではPALLADIUM試験(MF/IND vs 中用量/高用量ICS)について紹介されています。

今後、学会や論文などで新しい報告がされればそれが記事として公開されるはずですから定期的にチェックしたいですね!もし、m3.comに未登録の方がいればここをクリックして登録をお願いします。
参考資料
- アテキュラ吸入用カプセル 添付文書 ノバルティスファーマ株式会社
- アテキュラ吸入用カプセル インタビューフォーム ノバルティスファーマ株式会社
- アテキュラ吸入用カプセル中用量/エナジア吸入用カプセル高用量に係る医薬品リスク管理計画書
- アテキュラ吸入用カプセル中用量 同吸入用カプセル高用量に関する資料 ノバルティスファーマ株式会社
- アテキュラ吸入用カプセル 審議結果報告書 医薬・生活衛生局医薬品審査管理課
- 喘息予防・管理ガイドライン2018
- 厚生労働省 平成26年患者調査(傷病分類編) 傷病別年次推移表(http://www.mhlw.go.jp/toukei/saikin/hw/kanja/10syoubyo/index.html)
- Barnes PJ, et al. How do corticosteroids work in asthma? Ann Intern Med 2003; 139: 359-70.
- Lung function, pharmacokinetics, and tolerability of indacaterol maleate and acetate in asthma patients(EMS2019)
- Naline E, et al. Eur Respir J. 2007;29:575-581.(Effect of indacaterol, a novel long-acting β2-agonist, on isolated human bronchi)
- COPD(慢性閉塞性肺疾患)診断と治療のためのガイドライン第5版
*1:ラバ、Long Acting β2 Agonist
*2:アイシーエス、Inhaled CorticoSteroids
*3:INDacaterol
*4:Mometasone Furoate
*5:Chronic Obstructive Pulmonary Disease
*6:INDacaterol
*7:GLYcopyrronium
*8:Mometasone Furoate
*9:PhosphoLipase A2
*10:Short-Acting β-Agonists
*11:Dry Powder Inhaler
*12:pressurized Metered-Dose Inhaler
*13:エイコー、Asthma and COPD Overlap
*14:Indacaterol Acetate(インダカテロール酢酸塩)
*15:Fluticasone Propionate(フルチカゾンプロピオン酸エステル)
*16:Salmeterol Xinafoate(サルメテロールキシナホ酸)