イベニティ皮下注はヒト抗スクレロスチンモノクローナル抗体であるロモソズマブ(遺伝子組換え)を有効成分とする骨粗鬆症治療薬です。
骨形成の促進と骨吸収の抑制の両方の作用を併せ持つ初めての骨粗鬆症治療薬で、急速な骨密度の改善を可能とする薬剤です。
イベニティ皮下注シリンジの概要
平成31年3月4日発売
- 医薬品名と薬価
- イベニティ皮下注105mgシリンジ:24,720.00円/筒
- 成分名:ロモソズマブ(遺伝子組換え)
- 申請者:アステラス・アムジェン・バイオファーマ
- 効能・効果:骨折の危険性の高い骨粗鬆症
- 用法・用量:通常、成人にはロモソズマブ(遺伝子組換え)として210mgを1ヵ月に1回、12ヵ月皮下投与する。
- 1日薬価:1,625円
- 加算等:
- 有用性加算(Ⅱ)(A=5%)
- 新薬創出等加算
有効成分のロモソズマブはヒト抗スクレロスチンモノクローナル抗体です。
骨形成の促進に加えて、骨吸収の抑制効果も持つ新規作用機序の薬剤です。
骨粗鬆症全般ではなく、「骨折の危険性の高い」骨粗鬆症に限定された保険適応となっています。
海外では未承認で、日本で初めて承認される薬剤です。(申請は海外が早かったのですが、承認段階で日本が先になっています)
フォルテオ皮下注キット600μg(薬価:43,334円/キット、1日薬価:1,548円)の1日薬価を元に薬価を計算、有用性加算(Ⅱ)(A=5%)が適用されています。
加算適用のため、新薬創出等加算に該当します。
骨粗鬆症とは?
骨粗鬆症は、低骨量と骨強度が低下(骨の質と量の低下)した結果、骨折リスクが増大する疾患です。
閉経後の女性に多い疾患と考えられがちですが、男性おいても重要な問題となっています。
加齢に伴い患者数が増加する疾患であるため、高齢化問題を抱える日本においては今後も患者数が増加していくことが予想されています。
日本国内における骨粗鬆症の推定患者数は2005年のデータでは約1,280万人(男性300万人、女性980万人)とされています。
骨粗鬆症により引き起こされる骨折は患者本人の負担となるだけでなく、家族・介護者へも影響し、社会的な経済的損失となります。
そのため、骨粗鬆症によって失われた骨強度を改善、骨折リスクを低下させるために様々な薬剤が開発されていますが、まだまだ十分とは言えない状況です。
スクレロスチンと骨粗鬆症治療薬ロモソズマブ
イベニティ皮下注の有効成分であるロモソズマブの働きについてまとめていきます。
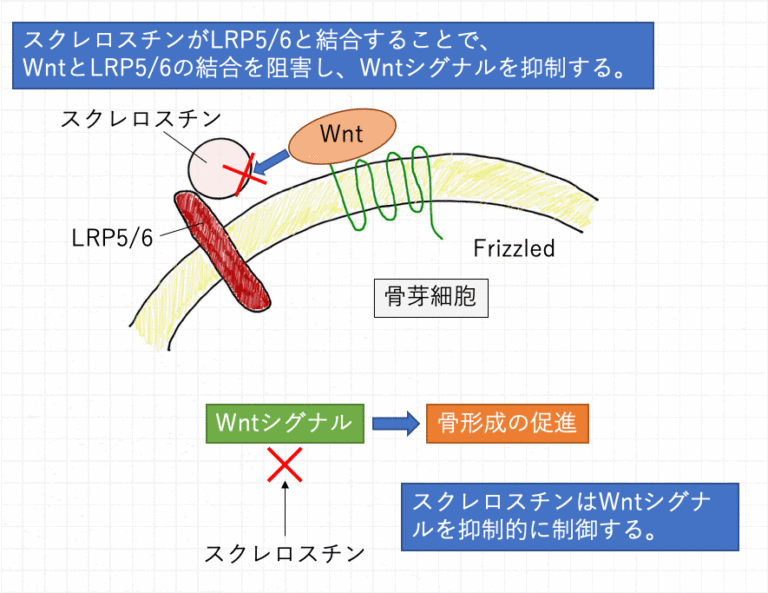
骨細胞で産生されるスクレロスチンは骨芽細胞のWnt‒βカテニンシグナル伝達を阻害することで骨芽細胞の活性を抑制、骨形成を抑制する糖タンパク質です。

また、スクレロスチンは破骨細胞を活性化させ、骨吸収を促進する働きも持っています。
ヒト抗スクレロスチンモノクローナル抗体であるロモソズマブはスクレロスチンに結合し、その働きを阻害することで骨粗鬆症に対する効果を発揮します。
ロモソズマブがスクレロスチンに結合、その働きを阻害することで、Wnt(ウィント)シグナル伝達経路が進み、骨形成は促進、骨吸収は抑制されます。

イベニティの投与により、海綿骨と皮質骨の両方の骨量が増加、骨の構造および強度が改善されることで、骨折リスクが低下すると推測されています。
デュアル・エフェクト
イベニティは骨形成促進作用・骨吸収抑制作用の両方、デュアル・エフェクトを有する薬剤です。
骨吸収抑制、骨形成促進の両作用を持つ骨粗鬆症治療薬はイベニティが初めてになるため、その効果が期待されます。
ここ数年の骨粗鬆症の治療薬の選択肢は主に以下のようになっています。
PTH製剤が唯一の骨形成促進剤で大きな効果が期待できるのですが、生涯で2年間しか使用できない(ヒトにおける骨肉腫の発生リスクが不明であるため)のが欠点です。
そのため、骨吸収抑制剤やカルシウム代謝調節剤(主に活性型ビタミンD3製剤)で治療を行い、それでも改善しない場合の最後の手段として、PTH製剤が使用されることが多いと思います。
それに対して、イベニティは「骨折の危険性の高い骨粗鬆症」という適応からわかるように、悪化してしまっている骨粗鬆症に対して、まず最初にイベニティが使用され、骨密度をある程度改善してから骨吸収抑制剤での治療に切り替えていくという使用方法が想定されます。
イベニティ皮下注のDI
を元にドラッグインフォメーションについてまとめていきたいと思います。
禁忌
イベニティ皮下注の禁忌は以下の2種類のみです。
【禁忌(次の患者には投与しないこと)】
- 本剤の成分に対し過敏症の既往歴のある患者
- 低カルシウム血症の患者[低カルシウム血症が悪化するおそれがある(「重要な基本的注意」及び「重大な副作用」の項参照)]
引用元:イベニティ皮下注 添付文書
1つ目の過敏症の既往歴はさておき、気をつけたいのは2番目の低カルシウム血症です。
でも、これも当然ですよね。
骨形成を促進(血中のカルシウムを使用)して、骨吸収を抑制(骨から血中にカルシウムが溶け出すのを防ぐ)わけですから。
RMP:過敏症
イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
の「重要な特定されたリスク」に過敏症についての記載があります。
過敏症
全てのモノクローナル抗体にはアナフィラキシーを含む過敏反応の潜在的なリスクがある。ロモソズマブ群はプラセボ群より過敏症関連事象の発現割合は低かったが、ロモソズマブと血管浮腫、多形紅斑、発疹、皮膚炎、蕁麻疹を含む過敏症関連事象との関連性が示されていること、過敏症に関連する重篤な有害事象及び投与中止に至った事象がロモソズマブ群でプラセボ群と比較して多く認められていること、市販予定製剤(90mg/mL製剤)において臨床試験用製剤(70mg/mL製剤)よりも多く認められていることから、過敏症を重要な特定されたリスクとした。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
モノクローナル抗体である以上、過敏症は避けて通れません。
RMP:低カルシウム血症
低カルシウム血症もイベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書の「重要な特定されたリスク」に記載されています。
低カルシウム血症
ロモソズマブによるスクレロスチン阻害により、投与初期に急激に骨量が増加し、カルシウムなどの骨形成に関与する基質に対する需要が大きくなることから血清カルシウム濃度が減少する可能性がある。国内外の臨床試験データでロモソズマブを投与された被験者にアルブミン補正血清カルシウム値でグレード1及び2を示した被験者が認められたこと、重度の腎機能障害者又は末期腎不全患者では低カルシウム血症の患者が認められたこと、悪化した場合重篤な転帰を辿る可能性があることから低カルシウム血症を重要な特定されたリスクとした。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
さらに、これに関連して添付文書の重要な基本的注意には以下の記載があります。
【使用上の注意】
2.重要な基本的注意
- 低カルシウム血症やマグネシウム、intact-PTH等の骨・ミネラル代謝異常がある場合には、本剤投与前にあらかじめ治療すること。[「禁忌」、「慎重投与」及び「重大な副作用」の項参照]
- 本剤投与中は適切なカルシウム及びビタミンDの補給を行うこと。本剤投与後に血清カルシウム値が低下する可能性があるので、低カルシウム血症の徴候や症状がないか観察し、血清カルシウム値に注意すること。なお、臨床試験では、 本剤投与後2週間から1ヵ月の時点で血清カルシウム値の低下が認められている。[「禁忌」、「慎重投与」及び「重大な副作用」の項参照]
引用元:イベニティ皮下注 添付文書
骨密度改善効果が期待できる分、低カルシウム血症への注意も必要となりますね。
デノタスチュアブルが使用できれば都合がいいですが適応外(デノタスチュアブルの適応はRANKL阻害剤投与の低カルシウム血症の治療・予防)なのでエディロールを併用するのが基本になるのかな?
効能・効果
【効能・効果】
骨折の危険性の高い骨粗鬆症
〈効能・効果に関連する使用上の注意〉
- 本剤の適用にあたっては、低骨密度、既存骨折、加齢、大腿骨頸部骨折の家族歴等の骨折の危険因子を有する患者を対象とすること。
- 海外で実施されたアレンドロン酸ナトリウムを対照とした比較試験において、心血管系事象(虚血性心疾患又は脳血管障害)の発現割合がアレンドロン酸ナトリウム群に比較して本剤群で高い傾向が認められている。本剤の投与にあたっては、本剤のベネフィットとリスクを十分に理解した上で、適用患者を選択すること。[「重要な基本的注意」、「その他の注意」及び【臨床成績】の項参照]
引用元:イベニティ皮下注 添付文書
心血管リスクが非常に気になるところです・・・。
重要な基本的注意には以下のように記載されています。
【使用上の注意】
2.重要な基本的注意
- 虚血性心疾患又は脳血管障害のリスクが高い患者への投与は有益性と危険性を考慮して判断すること。また、投与する場合には、虚血性心疾患及び脳血管障害の徴候や症状を患者に説明し、徴候や症状が認められた場合は、速やかに医療機関を受診するよう指導すること。[「効 能・効果に関連する使用上の注意」及び「その他の注意」の項参照]
引用元:イベニティ皮下注 添付文書
RMP:重篤な心血管系事象
イベニティの心血管リスクについて、以下のようなコメントを見つけました。
浜谷 重篤な心血管系有害事象の発現率に関して、プラセボ対照で実施した「FRAME試験」(7180例、うち日本人492例)ではイベニティ群とプラセボ群で不均衡は認められなかったのですが、標準治療薬アレンドロネート(アレンドロン酸ナトリウム)を対照として欧州で実施した「ARCH試験」(4093例、日本人の登録なし)ではイベニティ群2.5%、アレンドロネート群1.9%と不均衡が認められました。
アレンドロネートを含むビスホスホネート製剤では以前より心血管系事象を低下させるという報告が散見され、他の骨粗鬆症治療薬の臨床試験データや疫学データと比較すると、イベニティ群の発現率は同等かむしろ低い。臨床医の先生方にはその辺りの事実を正確にお伝えしていきたいと考えています。
引用元:〈骨形成促進〉と〈骨吸収抑制〉両方の作用を持つイベニティは、骨粗鬆症治療の「最終兵器」【Breakthrough 医薬品研究開発の舞台裏】(web医事新報 2019/04/26)
このコメントが正しいのであればそこまで心配は不要なのか?
イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書の「重要な潜在的リスク」に「重篤な心血管系事象」について記載されています。
重篤な心血管系事象
大動脈及び血管の石灰化巣にスクレロスチンの発現が確認されたため、ロモソズマブによるスクレロスチンの阻害は、血管の石灰化を促進又は悪化させる理論的な懸念がある。しかし、スクレロスチン発現の欠如または低下により全身性の骨形成促進を示す硬結性骨化症又はvan Buchem病患者において、血管石灰化又は心血管疾患の早期発症の増加は報告されていない。 また、非臨床試験データではロモソズマブが心血管系の機能又は心血管系事象発現には影響していないことが示唆されている。しかしながら、重篤な心血管系事象についてプラセボを対照とした20070337試験(日本人含む)ではプラセボとの不均衡は示されなかったが、アレンドロネートを対照とした20110142試験(日本人は含まない)では不均衡が認められたため重要な潜在的リスクとした。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
プラセボとの差はなかったので、アレンドロネートの差が問題というよりは、理論上起こりうるものであるということが懸念材料なのかもしれませんね。
やはり新規作用機序、かつ海外で未承認の薬剤である以上、慎重になるべきところだと思います。
海外での審査でどう評価されるか気になるところですね。
重篤な脳・心血管系事象についての注意喚起
2019年7月24日、アステラス・アムジェン・バイオファーマとアステラス製薬からイベニティ皮下注の重篤な脳・心血管系事象について、「適正使用のお願い」を発出し、注意喚起を行いました。
これは販売開始3ヶ月間で重篤な脳・心血管疾患が11例報告、因果関係が否定できない心血管事象による死亡が1例含まれていたことを受けてのものです。
基本的には上にもまとめている添付文書に記載されている内容の再確認による注意喚起となっています。
まとめると以下の通りです。
- WHO による重症骨粗鬆症の定義等を参考に「骨折の危険性の高い」骨粗鬆症患者に対して使用する
- 虚血性心疾患又は脳血管障害のリスクが高い患者への投与は有益性と危険性を考慮して使用を判断
- 他の医療機関で虚血性心疾患又は脳血管障害の治療中、もしくはそれらの発現リスクが高い疾患の治療中である場合には、互いに連携し、処方の必要性を慎重に判断
- 虚血性心疾患及び脳血管障害の徴候や症状を患者に説明し、徴候や症状が認められた場合には速やかに医療機関を受診するよう患者への指導を実施(イベニティ皮下注 105mgシリンジの患者カードの携帯・提示の指導)
参考として、米国ではBoxed Warningとして以下の通り記載されています。
米国添付文書(Boxed Warning:心筋梗塞、脳卒中及び心血管死の潜在的リスク)
- 本剤により心筋梗塞、脳卒中及び心血管死のリスクが増大するおそれがある
- 過去 1 年以内に心筋梗塞又は脳卒中の既往を有する患者には、本剤の投与を開始すべきでない。その他の心血管系リスクファクターを有する患者については、有益性と危険性を考慮して判断すること
- 本剤投与中に心筋梗塞又は脳卒中が発現した場合は、本剤の投与を中止すべきである
イベニティ皮下注処方時の留意事項
効能・効果および用法・用量に関わる留意事項について通知が出されています。
2 薬価基準の一部改正に伴う留意事項について
(6)イベニティ皮下注105mgシリンジ
- 本製剤の効能・効果に関連する使用上の注意に、「本剤の適用にあたっては、低骨密度、既存骨折、加齢、大腿骨頸部骨折の家族歴等の骨折の危険因子を有する患者を対象とすること。」と記載されているので、使用に当たっては十分留意すること。
- 本製剤の用法・用量に「1ヵ月に1回、12ヵ月皮下投与する」とされ、これに関連する使用上の注意に、「本剤の骨折抑制効果は12ヵ月の投与で検証されており、12ヵ月を超えた投与では検討されていない。また、本剤投与終了後に原則として適切な骨粗鬆症薬による治療を継続すること。」と記載されているので、使用に当たっては十分留意すること。
- 本製剤を12ヵ月投与した後に本製剤を再投与する場合、再投与開始に当たっては、次の事項を診療報酬明細書の摘要欄に記載すること。
- ア 骨折の危険性が高いと判断した理由
- イ 本製剤を再投与するまでに投与した骨粗鬆症治療薬の品名
「低骨密度、既存骨折、加齢、大腿骨頸部骨折の家族歴等の骨折の危険因子を有する患者」は特に具体的に明記されていません。
基本的に12ヶ月の使用になり、再投与については、それまでに使用した薬品名のレセプト記載が必要となります。
用法・用量
【用法・用量】
通常、成人にはロモソズマブ(遺伝子組換え)として210mgを1ヵ月に1回、12ヵ月皮下投与する。
〈用法・用量に関連する使用上の注意〉
- 本剤の骨折抑制効果は12ヵ月の投与で検証されており、12ヵ月を超えた投与では検討されていない。また、本剤投与終了後に原則として適切な骨粗鬆症薬による治療を継続すること。
- ロモソズマブ(遺伝子組換え)210mgを投与するために、本剤2本を皮下に投与すること。
- 本剤の投与が予定から遅れた場合は可能な限り速やかに投与を行い、以後、その投与を基点とし、1ヵ月間隔で投与すること。
引用元:イベニティ皮下注 添付文書
1回に2本の投与なんですね。
イベニティには12カ月の投与制限がありますが、PTH製剤の生涯24カ月投与制限とは異なり、連続12カ月の投与制限で、生涯にわたって制限するものではありません。
慎重投与
【使用上の注意】
1.慎重投与(次の患者には慎重に投与すること)
重度の腎機能障害患者(eGFRが30mL/min/1.73m2未満)あるいは透析を受けている患者[低カルシウム血症が発現しやすい(「重要な基本的注意」、「重大な副作用」の項参照)] 引用元:イベニティ皮下注 添付文書
薬剤の性質上、腎機能障害患者に注意が必要なのは当然ですね。
RMP:腎機能障害患者における安全性
イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
の「重要な不足情報」に腎機能障害患者における安全性について記載されています。
腎機能障害患者における安全性
腎機能障害者では 1,25(OH)2 ビタミンDの産生能が低下しうることを踏まえると、ロモソズマブ投与による低カルシウム血症のリスクが高まること、及び腎機能障害患者のうち、特に透析を要する患者では、一般に血管石灰化のリスクが高いことが想定される。 臨床試験における重度腎機能障害患者及び末期腎不全患者への投与例数が少ないことから重要な不足情報とした。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
重要な基本的注意
1〜3はすでに触れているのでそれ以降について。
【使用上の注意】
2.重要な基本的注意
- 本剤による投与終了後、骨吸収が一過性に亢進したことから、本剤の治療を終了又は中止する場合には、本剤治療終了後又は中止後に骨吸収抑制薬の使用を考慮すること。[「臨床成績」の項参照]
- 顎骨壊死・顎骨骨髄炎があらわれることがあるので、以下の点に留意すること。[「重大な副作用」の項参照]
- リスク因子としては、悪性腫瘍、化学療法、血管新生阻害剤、コルチコステロイド治療、放射線療法、口腔の不衛生、歯科処置の既往等が知られている。
- 本剤の投与前は、口腔内の管理状態を確認すること。また、患者に対し、必要に応じて、適切な歯科治療を受け、侵襲的な歯科処置をできる限り済ませておくよう指導すること。
- 患者に対し、本剤投与中は口腔内を清潔に保つこと、定期的な歯科検査を受けること、歯科受診時に本剤の使用を歯科医師に告知することを説明し、異常が認められた場合には歯科又は口腔外科を受診するよう指導すること。
- 本剤投与中に顎骨壊死を発症した又は発症の疑いのある患者に対し、歯科又は口腔外科を受診するよう指導すること。
- 本剤の中止は本剤の有益性と危険性を考慮して判断すること。
- 骨吸収抑制作用を有するビスホスホネート系薬剤を長期使用している患者において、非外傷性の大腿骨転子下及び近位大腿骨骨幹部の非定型骨折が発現したとの報告がある。これらの報告では、完全骨折が起こる数週間から数ヵ月前に大腿部や鼠径部等において前駆痛が認められている報告もあることから、このような症状が認められた場合には、X線検査等を行い、適切な処置を行うこと。また、両側性の骨折が生じる可能性があることから、片側で非定型骨折が起きた場合には、反対側の大腿骨の症状等を確認し、X線検査を行うなど、慎重に観察すること。 X線検査時には骨皮質の肥厚等、特徴的な画像所見がみられており、そのような場合には適切な処置を行うこと。[「重大な副作用」の項参照]
引用元:イベニティ皮下注 添付文書
効能・効果の部分に記載しましたが、やはり心血管リスクについては十分考慮する必要があります。
RMP:治療終了・中止後の安全性
投与終了後の骨吸収の一過性亢進が見られるということなので、12カ月経過後にはデスノマブやBP製剤に切り替える必要がありますね。
イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書の「重要な潜在的リスク」に治療終了・中止後の安全性について記載されています。
治療終了・中止後の安全性
臨床試験でロモソズマブ投与終了後において一過性の骨吸収の亢進が認められていること、他の骨吸収抑制作用を有する抗体製剤において治療中止後に一過性の骨吸収の亢進、並びに多発性椎体骨折のリスク増加が認められたとの報告があること等を踏まえ、治療終了・中止後の安全性を重要な潜在的リスクに設定した。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
RMP:顎骨壊死
顎骨壊死・顎骨骨髄炎、いわゆる薬剤関連顎骨壊死(MRONJ*3)です。
以前はビスホスホネート関連顎骨壊死(BRONJ*4)と呼ばれていましたね。
イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書の「重要な潜在的リスク」に顎骨壊死について記載されています。
顎骨壊死
骨吸収抑制薬の使用に伴い、顎骨壊死(osteonecrosis of the jaw:ONJ)が認められている。 ONJの病因は明らかでないが、ロモソズマブには骨吸収抑制作用があることから理論的には侵襲的歯科治療後や歯牙破折での骨修復の妨げとなり、それ自身又はそれに未知のメカニズムが加わることでONJを発現するリスクとなる可能性があるため重要な潜在的リスクとした。
非臨床データの所見では、ロモソズマブに生涯曝露されたラットにおける歯疾患及び炎症は、壊死骨の露出といったようなONJ様所見を示さなかった。抗スクレロスチン抗体投与は限局性歯周炎の卵巣摘出ラットモデルで歯槽骨頂部の高さ及び骨量を増加させた。骨折治癒モデルでは、傷害に応じた局所の破骨細胞活性は、ビスホスホネート及び RANKL 阻害剤と比較して、抗スクレロスチン抗体投与により良好に維持された。
日本人集団(20070337試験)において、12カ月間のプラセボ対照解析対象集団ではONJと判 定された被験者はいなかった。しかし、本試験の本剤投与群の二重盲検期間後にONJが1例認められた。この症例は、非重篤な歯周炎の有害事象の既往のある被験者で、二重盲検期間後のデノスマブを1回投与後にONJを発現した。本事象はデノスマブによる副作用と判断さ れ、二重盲検期に投与された本剤との因果関係は否定された。また、20101291試験ではONJの疾患判定は行われなかったが、事象としてONJは報告されていない。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
MRONJの発現を完全には否定できないかな・・・と言ったところですが、BP薬やデスノマブほどのリスクはないのかな?
RMP:非定型大腿骨骨折
大腿骨転子下及び近位大腿骨骨幹部の非定型骨折は重要な基本的注意に記載されている通りです。
イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書の「重要な潜在的リスク」に非定型大腿骨骨折について記載されています。
非定型大腿骨骨折
国内外の臨床データでは少数例ではあるがロモソズマブ群で非定型大腿骨骨折(atypical femoral fracture:AFF)が認められていること、ロモソズマブは、骨吸収抑制活性を含むデュアル・エフェクトを有するため、AFFのリスクが増加する懸念があることから AFFを重要な潜在的リスクとした。
日本人集団(20070337試験)において、12カ月間のプラセボ対照解析対象集団ではAFFと判定された症例はなかった。20101291試験ではAFFの疾患判定は行われなかったが、事象としてAFFは報告されていない。
国内外の臨床試験データでは右大腿骨骨幹部を骨折しグレード3(重度)として報告された1例がAFFと判定された。このAFFは、ロモソズマブ3.5カ月間投与後に発症したこと、及び治験開始前に骨折部位に前駆痛の既往歴があったことから、スクリーニング時にビタミンDが低値だったこの被験者では特発性事象である可能性が高かった。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
副作用
これまでに出てきたもの以外で特に特徴的な副作用はありません。
副作用
骨粗鬆症患者を対象とした主要なプラセボ対照 国際共同第III相試験(20070337試験及び20110174試験)で本剤の投与を受けた3744例中615例(16.4%)に臨床検査値異常を含む副作用が認められた。主な副作用は、関節痛(1.9%)、注射部位疼痛(1.3%)、注射部位紅斑(1.1%)、鼻咽頭炎(1.0%)で あった。(承認時)
引用元:イベニティ皮下注 添付文書
重大な副作用はこれまでにまとめた通りです。
重大な副作用
- 低カルシウム血症(頻度不明):QT延長、痙攣、テタニー、しびれ、失見当識等を伴う低カルシウム血症があらわれることがあるので、観察を十分に行うこと。低カルシウム血症が認められた場合には、カルシウム及びビタミンDの補充に加えて、緊急時には、カルシウムの点滴投与を併用するなど、適切な処置を速やかに行うこと。[「重要な基本的注意」の項参照]
- 顎骨壊死・顎骨骨髄炎(頻度不明):顎骨壊死・顎骨骨髄炎があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど、適切な処置を行うこと。[「重要な基本的注意」の項参照]
- 大腿骨転子下及び近位大腿骨骨幹部の非定型骨折(頻度不明):大腿骨転子下及び近位大腿骨骨幹部の非定型骨折を生じることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど、適切な処置を行うこと。[「重要な基本的注意」の項参照]
引用元:イベニティ皮下注 添付文書
そのほか想定されるリスク(RMP)
RMPに記載されている内容をまとめておきます。
過骨症
神経障害を伴う過骨症は、硬結性骨化症及びvan Buchem病の特徴である。過骨症の可能性のある事象の発現割合は低いが、ロモソズマブによる骨形成促進が骨の肥厚に関与する可能性があるため重要な潜在的なリスクとした。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
胎児へのリスク
ロモソズマブの治療対象(男性及び閉経後の女性)とは関係性は低いが、ヒト胎児の発育に低いながらもリスクが存在することから胎児へのリスクを重要な潜在的リスクとした。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
抗体産生の影響
抗体には、医薬品の活性の低下や消失、内因性分子の中和、過敏反応などの種々の作用がある。抗ロモソズマブ抗体の臨床的重要性は明らかではなく、臨床試験において抗ロモソズマ ブ抗体出現による有効性、安全性への影響は認められていない。しかしながら、抗ロモソズマブ抗体産生が生体へ潜在的に影響する可能性が考えられることから抗体産生の影響を重要な潜在的リスクとした。
引用元:イベニティ皮下注105mgシリンジに係る医薬品リスク管理計画書
治療終了後の骨吸収の亢進はしっかりと覚えておかないといけませんね。
骨粗鬆症治療薬一覧
イベニティ登場前の骨粗鬆症治療薬を一覧表にしました。(参考:骨粗鬆症の予防と治療ガイドライン2015年版)
将来的にはロモソズマブ(イベニティ)も追加されることになります。
表中のA〜Cは有効性の評価です。
- 骨密度上昇
- A:上昇効果がある
- B:上昇するとの報告がある
- C:上昇するとの報告はない
- 骨折発生抑制効果
- A:抑制する
- B:抑制するとの報告がある
- C:抑制するとの報告はない
| 治療薬 | 骨密度 | 錐体骨折 | 非錐体骨折 | 大腿骨近位部骨折 | 疼痛改善 | |
|---|---|---|---|---|---|---|
| カルシウム剤 | B | B | B | C | – | |
| 女性ホルモン | 結合型エストロゲン | A | A | A | A | – |
| エストラジオール | A | B | B | C | – | |
| 活性型ビタミンD3製剤 | アルファカルシドール カルシトリオール | B | B | B | C | – |
| エルデカルシドール | A | A | B | C | – | |
| ビタミンK2製剤 | メナテトレノン | B | B | B | C | – |
| ビスホスホネート薬 | エチドロネート | A | B | C | C | – |
| アレンドロネート リセドロネート | A | A | A | A | – | |
| ミノドロン酸 | A | A | C | C | – | |
| イバンドロネート | A | A | B | C | – | |
| SERM | ラロキシフェン | A | A | B | C | – |
| バゼドキシフェン | A | A | B | C | – | |
| カルシトニン製剤 | B | B | C | C | A | |
| 副甲状腺ホルモン | テリパラチド | A | A | A | C | – |
| テリパラチド酢酸塩 | A | A | C | C | – | |
| 坑RANKL抗体 | デスノマブ | A | A | A | A | – |
まとめ
この10年の骨粗鬆症治療薬の進歩は凄まじいものがありますね。
ヒト抗スクレロスチンモノクローナル抗体。
ついに、骨吸収抑制と骨形成促進の両方の作用を持つ製剤の登場です。
スクレロスチンという糖タンパク質をターゲットとする新たな作用機序を持つ薬剤です。
その効果に期待する一方で、有害事象についても慎重にならざるを得ません。
実際、心血管リスクについては注意喚起が行われました。
今後、詳細なメカニズムが解明され、薬剤の立ち位置が決まってくるとは思うのですが、既存の薬剤と含めて頭の中を整理しておかなければいけませんね。